Aktīvās sastāvdaļas: rituksimabs
MabThera 100 mg koncentrāts infūziju šķīduma pagatavošanai
Mabthera iepakojuma ieliktņi ir pieejami šādu izmēru iepakojumiem:- MabThera 100 mg koncentrāts infūziju šķīduma pagatavošanai
- MabThera 500 mg koncentrāts infūziju šķīduma pagatavošanai
- MabThera 1400 mg šķīdums zemādas injekcijām
Indikācijas Kāpēc lieto Mabthera? Kam tas paredzēts?
Kas ir MabThera
MabThera satur aktīvo vielu “rituksimabu”, proteīna veidu, ko sauc par “monoklonālo antivielu”, kas saistās ar noteiktu balto asins šūnu virsmu, ko sauc par B limfocītiem. Kad rituksimabs saistās ar šo šūnu virsmu, tās nogalina.
Kāpēc lieto MabThera
MabThera var lietot dažādu slimību ārstēšanai pieaugušajiem. Ārsts var izrakstīt MabThera, lai ārstētu:
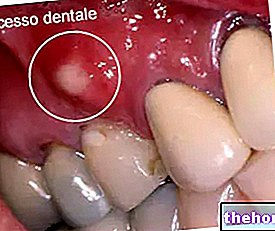
a) Ne-Hodžkina limfoma
Ne-Hodžkina limfoma ir limfātisko audu (imūnsistēmas daļa) slimība, kurā iesaistīti B limfocīti-īpašs balto asins šūnu veids.
MabThera var lietot monoterapijā (atsevišķi) vai kopā ar citām zālēm, ko kopā sauc par “ķīmijterapiju”.
Pacientiem, kuru ārstēšana izrādās efektīva, MabThera var lietot kā uzturošo terapiju 2 gadus pēc sākotnējās ārstēšanas pabeigšanas.
b) Hroniska limfas leikēmija
Hroniska limfoleikoze (CLL) ir visizplatītākā pieaugušo leikēmijas forma. HLL ietver noteiktu limfocītu - B šūnu, kuras izcelsme ir kaulu smadzenēs un nobriest limfmezglos. Pacientiem ar HLL ir pārāk daudz patoloģisku limfocītu, kas kļūst par tiem uzkrājas galvenokārt kaulu smadzenēs un asinīs.Šo patoloģisko B limfocītu proliferācija ir iespējamo simptomu cēlonis.MabThera kombinācijā ar ķīmijterapiju iznīcina šīs šūnas, kuras bioloģiski procesi pakāpeniski izvada no organisma.
c) reimatoīdais artrīts
MabThera lieto reimatoīdā artrīta ārstēšanai.Reimatoīdais artrīts ir slimība, kas skar locītavas. B limfocīti ir atbildīgi par dažiem jūsu simptomiem. MabThera lieto reimatoīdā artrīta ārstēšanai cilvēkiem, kuri ir izmēģinājuši citas zāles, bet ir pārstājuši darboties, nedarbojās pietiekami labi vai izraisīja blakusparādības. MabThera parasti lieto kopā ar citām zālēm, ko sauc par metotreksātu. MabThera palēnina locītavu bojājumus, ko izraisa reimatoīdais artrīts un palielina spēju veikt parastās ikdienas darbības.
Vislabākā reakcija uz MabThera ir novērota tiem, kam ir pozitīvs asins tests attiecībā uz reimatoīdo faktoru (RF) un / vai anticiklisko citrulināto peptīdu (anti-CCP). Abi testi parasti ir pozitīvi reimatoīdā artrīta gadījumā un palīdz apstiprināt diagnozi.
d) Granulomatoze ar poliangiītu un mikroskopisku poliangiītu
MabThera lieto granulomatozes remisijas ierosināšanai ar poliangiītu (oficiāli saukta par Vīgenera slimību) vai mikroskopisku poliangiītu kopā ar glikokortikoīdiem. Granulomatoze ar poliangiītu un mikroskopisks poliangiīts ir divi asinsvadu iekaisuma veidi, kas galvenokārt skar plaušas un nieres, bet var ietekmēt arī citus orgānus.B limfocīti ir iesaistīti šo apstākļu cēloņos.
Kontrindikācijas Kad Mabthera nedrīkst lietot
Nelietojiet MabThera šādos gadījumos:
- ja Jums ir alerģija pret rituksimabu, citiem rituksimabam līdzīgiem proteīniem vai kādu citu (6. punktā minēto) šo zāļu sastāvdaļu;
- ja Jums pašlaik ir "smaga aktīva infekcija;
- ja imūnsistēma ir vāja;
- ja Jums ir smaga sirds mazspēja vai smaga nekontrolēta sirds slimība un Jums ir reimatoīdais artrīts, granulomatoze ar poliangiītu vai mikroskopisks poliangiīts.
Nelietojiet MabThera, ja kaut kas no iepriekš minētā attiecas uz jums. Ja neesat pārliecināts, pirms MabThera lietošanas konsultējieties ar ārstu, farmaceitu vai medmāsu.
Piesardzība lietošanā Kas jāzina pirms Mabthera lietošanas
Pirms MabThera lietošanas konsultējieties ar ārstu, farmaceitu vai medmāsu:
- ja Jums agrāk ir bijusi hepatīta infekcija vai tā var būt arī tagad, jo dažos gadījumos MabThera var izraisīt B hepatīta atkārtotu aktivāciju, kas ļoti retos gadījumos var būt letāla. Ārsts rūpīgi uzraudzīs pacientus ar B hepatīta infekciju, lai konstatētu šīs infekcijas pazīmes;
- ja Jums kādreiz ir bijušas sirds problēmas (piemēram, stenokardija, sirdsklauves vai sirds mazspēja) vai ir bijušas elpošanas problēmas.
Ja kaut kas no iepriekš minētā attiecas uz jums (vai ja neesat pārliecināts), pirms MabThera lietošanas konsultējieties ar ārstu, farmaceitu vai medmāsu. Jūsu ārstam, iespējams, būs jāpievērš īpaša uzmanība MabThera lietošanas laikā.
Ja Jums ir reimatoīdais artrīts, granulomatoze ar poliangiītu vai mikroskopisks poliangiīts, konsultējieties ar savu ārstu
- ja domājat, ka Jums ir infekcija, pat viegla kā saaukstēšanās.Šūnas, kuras ir skārusi MabThera, izmanto, lai cīnītos ar infekcijām, un pirms MabThera lietošanas jāgaida, līdz infekcija ir izzudusi. Pastāstiet arī savam ārstam, ja Jums agrāk ir bijušas daudzas infekcijas vai ja Jums ir smagas infekcijas;
- ja jūs domājat, ka tuvākajā laikā jums būs nepieciešama kāda vakcinācija, ieskaitot vakcinācijas, kas nepieciešamas, lai ceļotu uz citām valstīm. Dažas vakcīnas nedrīkst ievadīt vienlaikus ar MabThera vai mēnešos pēc MabThera lietošanas. Pirms MabThera lietošanas ārsts apsvērs, vai jūs varat vakcinēties.
Bērni un pusaudži
Pirms šo zāļu lietošanas konsultējieties ar ārstu, farmaceitu vai medmāsu, ja jūs vai jūsu bērns ir jaunāki par 18 gadiem, jo pašlaik nav daudz informācijas par MabThera lietošanu bērniem un pusaudžiem.
Mijiedarbība Kādas zāles vai pārtikas produkti var mainīt Mabthera iedarbību
Pastāstiet ārstam, farmaceitam vai medmāsai par visām zālēm, kuras lietojat, pēdējā laikā esat lietojis vai varētu lietot, ieskaitot bezrecepšu zāles un augu izcelsmes zāles, jo MabThera var ietekmēt dažu zāļu iedarbību un otrādi.
Īpaši pastāstiet ārstam:
- ja lietojat zāles hipertensijas ārstēšanai. Jums var lūgt pārtraukt šo zāļu lietošanu 12 stundas pirms MabThera lietošanas, jo dažiem cilvēkiem MabThera lietošanas laikā pazeminās asinsspiediens;
- ja agrāk esat lietojis zāles, kas ietekmē imūnsistēmu, piemēram, ķīmijterapiju vai imūnsupresīvas zāles.
Ja kaut kas no iepriekš minētā attiecas uz jums (vai ja neesat pārliecināts), pirms MabThera lietošanas konsultējieties ar ārstu, farmaceitu vai medmāsu.
Brīdinājumi Ir svarīgi zināt, ka:
Grūtniecība, zīdīšanas periods un auglība
Jums jāpastāsta ārstam vai medmāsai, ja esat grūtniece, Jums ir aizdomas vai plānojat grūtniecību, jo MabThera var šķērsot placentu un ietekmēt bērnu.
Ja pastāv grūtniecības iestāšanās iespēja, jums un jūsu partnerim MabThera terapijas laikā un 12 mēnešu laikā pēc pēdējās MabThera terapijas saņemšanas būs jāizmanto efektīva kontracepcijas metode.
MabThera var nokļūt mātes pienā, tāpēc terapijas laikā ar šīm zālēm un 12 mēnešus pēc pēdējās ārstēšanas ar MabThera nedrīkst barot bērnu ar krūti.
Transportlīdzekļu vadīšana un mehānismu apkalpošana
Nav zināms, vai MabThera ietekmē spēju vadīt transportlīdzekļus un apkalpot mehānismus.
Devas un lietošanas veids Kā lietot Mabthera: Devas
Administrācija
MabThera Jums ievadīs ārsts vai medicīnas māsa, kam ir pieredze šīs terapijas lietošanā. Viņi rūpīgi uzraudzīs Jūs šo zāļu lietošanas laikā, lai atklātu jebkādas blakusparādības.
MabThera vienmēr ievadīs pilienu pa pilienam infūzijas veidā vēnā (intravenoza infūzija).
Zāles, kas ievadītas pirms katras MabThera infūzijas
Pirms MabThera infūzijas Jums tiks ievadītas citas zāles (premedikācija), lai izvairītos vai samazinātu iespējamo blakusparādību rašanos.
Cik daudz un cik bieži jūs saņemsiet terapiju
a) Ja Jums tiek ārstēta ne-Hodžkina limfoma
- Ja Jums tiek ievadīts tikai MabThera
MabThera Jums tiks ievadīts reizi nedēļā 4 nedēļas. Ir iespējami atkārtoti ārstēšanas kursi ar MabThera.
- Ja Jums tiek dota MabThera kombinācijā ar ķīmijterapiju
Jūs saņemsiet MabThera tajā pašā dienā, kad saņemat ķīmijterapiju; to ievadīšana parasti notiek ik pēc 3 nedēļām, ne vairāk kā 8 reizes
- Ja jūs labi reaģējat uz ārstēšanu, MabThera Jums var ievadīt kā uzturošo terapiju ik pēc 2 līdz 3 mēnešiem divus gadus. Pamatojoties uz jūsu reakciju uz zālēm, ārsts var mainīt šo lietošanas režīmu.
b) ja Jums tiek ārstēta hroniska limfoleikoze
Ja Jūs ārstējat ar MabThera kombinācijā ar ķīmijterapiju, Jūs saņemsiet MabThera infūzijas 1. cikla 0. dienā, pēc tam katra cikla 1. dienā kopumā 6 ciklus. Katrs cikls ilgst 28 dienas. Pēc MabThera infūzijas jāveic ķīmijterapija.Ārsts izlems, vai Jums vienlaikus jālieto atbalstoša terapija.
c) ja Jums tiek ārstēts reimatoīdais artrīts
Katrs ārstēšanas cikls sastāv no divām atsevišķām infūzijām, kas tiek ievadītas ar 2 nedēļu intervālu. Ir iespējami atkārtoti ārstēšanas kursi ar MabThera. Pamatojoties uz jūsu slimības pazīmēm un simptomiem, ārsts izlems, kad veikt turpmākus kursus. Tas varētu notikt vairāku mēnešu laikā.
d) ja Jums tiek ārstēta granulomatoze ar poliangiītu vai mikroskopisku poliangiītu
Ārstēšana ar MabThera ietver četras atsevišķas infūzijas ar iknedēļas intervālu. Pirms ārstēšanas uzsākšanas ar MabThera kortikosteroīdus ievadīs injekciju veidā. Ārsts jebkurā laikā var uzsākt kortikosteroīdu lietošanu iekšķīgi, lai ārstētu Jūsu stāvokli.
Ja jums ir kādi jautājumi par šo zāļu lietošanu, jautājiet savam ārstam, farmaceitam vai medmāsai.
Blakusparādības Kādas ir Mabthera blakusparādības
Tāpat kā citas zāles, šīs zāles var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas.
Lielākā daļa blakusparādību ir vieglas vai vidēji smagas, bet dažos gadījumos tās var būt smagas un tām nepieciešama ārstēšana. Reti dažas no šīm reakcijām ir bijušas letālas.
Infūzijas reakcijas
Pirmās infūzijas laikā vai pirmo 2 stundu laikā pēc tās var parādīties drudzis, drebuļi un trīce.Retāk dažiem pacientiem var būt sāpes infūzijas vietā, pūslīšu veidošanās, ādas nieze, savārgums, nogurums, galvassāpes, apgrūtināta elpošana, mēles vai rīkles pietūkums, kairinājums vai iesnas, vemšana, siltums vai siltums. Sirdsklauves, sirdslēkme vai samazināšanās trombocītu skaitā. Ja Jums ir sirds slimība vai stenokardija, šīs reakcijas var pasliktināties. Ja Jums rodas kāds no šiem simptomiem, nekavējoties informējiet par to infūzijas ievadītāju, jo infūzijas ātrumu var būt nepieciešams palēnināt vai pārtraukt. Var būt nepieciešama papildu ārstēšana, piemēram, ar antihistamīnu vai paracetamolu. Kad šie simptomi izzūd vai uzlabojas, infūziju var atsākt. Šīs reakcijas retāk rodas pēc otrās infūzijas. Ārsts var izlemt pārtraukt ārstēšanu ar MabThera, ja šīs reakcijas ir smagas.
Infekcijas
Nekavējoties pastāstiet ārstam, ja Jums ir kādas infekcijas pazīmes, tostarp:
- drudzis, klepus, iekaisis kakls, dedzināšana urinējot, vājums vai vispārēja slikta pašsajūta;
- atmiņas zudums, apgrūtināta domāšana, grūtības staigāt vai redzes zudums - to cēlonis var būt ļoti reta "nopietna infekcija, kas ir bijusi letāla (progresējoša multifokāla leikoencefalopātija vai PML). Ārstēšanas laikā ar MabThera infekcijas var attīstīties vieglāk.
- Tie bieži ir saaukstēšanās gadījumi, taču ir bijuši pneimonijas vai urīnceļu infekcijas gadījumi. Šie nosacījumi ir uzskaitīti zemāk esošajā sarakstā “Citas nevēlamās blakusparādības”.
Ja tiekat ārstēts no reimatoīdā artrīta, šo informāciju atradīsit arī pacienta brīdinājuma kartītē, ko jums sniegs ārsts. Ir svarīgi nēsāt līdzi šo brīdinājuma kartīti un parādīt to ģimenes loceklim vai jebkuram citam. citādi parūpējies par viņu.
Ādas reakcijas
Ļoti reti var rasties smagas ādas reakcijas ar pūslīšiem, kas var būt dzīvībai bīstami. Uz ādas vai gļotādām, piemēram, mutes, dzimumorgānu vai plakstiņu zonā, var parādīties apsārtums, kas bieži vien ir saistīts ar pūslīšiem, un var būt drudzis. Nekavējoties pastāstiet ārstam, ja Jums rodas kāds no šiem simptomiem.
Citas blakusparādības
a) ja Jums tiek ārstēta ne-Hodžkina limfoma vai hroniska limfoleikoze
Ļoti bieži sastopamas blakusparādības (var skart vairāk nekā 1 no 10 cilvēkiem):
- baktēriju vai vīrusu infekcijas, bronhīts
- zems balto asins šūnu skaits ar drudzi vai bez tās, vai trombocīti (asins šūnas)
- slikta dūša
- galvas ādas baldness zonas, drebuļi, galvassāpes
- imūnsistēmas pavājināšanās - dažu antivielu, ko sauc par “imūnglobulīniem” (IgG), samazināšanās asinīs, kas palīdz organismam pasargāt sevi no infekcijām.
Biežas blakusparādības (var skart līdz 1 no 10 cilvēkiem):
- asins infekcijas (sepse), pneimonija, jostas roze, saaukstēšanās, bronhu infekcija, sēnīšu infekcijas, nezināmas izcelsmes infekcijas, sinusīts, B hepatīts
- zems sarkano asins šūnu skaits (anēmija), zems visu asins šūnu skaits
- alerģiskas reakcijas (paaugstināta jutība)
- augsts cukura līmenis asinīs, svara zudums, sejas un ķermeņa pietūkums, augsts "enzīma" LDH "līmenis asinīs, zems kalcija līmenis asinīs
- neparastas ādas sajūtas - piemēram, nejutīgums, tirpšana, tirpšana, dedzināšana, izstieptas ādas sajūta, samazināta pieskāriena sajūta
- nemiera sajūta, grūtības aizmigt
- izteikts sejas un citu ādas zonu apsārtums asinsvadu paplašināšanās rezultātā
- reibonis vai trauksme
- pastiprināta asarošana, asaru kanālu problēmas, acu iekaisums (konjunktivīts)
- nepārtraukta zvana ausīs, sāpes ausī
- sirds problēmas - piemēram, sirdslēkme, neregulāra vai ātra sirdsdarbība
- augsts vai zems asinsspiediens (asinsspiediena pazemināšanās, īpaši stāvot)
- muskuļu kontrakcija elpceļos, kas izraisa sēkšanu (bronhu spazmas), iekaisums, kairinājums plaušās, kaklā un deguna blakusdobumos, elpas trūkums, iesnas
- vemšana, caureja, sāpes vēderā, rīkles un mutes kairinājums vai čūlas, rīšanas problēmas, aizcietējums, gremošanas traucējumi
- ēšanas traucējumi: nepietiekama uztura uzņemšana, kā rezultātā samazinās svars
- nātrene, pastiprināta svīšana, nakts svīšana
- muskuļu problēmas - piemēram, muskuļu stīvums, locītavu vai muskuļu sāpes, muguras un kakla sāpes
- vispārējs savārgums, nemiers vai nogurums, trīce, gripas pazīmes
- vairāku orgānu mazspēja.
Retākas blakusparādības (var skart līdz 1 no 100 cilvēkiem):
- asinsreces problēmas, samazināta sarkano asins šūnu veidošanās un pastiprināta sarkano asins šūnu iznīcināšana (hemolītiskā un aplastiskā anēmija), limfmezglu pietūkums vai palielināšanās
- zems garastāvoklis un intereses vai prieka zudums par darbību, nervozitāte
- problēmas, kas saistītas ar garšu - piemēram, garšas sajūtas izmaiņas
- sirds problēmas - piemēram, lēna sirdsdarbība vai sāpes krūtīs (stenokardija)
- astma, nepietiekams skābekļa daudzums, kas sasniedz ķermeņa orgānus
- vēdera uzpūšanās.
Ļoti retas blakusparādības (var skart līdz 1 no 10 000 cilvēkiem):
- dažu veidu antivielu (imūnglobulīnu - IgM) īstermiņa palielināšanās asinīs, ķīmiskas izmaiņas asinīs mirstošu vēža šūnu sadalīšanās dēļ
- roku un kāju nervu bojājumi, sejas paralīze
- sirdskaite
- asinsvadu iekaisums, ieskaitot tos, kas izraisa ādas simptomus
- elpošanas mazspēja
- zarnu sienas bojājumi (perforācija)
- smagas ādas problēmas ar pūslīšu veidošanos, potenciāli letālas. Uz ādas vai gļotādām, piemēram, mutes, dzimumorgānu vai plakstiņu iekšienē, var parādīties apsārtums, kas bieži vien ir saistīts ar pūslīšiem, un var būt drudzis.
- nieru mazspēja
- smags redzes zudums.
Nav zināms (šo blakusparādību rašanās biežums nav zināms):
- balto asins šūnu samazināšanās nav tūlītēja
- trombocītu skaita samazināšanās drīz pēc infūzijas - atgriezenisks stāvoklis, bet retos gadījumos dzīvībai bīstams
- dzirdes zudums, citu sajūtu zudums.
b) ja Jums tiek ārstēts reimatoīdais artrīts
Ļoti bieži sastopamas blakusparādības (var skart vairāk nekā 1 no 10 cilvēkiem):
- infekcijas, piemēram, pneimonija (bakteriāla)
- sāpes urinējot (urīnceļu infekcija)
- alerģiskas reakcijas, kas var rasties infūzijas laikā, bet var rasties līdz 24 stundām pēc infūzijas
- asinsspiediena izmaiņas, slikta dūša, izsitumi, drudzis, niezoša sajūta, iesnas vai aizlikts deguns, šķavas, trīce, ātra sirdsdarbība un nogurums
- galvassāpes
- izmaiņas laboratorijas testos, ko pieprasa ārsts. Tie ietver noteiktu specifisku olbaltumvielu (imūnglobulīnu) daudzuma samazināšanos asinīs, kas palīdz aizsargāties pret infekciju.
Biežas blakusparādības (var skart līdz 1 no 10 cilvēkiem):
- infekcijas, piemēram, bronhu iekaisums (bronhīts)
- sāpju un pilnības sajūta aiz deguna, vaigiem un acīm (sinusīts), sāpes vēderā, vemšana un caureja, apgrūtināta elpošana
- pēdu sēnīšu infekcija (sportista pēdas)
- augsts holesterīna līmenis asinīs
- neparastas sajūtas uz ādas, piemēram, nejutīgums, tirpšana, tirpšana vai dedzināšana, išiass, migrēna, reibonis
- matu izkrišana
- trauksme, depresija
- gremošanas traucējumi, caureja, skābes reflukss, kairinājums un / vai čūlas kaklā un mutē
- sāpes vēderā, mugurā, muskuļos un / vai locītavās.
Retākas blakusparādības (var skart līdz 1 no 100 cilvēkiem):
- liekā šķidruma aizture sejā un ķermenī
- iekaisums, kairinājums un / vai sasprindzinājums plaušās, rīklē, klepus
- ādas reakcijas, tai skaitā nātrene, nieze, izsitumi
- alerģiskas reakcijas, tostarp sēkšana vai elpas trūkums, sejas un mēles pietūkums, sabrukums.
Ļoti retas blakusparādības (var skart līdz 1 no 10 000 cilvēkiem):
- simptomu komplekss, kas rodas dažu nedēļu laikā pēc MabThera infūzijas, ieskaitot alerģiskas reakcijas, piemēram, izsitumus, niezi, locītavu sāpes, limfmezglu pietūkumu un drudzi
- smagas ādas reakcijas ar pūslīšiem, kas var būt dzīvībai bīstamas. Uz ādas vai gļotādām, piemēram, mutes, dzimumorgānu vai plakstiņu zonā, var parādīties apsārtums, kas bieži vien ir saistīts ar pūslīšiem, un var būt drudzis.
Citas MabThera terapijas blakusparādības, par kurām ziņots reti, ir balto asins šūnu (neitrofilu) skaita samazināšanās, ko lieto infekciju apkarošanai. Dažas infekcijas var būt nopietnas (lūdzu, skatiet informāciju par infekcijām šajā sadaļā).
c) ja Jums ārstē granulomatozi ar poliangiītu vai mikroskopisku poliangiītu
Ļoti bieži sastopamas blakusparādības (var skart vairāk nekā 1 no 10 cilvēkiem):
- infekcijas, piemēram, plaušu infekcijas, urīnceļu infekcijas (sāpīga urinēšana), saaukstēšanās un herpes infekcijas
- alerģiskas reakcijas, kas var rasties infūzijas laikā, bet var rasties līdz 24 stundām pēc infūzijas
- caureja
- klepus vai elpas trūkums
- deguna asiņošana
- paaugstināts asinsspiediens
- sāpes locītavās vai mugurā
- muskuļu raustīšanās vai trīce
- reibonis
- trīce (trīce, bieži rokās)
- miega traucējumi (bezmiegs)
- roku un potīšu pietūkums.
Biežas blakusparādības (var skart līdz 1 no 10 cilvēkiem):
- gremošanas traucējumi
- aizcietējums
- izsitumi uz ādas, ieskaitot pūtītes vai plankumus
- ādas pietvīkums vai apsārtums
- iesnas
- muskuļu stīvums vai muskuļu sāpes
- sāpes muskuļos vai rokās vai kājās
- zems sarkano asins šūnu skaits (anēmija)
- zems trombocītu skaits asinīs palielinās kālija daudzums asinīs
- sirds ritma vai sirdsdarbības ātruma izmaiņas ātrāk nekā parasti.
Ļoti retas blakusparādības (var skart līdz 1 no 10 000 cilvēkiem):
- smagas ādas reakcijas ar pūslīšiem, kas var būt dzīvībai bīstamas. Uz ādas vai gļotādām, piemēram, mutes, dzimumorgānu vai plakstiņu iekšpusē, var parādīties apsārtums, kas bieži vien ir saistīts ar pūslīšiem, un var būt drudzis.
- atkārtota iepriekšēja B hepatīta infekcija.
MabThera var izraisīt izmaiņas arī ārsta noteiktajos laboratoriskajos testos.
Ja Jūs lietojat MabThera kombinācijā ar citām zālēm, dažas blakusparādības var rasties citu zāļu dēļ.
Ziņošana par blakusparādībām
Ja Jums rodas jebkādas blakusparādības, konsultējieties ar ārstu, farmaceitu vai medmāsu. Tas attiecas arī uz iespējamām blakusparādībām, kas nav minētas šajā lietošanas instrukcijā. Jūs varat ziņot par blakusparādībām arī tieši, izmantojot V pielikumā minēto valsts ziņošanas sistēmu. sniedziet vairāk informācijas par šo zāļu drošumu.
Derīguma termiņš un saglabāšana
Uzglabāt šīs zāles bērniem neredzamā un nepieejamā vietā.
Nelietot šīs zāles pēc derīguma termiņa beigām, kas norādīts uz kastītes pēc „Derīgs līdz”. Derīguma termiņš attiecas uz mēneša pēdējo dienu.
Uzglabāt ledusskapī (2 ° C - 8 ° C). Uzglabāt trauku ārējā iepakojumā, lai pasargātu no gaismas.
Neizmetiet zāles kanalizācijā vai sadzīves atkritumos. Jautājiet farmaceitam, kā izmest zāles, kuras vairs nelietojat. Tas palīdzēs aizsargāt vidi.
Ko MabThera satur
- MabThera aktīvā viela ir rituksimabs. Flakons satur 100 mg rituksimaba (10 mg / ml).
- Citas sastāvdaļas ir nātrija citrāts, polisorbāts 80, nātrija hlorīds, nātrija hidroksīds, sālsskābe un ūdens injekcijām.
MabThera ārējais izskats un iepakojums
MabThera ir dzidrs un bezkrāsains šķīdums infūziju šķīduma koncentrāta veidā. 10 ml flakoni ir pieejami iepakojumā pa 2 flakoniem.
Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī. Pašlaik pieejamā informācija var nebūt atjaunināta.
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija.
01.0 ZĀĻU NOSAUKUMS
MABTHERA 100 MG KONCENTRĀTS infūziju šķīduma pagatavošanai
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS
Katrs ml satur 10 mg rituksimaba.
Katrs flakons satur 100 mg rituksimaba.
Rituksimabs ir ģenētiski modificēta himēriska peles / cilvēka monoklonāla antiviela, kas sastāv no glikozilēta imūnglobulīna ar cilvēka IgG1 konstantiem reģioniem un peles vieglās ķēdes un smagās ķēdes mainīgā reģiona sekvencēm.
Antivielu ražo, izmantojot zīdītāju šūnu suspensijas kultūru (ķīniešu kāmja olnīcas), un attīra ar afīnu hromatogrāfiju un jonu apmaiņu, ieskaitot īpašas vīrusu inaktivācijas un noņemšanas procedūras.
Pilnu palīgvielu sarakstu skatīt apakšpunktā 6.1.
03.0 ZĀĻU FORMA
Koncentrāts infūziju šķīduma pagatavošanai.
Dzidrs un bezkrāsains šķidrums.
04.0 KLĪNISKĀ INFORMĀCIJA
04.1 Terapeitiskās indikācijas
MabThera ir indicēts pieaugušajiem šādām indikācijām:
Ne-Hodžkina limfoma (NHL)
MabThera ir indicēts iepriekš neārstētu pacientu ar III-IV stadijas folikulāro limfomu ārstēšanai kombinācijā ar ķīmijterapiju.
MabThera uzturošā terapija ir indicēta folikulu limfomas pacientu ārstēšanai, kuri reaģē uz indukcijas terapiju.
MabThera monoterapija ir indicēta pacientu ar III-IV stadijas folikulāro limfomu ārstēšanai, kuriem ir ķīmijizturība vai kuriem pēc ķīmijterapijas ir otrais vai nākamais recidīvs.
MabThera ir indicēts pacientu ar CD20 pozitīvu difūzu lielu B šūnu ne-Hodžkina limfomu ārstēšanai kombinācijā ar CHOP ķīmijterapiju (ciklofosfamīds, doksorubicīns, vinkristīns, prednizolons).
Hroniska limfoleikoze (HLL)
MabThera kombinācijā ar ķīmijterapiju ir indicēts pacientu ārstēšanai ar iepriekš neārstētu un recidivējošu / refraktāru hronisku limfoleikozi. Ir pieejami tikai ierobežoti dati par efektivitāti un drošību pacientiem, kuri iepriekš ārstēti ar monoklonālām antivielām, ieskaitot MabThera, vai pacientiem, kuri nav izturīgi pret iepriekšējo ārstēšanu ar MabThera plus ķīmijterapiju.
Papildu informāciju skatīt 5.1. Sadaļā.
Reimatoīdais artrīts
MabThera kombinācijā ar metotreksātu ir indicēts smaga aktīva reimatoīdā artrīta ārstēšanai pieaugušiem pacientiem, kuriem ir bijusi “nepietiekama reakcija vai nepanesība pret citiem slimību modificējošiem pretreimatisma līdzekļiem (DMARD), ieskaitot vienu vai vairākus audzēja nekrozes faktora inhibitorus”. (TNF).
Ir pierādīts, ka MabThera samazina rentgenstaru novērtēto locītavu bojājumu progresēšanas ātrumu un uzlabo fizisko funkciju, ja to lieto kombinācijā ar metotreksātu.
Granulomatoze ar poliangiītu un mikroskopisku poliangiītu
MabThera kombinācijā ar glikokortikoīdiem ir indicēts remisijas ierosināšanai pieaugušiem pacientiem ar granulomatozi ar (Vegenera) poliangiītu (GPA) un smagu aktīvu mikroskopisku poliangiītu (MPA).
04.2 Devas un lietošanas veids
MabThera jāievada pieredzējuša veselības aprūpes speciālista stingrā uzraudzībā un vidē, kur nekavējoties ir pieejams reanimācijas aprīkojums (skatīt apakšpunktu 4.4).
Pirms katras MabThera lietošanas vienmēr jāveic premedikācija ar pretdrudža zālēm un antihistamīna līdzekļiem, piemēram, paracetamolu un difenhidramīnu.
Pacientiem ar ne Hodžkina limfomu un hronisku limfoleikozi (HLL) jāapsver premedikācija ar glikokortikoīdiem, ja MabThera netiek lietots kombinācijā ar glikokortikoīdus saturošu ķīmijterapiju.
Pacientiem ar reimatoīdo artrītu premedikācija ar 100 mg metilprednizolona intravenozu ievadīšanu jāpabeidz 30 minūtes pirms MabThera infūzijas, lai samazinātu ar infūziju saistītu reakciju (IRR) biežumu un smagumu.
Pacientiem, kuri cieš no granulomatozes ar poliangiītu (Vegenera) vai mikroskopisku poliangiītu, 1 līdz 3 dienas pirms pirmās MabThera infūzijas ieteicams ievadīt intravenozu metilprednizolona devu 1000 mg dienā (pēdējo metilprednizolona devu var ievadīt tajā pašā dienā kā pirmā MabThera infūzija) Pēc tam jālieto perorāls prednizons devā 1 mg / kg dienā (nedrīkst pārsniegt 80 mg dienā un pēc iespējas ātrāk samazināt devu atkarībā no klīniskā stāvokļa). un pēc ārstēšanas ar MabThera.
Devas
& EGRAVE; Ir svarīgi pārbaudīt zāļu marķējumu, lai pārliecinātos, ka pacientam tiek ievadīts atbilstošais preparāts (intravenozi vai subkutāni), kā noteikts.
Ne-Hodžkina limfoma
Folikulāra ne-Hodžkina limfoma
Asociācijas terapija
Ieteicamā MabThera deva kombinācijā ar ķīmijterapiju indukcijas ārstēšanai iepriekš neārstētiem vai recidivējošiem / refraktāriem pacientiem ar folikulāru limfomu ir 375 mg / m2 ķermeņa virsmas laukuma vienā ciklā līdz 8 cikliem.
MabThera jāievada katra ķīmijterapijas cikla 1. dienā pēc i.v. ķīmijterapijas glikokortikoīdu sastāvdaļa, ja tāda ir.
Uzturošā terapija
• Iepriekš neārstēta folikulāra limfoma
Ieteicamā MabThera deva, ko lieto kā uzturošo terapiju iepriekš neārstētiem folikulāras limfomas pacientiem, kuri ir reaģējuši uz indukcijas terapiju, ir: 375 mg / m2 ķermeņa virsmas laukuma reizi divos mēnešos (sākot no 2 mēnešiem pēc pēdējās terapijas devas). progresu vai ne ilgāk kā divus gadus.
• recidivējoša / ugunsizturīga folikulāra limfoma
Ieteicamā MabThera deva, ko lieto kā uzturošo terapiju pacientiem ar recidivējošu / rezistentu folikulāru limfomu un kuri ir reaģējuši uz indukcijas terapiju, ir 375 mg / m2 ķermeņa virsmas laukuma reizi 3 mēnešos (sākot no 3 mēnešiem pēc pēdējās terapijas devas). slimības progresēšanu vai ne ilgāk kā divus gadus.
Monoterapija
• recidivējoša / ugunsizturīga folikulāra limfoma
Ieteicamā MabThera monoterapijas deva, ko izmanto kā indukcijas terapiju pieaugušiem pacientiem ar III-IV stadijas folikulāro limfomu, kuri ir ķīmijizturīgi vai kuriem pēc ķīmijterapijas ir otrais vai nākamais recidīvs, ir 375 mg / m2 ķermeņa virsmas laukuma, ievadot intravenozas infūzijas veidā. reizi nedēļā četras nedēļas.
Atkārtotai terapijai ar MabThera monoterapiju pacientiem, kuri ir reaģējuši uz iepriekšēju ārstēšanu ar MabThera monoterapiju recidivējošas / ugunsizturīgas folikulārās limfomas ārstēšanai, ieteicamā deva ir 375 mg / m2 ķermeņa virsmas laukuma, ievadot intravenozas infūzijas veidā reizi nedēļā četras nedēļas. (Skatīt apakšpunktu 5.1) ).
Izkliedēta liela B šūnu ne-Hodžkina limfoma
MabThera jālieto kombinācijā ar CHOP ķīmijterapiju. Ieteicamā deva ir 375 mg / m2 ķermeņa virsmas laukuma, ievadot katra ķīmijterapijas cikla 1. dienā 8 ciklus pēc CHOP glikokortikoīdu sastāvdaļas intravenozas infūzijas. MabThera drošība un efektivitāte kombinācijā ar citām ķīmijterapijām difūzās lielo B šūnu ne-Hodžkina limfomas gadījumā vēl nav noskaidrota.
Devas pielāgošana ārstēšanas laikā
Nav ieteicams samazināt MabThera devu. Ja MabThera lieto kombinācijā ar ķīmijterapiju, ķīmijterapijas zālēm ir jāsamazina standarta deva.
Hroniska limfoleikoze
Lai samazinātu audzēja sabrukšanas sindroma risku, HLL pacientiem ieteicams veikt profilaksi ar atbilstošu hidratāciju un urikostatu ievadīšanu, sākot 48 stundas pirms terapijas uzsākšanas. Pacientiem ar HLL, kuru limfocītu skaits ir> 25 x 109 / l, ieteicams lietot prednizonu / 100 mg prednizolona intravenozi tieši pirms MabThera infūzijas, lai samazinātu akūtu infūzijas reakciju un / vai citokīnu izdalīšanās sindroma ātrumu un smagumu.
Ieteicamā MabThera deva kombinācijā ar ķīmijterapiju iepriekš neārstētiem un recidivējošiem / refraktāriem pacientiem ir 375 mg / m2 ķermeņa virsmas laukuma, kas ievadīts pirmā ārstēšanas cikla 0. dienā, kam seko 500 mg / m2 ķermeņa virsmas laukuma katra nākamā cikls kopumā 6 cikliem. Pēc MabThera infūzijas jāveic ķīmijterapija.
Reimatoīdais artrīts
Pacientiem, kuri saņem MabThera, katrai infūzijai jāsniedz pacienta brīdinājuma karte.
MabThera kurss sastāv no divām intravenozām infūzijām pa 1000 mg katrā. Ieteicamā MabThera deva ir 1000 mg intravenozas infūzijas veidā, kam seko otra 1000 mg intravenoza infūzija divas nedēļas vēlāk.
Nepieciešamība pēc turpmākas ārstēšanas jāizvērtē 24 nedēļas pēc iepriekšējā cikla. Atkārtota ārstēšana jāveic tajā laikā, ja saglabājas atlikušā slimības aktivitāte, pretējā gadījumā atkārtota ārstēšana jāatliek, līdz slimības atlikušā aktivitāte atkal parādās.
Pieejamie dati liecina, ka klīniskā atbildes reakcija parasti tiek sasniegta 16 līdz 24 nedēļu laikā pēc sākotnējā ārstēšanas kursa. Pacientiem, kuri šajā laikā neredz terapeitisko ieguvumu, rūpīgi jāapsver, vai turpināt terapiju.
Granulomatoze ar poliangiītu un mikroskopisku poliangiītu
Pacientiem, kuri tiek ārstēti ar MabThera, katrai infūzijai jāsniedz pacienta brīdinājuma kartīte.
Ieteicamā MabThera deva granulomatozes ar poliangiītu un mikroskopisku poliangiītu remisijas indukcijas terapijai ir 375 mg / m2 ķermeņa virsmas laukuma, ievadot intravenozas infūzijas veidā reizi nedēļā 4 nedēļas (kopā 4 infūzijas).
Pacientiem ar granulomatozi ar poliangiītu un mikroskopisku poliangiītu ārstēšanas laikā ar MabThera un pēc tās ieteicama pneimonijas profilakse. Pneumocystis jiroveci, (PCP), ja nepieciešams.
Īpašas populācijas
Pediatriskā populācija
MabThera drošība un efektivitāte, lietojot bērniem un pusaudžiem līdz 18 gadu vecumam, vēl nav pierādīta.
Gados vecāki pacienti
Gados vecākiem pacientiem (> 65 gadus veci) deva nav jāpielāgo.
Lietošanas veids
Sagatavotais MabThera šķīdums jāievada intravenozas infūzijas veidā, izmantojot īpašu līniju. To nedrīkst ievadīt kā intravenozu spiedienu vai bolus. Pacienti rūpīgi jānovēro attiecībā uz citokīnu izdalīšanās sindroma parādīšanos (skatīt apakšpunktu 4.4). Pacientiem, kuriem attīstās smagas reakcijas, īpaši smaga aizdusa, bronhu spazmas vai hipoksija, infūzija nekavējoties jāpārtrauc. Pacientiem ar ne-Hodžkina limfomu pēc tam jānovērtē audzēja sabrukšanas sindroma klātbūtne, veicot atbilstošus laboratorijas testus un plaušu infiltrācijas klātbūtni krūšu kurvja rentgenogrammā. Visiem pacientiem infūziju nedrīkst atsākt, kamēr nav pilnībā izzuduši visi simptomi un laboratorisko rādītāju normalizēšana un krūšu kurvja rentgenogrāfija. Tikai tad infūziju var atsākt ar sākotnējo ātrumu, kas samazināts uz pusi no iepriekš izmantotās.Ja tās pašas nopietnas blakusparādības atkārtojas, lēmums par ārstēšanas pārtraukšanu ir rūpīgi jāizvērtē katrā gadījumā atsevišķi.
Vieglas vai vidēji smagas ar infūziju saistītas reakcijas (IRR) (skatīt 4.8. Apakšpunktu) parasti reaģē uz infūzijas ātruma samazināšanos. Simptomiem uzlabojoties, infūzijas ātrumu var palielināt.
Pirmā infūzija
Ieteicamais sākotnējais infūzijas ātrums ir 50 mg / h; pēc pirmajām 30 minūtēm to var palielināt ar soli 50 mg / h ik pēc 30 minūtēm, maksimāli līdz 400 mg / h.
Turpmākās infūzijas
Visām indikācijām
Turpmākās MabThera devas var ievadīt ar sākotnējo infūzijas ātrumu 100 mg / h un palielināt ar 100 mg / h ar 30 minūšu intervālu, maksimāli līdz 400 mg / h.
Tikai reimatoīdā artrīta gadījumā
Alternatīva shēma ātrākai nākamo infūziju ievadīšanai
Ja pirmās vai nākamās infūzijas, ievadot MabThera 1000 mg devu saskaņā ar standarta infūzijas shēmu, pacientiem nav bijušas smagas ar infūziju saistītas reakcijas, otro un nākamās infūzijas var ievadīt ātrāk, ar tādu pašu ātrumu iepriekšējo infūziju koncentrācija (4 mg / ml 250 ml tilpumam).
Sāciet infūziju ar ātrumu 250 mg / h pirmajās 30 minūtēs un pēc tam 600 mg / h nākamajās 90 minūtēs.Ja ātrāka infūzija ir labi panesama, to pašu infūzijas grafiku var izmantot arī turpmāko infūziju ievadīšanai.
Ātrāku infūziju nedrīkst ievadīt pacientiem ar klīniski nozīmīgu sirds un asinsvadu slimību, tostarp aritmiju, vai kuriem agrāk ir bijušas smagas reakcijas uz rituksimaba infūziju vai jebkādu iepriekšēju bioloģisku terapiju.
04.3 Kontrindikācijas
Kontrindikācijas lietošanai ne-Hodžkina limfomas un hroniskas limfoleikozes gadījumā
Paaugstināta jutība pret aktīvo vielu, peļu proteīniem vai kādu citu 6.1. Apakšpunktā uzskaitīto palīgvielu.
Aktīvas, smagas infekcijas (skatīt apakšpunktu 4.4).
Pacienti ar smagu imūndeficītu.
Kontrindikācijas lietošanai reimatoīdā artrīta, granulomatozes ar poliangiītu un mikroskopiskā poliangiīta gadījumā
Paaugstināta jutība pret aktīvo vielu, peļu proteīniem vai kādu citu 6.1. Apakšpunktā uzskaitīto palīgvielu.
Aktīvas, smagas infekcijas (skatīt apakšpunktu 4.4).
Pacienti ar smagu imūndeficītu.
Smaga sirds mazspēja (Ņujorkas Sirds asociācijas IV klase) vai smaga, nekontrolēta sirds slimība (citus sirdsdarbības traucējumus skatīt apakšpunktā 4.4).
04.4 Īpaši brīdinājumi un piesardzība lietošanā
Lai uzlabotu bioloģisko zāļu izsekojamību, zāļu nosaukums MabThera skaidri jāreģistrē pacienta reģistrā.
Progresējoša multifokāla leikoencefalopātija
Visiem pacientiem, kas ārstēti ar MabThera pret reimatoīdo artrītu, granulomatozi ar poliangiītu un mikroskopisku poliangiītu, katrai infūzijai ir jāsniedz pacienta brīdinājuma kartīte. Brīdinājuma kartītē ir svarīga informācija par drošību pacientiem attiecībā uz potenciāli lielu infekciju risku, tostarp progresējošu multifokālu leikoencefalopātiju (PML).
Pēc MabThera lietošanas ziņots par ļoti retiem nāvējošiem PML gadījumiem. Pacienti regulāri jānovēro, lai konstatētu jaunus vai pasliktinošus neiroloģiskus simptomus vai pazīmes, kas liecina par PML. Ja ir aizdomas par PML, turpmāka lietošana jāpārtrauc līdz PML diagnoze ir izslēgta. Ārstam jānovērtē pacients, lai noteiktu, vai simptomi liecina par neiroloģisku disfunkciju, un, ja jā, vai šie simptomi, iespējams, liecina par PML. Ja ir klīniskas indikācijas, jāmeklē neirologa konsultācija.
Ja rodas šaubas, jāapsver turpmāka novērtēšana, tostarp tādi testi kā MRI, vēlams ar kontrastu, cerebrospinālā šķidruma (CSF) pārbaude, lai novērtētu JC vīrusa DNS, un atkārtoti neiroloģiski novērtējumi.
Ārstiem jābūt īpaši uzmanīgiem par simptomiem, kas liecina par PML, kurus pacients var nepamanīt (piemēram, kognitīvus, neiroloģiskus vai psihiskus simptomus). Pacientam arī jāiesaka informēt savu partneri vai aprūpētāju par ārstēšanu, jo viņš var pamanīt simptomus, par kuriem pacients nezina.
Ja pacientam attīstās PML, MabThera lietošana ir nepārtraukti jāpārtrauc.
Pēc imūnsistēmas atjaunošanas pacientiem ar imūndeficītu ar PML tika novērota stabilizācija vai uzlabošanās. Nav zināms, vai agrīna PML noteikšana un MabThera terapijas pārtraukšana novedīs pie līdzīgas stabilizācijas vai uzlabošanās.
Ne-Hodžkina limfoma un hroniska limfoleikoze
Ar infūziju saistītas reakcijas
MabThera ir saistīta ar ar infūziju saistītām reakcijām, kas potenciāli ir saistītas ar citokīnu un / vai citu ķīmisku mediatoru izdalīšanos.Citokīnu izdalīšanās sindroms var klīniski neatšķirties no akūtām paaugstinātas jutības reakcijām.
Šis reakciju kopums, kas ietver citokīnu izdalīšanās sindromu, audzēja sabrukšanas sindromu un anafilaktiskas un paaugstinātas jutības reakcijas, ir aprakstīts zemāk. Šīs reakcijas nav īpaši saistītas ar MabThera ievadīšanas veidu, un tās var novērot, lietojot abas zāļu formas.
Lietojot MabThera intravenozo zāļu formu pēcreģistrācijas periodā, ziņots par nopietnām un letālām ar infūziju saistītām reakcijām, kas sākas 30 minūšu līdz 2 stundu laikā pēc pirmās MabThera IV infūzijas uzsākšanas. Šīs reakcijas raksturoja plaušu notikumi un dažos gadījumos gadījumos bija ātra audzēja sabrukšana un audzēja līzes sindroma simptomi, kā arī drudzis, drebuļi, drebuļi, hipotensija, nātrene, angioneirotiskā tūska un citi simptomi (skatīt 4.8. apakšpunktu).
Smagu citokīnu izdalīšanās sindromu raksturo smaga aizdusa, ko bieži pavada bronhu spazmas un hipoksija, kā arī drudzis, drebuļi, drebuļi, nātrene un angioneirotiskā tūska. Šis sindroms var būt saistīts ar dažām audzēja sabrukšanas sindroma pazīmēm, piemēram, hiperurikēmiju, hiperkaliēmiju, hipokalciēmiju, hiperfosfatēmiju, akūtu nieru mazspēju, paaugstinātu laktāta dehidrogenāzes (LDH) koncentrāciju un var būt saistīts ar akūtu elpošanas mazspēju un nāvi. Akūtu elpošanas mazspēju var pavadīt tādi notikumi kā plaušu intersticiāla infiltrācija vai plaušu tūska, kas redzama krūškurvja rentgenogrammā.Sindroms bieži rodas vienas līdz divu stundu laikā pēc pirmās infūzijas uzsākšanas. Pacientiem, kuriem anamnēzē ir plaušu nepietiekamība vai plaušu audzēja infiltrācija, var būt paaugstināts sliktu iznākumu risks, un viņi jāārstē ar lielāku piesardzību. Pacientiem, kuriem attīstās smags citokīnu izdalīšanās sindroms, infūzija nekavējoties jāpārtrauc (skatīt 4.2. Apakšpunktu), un viņiem jāveic agresīva simptomātiska ārstēšana. Tā kā pēc sākotnējo klīnisko simptomu uzlabošanās var pasliktināties, šie pacienti rūpīgi jānovēro līdz audzēja sabrukšanas sindromam un plaušu infiltrācija ir atrisināta vai izslēgta.
Turpmāka pacientu ārstēšana pēc simptomu un pazīmju pilnīgas izzušanas reti izraisīja smaga citokīnu izdalīšanās sindroma atkārtošanos.
Pacienti ar lielu audzēja slodzi vai lielu skaitu (≥ 25 x 109 / L) cirkulējošu neoplastisko šūnu, piemēram, HLL slimnieki, kuriem var būt paaugstināts īpaši smaga citokīnu izdalīšanās sindroma risks, jāārstē ļoti piesardzīgi. Šie pacienti pirmās infūzijas laikā ir ļoti rūpīgi jānovēro. Šādiem pacientiem jāapsver iespēja izmantot samazinātu infūzijas ātrumu pirmajai infūzijai vai sadalīt devu divās dienās pirmajā ciklā un katrā nākamajā ciklā, ja limfocītu skaits joprojām ir> 25 x 109 / l.
Visu veidu ar infūziju saistītas blakusparādības (ieskaitot citokīnu izdalīšanās sindromu, kam 10% pacientu ir hipotensija un bronhu spazmas) novērotas 77% ar MabThera ārstēto pacientu (skatīt 4.8. Apakšpunktu). Šie simptomi parasti ir atgriezeniski. MabThera infūzijas laikā un, lietojot pretdrudža zāles, antihistamīna līdzekļus un dažreiz skābekli, intravenozas fizioloģiskās vai bronhodilatatora zāles, kā arī glikokortikoīdus, ja nepieciešams. Smagas reakcijas skatīt iepriekš aprakstītajā citokīnu izdalīšanās sindromā.
Pēc proteīnu intravenozas ievadīšanas pacientiem ziņots par anafilaktiskām un citām paaugstinātas jutības reakcijām. Atšķirībā no citokīnu izdalīšanās sindroma, paaugstinātas jutības reakcijas parasti rodas dažu minūšu laikā pēc infūzijas sākuma. Ja MabThera lietošanas laikā rodas alerģiska reakcija, zāles paaugstinātas jutības reakciju ārstēšanai, piem. tūlītējai lietošanai jābūt pieejamiem epinefrīnam (adrenalīnam), antihistamīna līdzekļiem un glikokortikoīdiem. Anafilakses klīniskās izpausmes var izskatīties līdzīgas citokīnu izdalīšanās sindroma klīniskajām izpausmēm (aprakstītas iepriekš). Par reakcijām, kas saistītas ar paaugstinātu jutību, ziņots retāk nekā par citokīnu izdalīšanos.
Papildu reakcijas, par kurām ziņots dažos gadījumos, bija miokarda infarkts, priekškambaru mirdzēšana, plaušu tūska un akūta atgriezeniska trombocitopēnija. Lietojot MabThera, var rasties hipotensija, tādēļ jāapsver antihipertensīvo zāļu lietošanas pārtraukšana 12 stundas pirms MabThera infūzijas.
Sirds darbības traucējumi
Ar MabThera ārstētiem pacientiem ir novēroti stenokardijas, sirds aritmijas gadījumi, piemēram, priekškambaru plandīšanās un fibrilācija, sirds mazspēja un / vai miokarda infarkts. Tādēļ pacienti, kuriem anamnēzē ir sirds slimība un / vai kardiotoksiska ķīmijterapija, rūpīgi jānovēro.
Hematoloģiskā toksicitāte
Lai gan MabThera pati par sevi nav mielosupresīva, īpaša piesardzība jāievēro, ārstējot pacientus ar autologiem kaulu smadzeņu trombocītu neitrofiliem un citām riska grupām ar, iespējams, kaulu smadzeņu darbības traucējumiem, neizraisot mielotoksicitāti.
MabThera terapijas laikā regulāri jāveic pilnīga asins analīze, ieskaitot neitrofilu un trombocītu skaitu.
Infekcijas
Terapijas laikā ar MabThera var rasties nopietnas infekcijas, tostarp nāve (skatīt apakšpunktu 4.8).
MabThera nedrīkst lietot pacienti ar smagām aktīvām infekcijām (piemēram, tuberkulozi, sepsi un oportūnistiskām infekcijām, skatīt apakšpunktu 4.3).
Ārstiem jābūt piesardzīgiem, apsverot MabThera lietošanu pacientiem, kuriem anamnēzē ir atkārtotas vai hroniskas infekcijas vai kuriem ir pamatslimības, kas var vēl vairāk predisponēt pacientus nopietnām infekcijām (skatīt 4.8. Apakšpunktu).
Ir ziņots par B hepatīta reaktivācijas gadījumiem pacientiem, kuri saņēma MabThera, tostarp ziņojumus par fulminantu hepatītu ar letālu iznākumu. Lielākā daļa šo pacientu saņēma arī citotoksisku ķīmijterapiju. Ierobežota informācija no pētījuma ar pacientiem ar recidivējošu / refraktāru HLL liecina, ka ārstēšana ar MabThera var arī pasliktināt primāro B hepatīta infekciju iznākumu. Pirms hepatīta terapijas uzsākšanas visiem pacientiem jāveic B hepatīta vīrusa (HBV) skrīnings. Vismaz jāiekļauj HBsAg un HBcAb dozēšana. Pēc tam šos testus var papildināt ar citiem atbilstošiem marķieriem saskaņā ar vietējām vadlīnijām. Pacientus ar aktīvu B hepatīta infekciju nedrīkst ārstēt ar MabThera. Jāizvērtē pacienti ar pozitīvu B hepatīta seroloģiju (gan HBsAg, gan HBcAb) hepatīta klīnicists pirms ārstēšanas uzsākšanas, un tas ir jāuzrauga un jākontrolē saskaņā ar vietējiem klīniskajiem standartiem, lai novērstu B hepatīta reaktivāciju.
Lietojot MabThera pēcreģistrācijas periodā NHL un HLL, ziņots par ļoti retiem progresējošas multifokālas leikoencefalopātijas (PML) gadījumiem (skatīt 4.8. Apakšpunktu). Lielākā daļa pacientu bija saņēmuši MabThera kombinācijā ar ķīmijterapiju vai kā daļu no asinsrades cilmes šūnu transplantācijas programmas.
Imunizācija
Imunizācijas drošība ar dzīvām vīrusu vakcīnām pēc MabThera terapijas nav pētīta NHL un HLL slimniekiem, un vakcinācija ar dzīvu vīrusu vakcīnām nav ieteicama. Pacienti, kuri tiek ārstēti ar MabThera, var saņemt pretvīrusu vakcināciju. Tomēr atbildes reakcija uz nedzīviem vīrusiem Vakcīnas var samazināt. Nejaušinātā pētījumā pacientiem ar recidivējošu zemas pakāpes NHL, kuri saņēma MabThera monoterapiju, salīdzinot ar neārstētiem veseliem brīvprātīgajiem, bija zemāks atbildes reakcijas līmenis uz vakcināciju ar stingumkrampju pastiprinātājiem (16% pret 81%) un Keyhole Limpet hemocianīna (KLH) neoantigēni (4% salīdzinājumā ar 76%, ja tiek novērtēts, vai antivielu titrs ir palielinājies vairāk nekā 2 reizes). Sagaidāms, ka HLL būs līdzīgi rezultāti, ņemot vērā abu slimību līdzības, tomēr klīniskie pētījumi to nav novērtējuši . pirmsterapijas antivielas pret antigēnu paneli (Streptococcus pneumoniae, A gripa, cūciņa, masaliņas, vējbakas) pēc ārstēšanas ar MabThera saglabājās vismaz 6 mēnešus.
Ādas reakcijas
Ir ziņots par nopietnām ādas reakcijām, piemēram, toksisku epidermas nekrolīzi (Laiela sindromu) un Stīvensa-Džonsona sindromu, dažām ar letālu iznākumu (skatīt 4.8. Apakšpunktu). Šādu notikumu gadījumā, ja ir aizdomas par saistību ar MabThera, ārstēšana uz visiem laikiem jāpārtrauc. Reimatoīdais artrīts, granulomatoze ar poliangiītu un mikroskopisks poliangiīts.
Populācijas ar reimatoīdo artrītu, kas iepriekš nav saņēmušas metotreksātu (MTX)
MabThera lietošana nav ieteicama pacientiem, kuri iepriekš nav saņēmuši MTX, jo nav noteikta labvēlīga ieguvuma un riska attiecība.
Ar infūziju saistītas reakcijas
MabThera ir saistīta ar ar infūziju saistītām reakcijām (IRR), kuras var būt saistītas ar citokīnu un / vai citu ķīmisku mediatoru izdalīšanos. Pirms katras MabThera infūzijas vienmēr jāievada premedikācija ar pretsāpju / pretdrudža līdzekļiem un antihistamīna līdzekļiem. ar reimatoīdo artrītu pirms katras MabThera infūzijas vienmēr jāievada premedikācija ar glikokortikoīdiem, lai samazinātu IRR biežumu un smagumu (skatīt 4.2. un 4.8. apakšpunktu).
Pēcreģistrācijas periodā pacientiem ar reimatoīdo artrītu ziņots par nopietniem IRR gadījumiem ar letālu iznākumu.
Reimatoīdā artrīta ārstēšanā lielākā daļa ar infūziju saistītu reakciju klīniskajos pētījumos bija vieglas vai vidēji smagas. Visbiežāk sastopamie simptomi bija alerģiskas reakcijas, piemēram, galvassāpes, nieze, rīkles kairinājums, apsārtums, izsitumi, nātrene, hipertensija un drudzis. Kopumā to pacientu īpatsvars, kuriem bija kāda infūzijas reakcija, pēc pirmās infūzijas bija lielāks nekā pēc otrās jebkurā ārstēšanas ciklā, IRR biežums samazinājās turpmākajos kursos (skatīt 4.8. Apakšpunktu). Ziņotās reakcijas parasti bija atgriezeniskas, samazinot infūzijas ātrumu vai pārtraucot MabThera ievadīšanu un, ja nepieciešams, lietojot pretdrudža līdzekļus, antihistamīna līdzekļus un dažkārt skābekli, intravenozu fizioloģisko šķīdumu vai bronhodilatatorus, kā arī glikokortikoīdus. Rūpīgi novērojiet pacientus. Atkarībā no IRR smaguma un nepieciešamās iejaukšanās, īslaicīgi vai neatgriezeniski jāpārtrauc MabThera lietošana. Vairumā gadījumu infūziju var atsākt, samazinot ātrumu līdz 50% (piemēram, no 100 mg / h līdz 50 mg / h), kad simptomi ir pilnībā izzuduši.
Zāles paaugstinātas jutības reakciju ārstēšanai, piem. epinefrīnam (adrenalīnam), antihistamīna līdzekļiem un glikokortikoīdiem jābūt pieejamiem tūlītējai lietošanai alerģisku reakciju gadījumā MabThera lietošanas laikā.
Nav datu par MabThera drošību pacientiem ar mērenu sirds mazspēju (NYHA III klase) vai smagu, nekontrolētu sirds slimību.Pacientiem, kuri tika ārstēti ar MabThera, tika novērots, ka jau esoši sirds išēmijas stāvokļi, piemēram, stenokardija, kļūst simptomātiski, kā arī priekškambaru mirdzēšana un plandīšanās. Tādēļ pacientiem ar sirds slimībām anamnēzē un tiem, kam iepriekšējas reakcijas uz sirds un plaušu blakusparādībām, pirms ārstēšanas ar MabThera jāapsver infūzijas reakciju izraisītu kardiovaskulāru komplikāciju risks, un lietošanas laikā pacienti rūpīgi jāuzrauga. MabThera infūzijas laikā var rasties hipotensija, tādēļ antihipertensīvo līdzekļu lietošanas pārtraukšana 12 stundas pirms MabThera infūzija.
IRR pacientiem ar granulomatozi ar poliangiītu un mikroskopisku poliangiītu bija līdzīgi tiem, kas novēroti klīniskajos pētījumos pacientiem ar reimatoīdo artrītu (skatīt 4.8. Apakšpunktu).
Sirds darbības traucējumi
Ar MabThera ārstētiem pacientiem ir novēroti stenokardijas, sirds aritmijas gadījumi, piemēram, priekškambaru plandīšanās un fibrilācija, sirds mazspēja un / vai miokarda infarkts. Tādēļ pacienti ar sirds slimībām anamnēzē ir rūpīgi jānovēro (skatīt iepriekš “Ar infūziju saistītas reakcijas”).
Infekcijas
Pamatojoties uz MabThera darbības mehānismu un zināšanām, ka B šūnām ir svarīga loma normālas imūnās atbildes uzturēšanā, pacientiem pēc MabThera terapijas ir paaugstināts infekciju risks (skatīt 5.1. Apakšpunktu). MabThera terapija (skatīt 4.8. Apakšpunktu) MabThera nedrīkst ievadīt pacientiem ar smagu aktīvu infekciju (piemēram, tuberkulozi, sepsi un oportūnistiskām infekcijām, skatīt 4.3. Apakšpunktu) vai pacientiem ar smagu imūndeficītu.
(piemēram, ja CD4 vai CD8 vērtības ir ļoti zemas). Ārstiem jāievēro piesardzība, apsverot MabThera lietošanu pacientiem, kuriem anamnēzē ir atkārtotas vai hroniskas infekcijas vai kuriem ir pamatslimības, kas var vēl vairāk predisponēt pacientus nopietnām infekcijām, piemēram, hipogammaglobulinēmiju (skatīt 4.8. Apakšpunktu). Pirms ārstēšanas ar MabThera tiek noteikti imūnglobulīni.
Pacienti, kuriem pēc ārstēšanas ar MabThera rodas infekcijas pazīmes un simptomi, nekavējoties jānovērtē un atbilstoši jāārstē. Pirms turpmāka ārstēšanas kursa ar MabThera uzsākšanas pacienti atkārtoti jānovērtē attiecībā uz iespējamo infekciju risku.
Pēc MabThera lietošanas reimatoīdā artrīta un autoimūno slimību, tai skaitā sistēmiskās sarkanās vilkēdes (SLE) un vaskulīta, ārstēšanā ir ziņots par ļoti retiem letālas progresējošas multifokālas leikoencefalopātijas (PML) gadījumiem.
B hepatīta infekcija
Pacientiem ar reimatoīdo artrītu, granulomatozi ar poliangiītu un mikroskopisku poliangiītu, kuri saņēmuši MabThera, ziņots par B hepatīta reaktivācijas gadījumiem, tostarp ar letālu iznākumu.
Pirms BabThera terapijas uzsākšanas visiem pacientiem jāveic B hepatīta vīrusa (HBV) skrīnings, un tajā jāiekļauj vismaz HBsAg un HBcAb testi. Pēc tam šos testus var papildināt ar citiem atbilstošiem marķieriem. Saskaņā ar vietējām vadlīnijām. B infekcija nav jāārstē ar MabThera. Pacienti ar pozitīvu B hepatīta seroloģiju (gan HBsAg, gan HBcAb) jānovērtē hepatologam un jānovēro un jānovēro saskaņā ar vietējiem klīniskajiem standartiem, lai novērstu B hepatīta reaktivāciju.
Neitropēnija vēlu
Mēriet neitrofilus pirms katra MabThera kursa un ar regulāriem starplaikiem līdz 6 mēnešiem pēc ārstēšanas pārtraukšanas un infekcijas pazīmju vai simptomu gadījumā (skatīt 4.8. Apakšpunktu).
Ādas reakcijas
Ir ziņots par nopietnām ādas reakcijām, piemēram, toksisku epidermas nekrolīzi (Laiela sindromu) un Stīvensa-Džonsona sindromu, dažām ar letālu iznākumu (skatīt 4.8. Apakšpunktu). Šādu notikumu gadījumā, ja ir aizdomas par saistību ar MabThera, ārstēšana uz visiem laikiem jāpārtrauc.
Imunizācija
Pirms MabThera terapijas ārstiem jāpārskata pacienta vakcinācijas statuss un jāievēro pašreizējās imunizācijas vadlīnijas.Vakcinācija jāpabeidz vismaz 4 nedēļas pirms pirmās MabThera ievadīšanas.
Imunizācijas drošība ar dzīvām vīrusu vakcīnām pēc MabThera terapijas nav pētīta, tāpēc MabThera terapijas laikā vai perifēro B šūnu samazināšanās periodā nav ieteicams vakcinēties ar dzīvu vīrusu vakcīnām.
Pacienti, kuri tiek ārstēti ar MabThera, var vakcinēties pret dzīviem vīrusiem. Tomēr atbildes reakcijas uz nedzīvām vīrusu vakcīnām var samazināt. Nejaušinātā pētījumā pacientiem ar reimatoīdo artrītu, kuri tika ārstēti ar MabThera un metotreksātu, atbildes reakcija bija līdzīga tiem pacientiem, kuri saņēma tikai metotreksātu pret stingumkrampju pastiprinātāja antigēniem (39% pret 42%), samazināja polisaharīdu vakcīnas līmeni. Pneimokoku (43% pret 82% līdz vismaz 2 antipneimokoku antivielu serotipiem) un KLH neoantigēniem (47% pret 93%), ja tos lieto 6 mēnešus pēc MabThera lietošanas. Ja MabThera terapijas laikā ir nepieciešama vakcinācija pret dzīviem vīrusiem, tās jāpabeidz vismaz 4 nedēļas pirms nākamā MabThera kursa sākuma.
"Vispasaules pieredzē par atkārtotu MabThera ārstēšanu viena gada laikā" reimatoīdā artrīta apstākļos, pacientu procentuālais daudzums ar pozitīviem antivielu titriem pret S. pneimonija, gripa, cūciņa, masaliņas, vējbakas un stingumkrampju toksīns parasti bija līdzīgi sākotnējiem rādītājiem.
Citu DMARD vienlaicīga / secīga lietošana reimatoīdā artrīta ārstēšanā
Nav ieteicams vienlaikus lietot MabThera un pretreimatisma terapiju, kas nav norādīta reimatoīdā artrīta indikācijā un devā.
Ir ierobežoti dati no klīniskajiem pētījumiem, lai pilnībā novērtētu citu DMARD (ieskaitot TNF inhibitorus un citus bioloģiskos līdzekļus) secīgas lietošanas drošību pēc MabThera (ieskaitot 4.5. Apakšpunktu). Pieejamie dati liecina, ka klīniski nozīmīgu infekciju biežums nemainās, ja tiek lietota šī terapija lieto pacientiem, kas iepriekš ārstēti ar MabThera; tomēr, ja pēc terapijas ar MabThera tiek lietoti bioloģiskie aģenti un / vai DMARD, pacienti rūpīgi jānovēro attiecībā uz infekcijas pazīmēm.
Neoplazmas
Imūnmodulējošas zāles var palielināt vēža risku. Pamatojoties uz ierobežoto pieredzi ar MabThera lietošanu pacientiem ar reimatoīdo artrītu (skatīt 4.8. Apakšpunktu), pašreizējie dati neliecina par paaugstinātu ļaundabīgu audzēju risku, tomēr pašlaik nevar izslēgt iespējamo cieto audzēju attīstības risku.
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi
Pašlaik ir ierobežoti dati par iespējamo zāļu mijiedarbību ar MabThera.
Pacientiem ar HLL vienlaicīga lietošana ar MabThera neietekmē fludarabīna vai ciklofosfamīda farmakokinētiku. Turklāt fludarabīns un ciklofosfamīds acīmredzami neietekmē MabThera farmakokinētiku.
Vienlaicīga lietošana ar metotreksātu neietekmēja MabThera farmakokinētiku pacientiem ar reimatoīdo artrītu.
Pacientiem, kuriem ir izveidojušās anti-peles vai anti-himēriskas antivielas (HAMA / HACA), var rasties alerģiskas vai paaugstinātas jutības reakcijas, ārstējot ar citām diagnostiskām vai terapeitiskām monoklonālām antivielām.
Pacientiem ar reimatoīdo artrītu 283 pacienti pēc MabThera saņēma bioloģisku DMARD terapiju. Šiem pacientiem klīniski nozīmīgu infekciju biežums MabThera terapijas laikā bija 6,01 uz 100 pacienta gadiem, salīdzinot ar 4,97 uz 100 pacienta gadiem pēc bioloģiskās DMARD terapijas.
04.6 Grūtniecība un zīdīšana
Kontracepcija vīriešiem un sievietēm
Tā kā rituksimabam ir ilgs aiztures laiks pacientiem ar B šūnu trūkumu, sievietēm reproduktīvā vecumā ārstēšanas laikā un līdz 12 mēnešiem pēc MabThera terapijas beigām jāizmanto efektīvas kontracepcijas metodes.
Grūtniecība
Ir zināms, ka IgG imūnglobulīni šķērso placentāro barjeru.
B šūnu līmenis zīdaiņiem pēc mātes MabThera iedarbības nav novērtēts klīniskajos pētījumos. Nav adekvātu un labi kontrolētu datu par pētījumiem ar grūtniecēm, tomēr ir ziņots par pārejošu B šūnu samazināšanos un limfocitopēniju zīdaiņiem, kas dzimuši mātēm, kuras grūtniecības laikā ir pakļautas MabThera iedarbībai. Līdzīga ietekme tika novērota pētījumos ar dzīvniekiem (skatīt 5.3. Apakšpunktu). Šī iemesla dēļ MabThera nedrīkst lietot grūtniecēm, ja vien iespējamais ieguvums neatsver iespējamo risku.
Zīdīšanas periods
Nav zināms, vai rituksimabs izdalās mātes pienā. Tomēr, tā kā mātes IgG izdalās mātes pienā un rituksimabs tika konstatēts pērtiķu laktācijas laikā, sievietes nedrīkst barot bērnu ar krūti ārstēšanas laikā ar MabThera un 12 mēnešus pēc ārstēšanas ar MabThera.
Auglība
Pētījumi ar dzīvniekiem neatklāja rituksimaba kaitīgu ietekmi uz reproduktīvajiem orgāniem.
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus
Nav veikti pētījumi par MabThera ietekmi uz spēju vadīt transportlīdzekļus un apkalpot mehānismus, lai gan līdz šim ziņotā farmakoloģiskā aktivitāte un blakusparādības liecina, ka MabThera neietekmē vai nedaudz ietekmē spēju vadīt transportlīdzekļus un vadīt transportlīdzekļus.
04.8 Nevēlamās blakusparādības
Pieredze ne-Hodžkina limfomas un hroniskas limfoleikozes ārstēšanā
Drošības profila kopsavilkums
MabThera vispārējais drošības profils ne-Hodžkina limfomas un hroniskas limfoleikozes gadījumā ir balstīts uz datiem, kas iegūti pacientiem klīniskajos pētījumos un pēcreģistrācijas uzraudzībā. Šie pacienti tika ārstēti ar MabThera monoterapijā (kā indukcijas vai pēcindukcijas uzturošā terapija) vai kombinācijā ar ķīmijterapiju.
Visbiežāk novērotās nevēlamās blakusparādības (ADR) pacientiem, kuri saņēma MabThera, bija tie, kas radās lielākajai daļai pacientu pirmās infūzijas laikā. Ar infūziju saistīto simptomu biežums ievērojami samazinās ar nākamajām infūzijām un ir mazāks par 1% pēc astoņām MabThera devām.
Infekcijas gadījumi (galvenokārt baktēriju un vīrusu) radās aptuveni 30–55% NHL pacientu, kuri tika ārstēti klīniskajos pētījumos, un aptuveni 30–50% CLL pacientu, kuri tika ārstēti klīniskajos pētījumos. Visbiežāk ziņotās vai novērotās nopietnās zāļu blakusparādības bija:
• IRR (ieskaitot citokīnu izdalīšanās sindromu un audzēja sabrukšanas sindromu), skatīt apakšpunktu 4.4.
• Infekcijas, skatīt apakšpunktu 4.4.
• Sirds un asinsvadu sistēmas traucējumi, skatīt apakšpunktu 4.4.
Citas nopietnas blakusparādības, par kurām ziņots, ir B hepatīta reaktivācija un PML (skatīt apakšpunktu 4.4).
Blakusparādību saraksts tabulas veidā
Blakusparādību biežums, par kurām ziņots, lietojot tikai MabThera vai kombinācijā ar ķīmijterapiju, ir apkopots 1. tabulā. Katrā sastopamības biežuma klasē nevēlamās blakusparādības ir norādītas to smaguma pakāpes samazinājuma secībā. Biežums ir definēts kā ļoti bieži (≥ 1/10), bieži ( ≥ 1/100 līdz
Blakusparādības, kas konstatētas tikai pēcreģistrācijas uzraudzības laikā un kuru biežumu nevar noteikt, ir uzskaitītas sadaļā "nav zināms".
1. tabula. Nevēlamās blakusparādības, par kurām ziņots klīniskajos pētījumos vai pēcreģistrācijas uzraudzībā pacientiem ar NHL un HLL, kuri tika ārstēti ar MabThera kā monoterapiju / uzturēšanu vai kombinācijā ar ķīmijterapiju
Turpmāk minētie termini ir ziņoti kā nevēlami notikumi klīnisko pētījumu laikā; tomēr tika ziņots par hematoloģisku toksicitāti, neitropēnisku infekciju, urīnceļu infekciju, jušanas traucējumiem, pireksiju ar līdzīgu vai zemāku sastopamību MabThera grupās, salīdzinot ar kontroles grupām.
Vairāk nekā 50% pacientu klīniskajos pētījumos ir ziņots par raksturīgām ar infūziju saistītas reakcijas pazīmēm un simptomiem, un tās novērotas galvenokārt pirmās infūzijas laikā, parasti pirmajās divās stundās.Šie simptomi galvenokārt ir drudzis, drebuļi un stīvums. Citi simptomi ir pietvīkums, angioneirotiskā tūska, bronhu spazmas, vemšana, slikta dūša, nātrene / izsitumi, nogurums, galvassāpes, rīkles kairinājums, rinīts, nieze, sāpes, tahikardija, hipertensija, hipotensija, aizdusa, dispepsija, astēnija un audzēja sabrukšanas sindroma simptomi. -līdz 12% gadījumu radās ar to saistītas reakcijas (piemēram, bronhu spazmas, hipotensija). Papildu reakcijas, par kurām ziņots dažos gadījumos, bija miokarda infarkts, priekškambaru mirdzēšana, plaušu tūska un akūta atgriezeniska trombocitopēnija. Iepriekš pastāvošu sirds slimību, piemēram, stenokardijas vai sastrēguma sirds mazspējas vai smagas sirds slimības (sirds mazspēja, miokarda infarkts, priekškambaru mirdzēšana), plaušu tūska, vairāku orgānu mazspēja, audzēja sabrukšanas sindroms, citokīnu atbrīvošanās sindroms, nieru mazspēja un elpošanas sistēmas saasināšanās par kļūmēm ziņots retāk vai nezināmi. Ar infūziju saistīto simptomu biežums ievērojami samazinājās ar sekojošām infūzijām un ir
Blakusparādību atlases apraksts
Infekcijas
MabThera izraisa B šūnu samazināšanos aptuveni 70-80% pacientu, taču šis notikums ir saistīts ar imūnglobulīna līmeņa pazemināšanos serumā tikai nelielai daļai pacientu.
Randomizētos pētījumos MabThera grupā biežāk ziņots par lokalizētām kandidozes infekcijām, piemēram, herpes zoster. Par nopietnām infekcijām ziņots aptuveni 4% pacientu, kuri tika ārstēti ar MabThera monoterapiju. Salīdzinot ar novērojumiem, divu gadu uzturošās terapijas laikā ar MabThera tika novērots augstāks visu infekciju, ieskaitot 3. vai 4. pakāpes infekcijas, biežums. Divu gadu ārstēšanas periodā netika konstatēta kumulatīva toksicitāte attiecībā uz infekcijām. ārstēšanas laikā ar MabThera ir ziņots par citām nopietnām vīrusu infekcijām - jaunām, atjaunotām vai saasinātām, no kurām dažas bija letālas. Lielākā daļa pacientu saņēma MabThera kombinācijā ar ķīmijterapiju vai kā daļu no asinsrades cilmes šūnu transplantācijas. Šo nopietno vīrusu infekciju piemēri ir infekcijas, ko izraisa herpes vīrusi (citomegalovīruss, Varicella Zoster vīruss un Herpes simplex), JC vīruss (progresējoša multifokāla leikoencefalopātija (PML)) un C hepatīta vīruss. Klīnisko pētījumu laikā ir ziņots arī par letālu PML gadījumiem, un tie ir notikuši ti pēc slimības progresēšanas un atkārtotas ārstēšanas. Ir ziņots par B hepatīta reaktivācijas gadījumiem, no kuriem lielākā daļa novērota pacientiem, kuri saņēma MabThera kombinācijā ar citotoksisku ķīmijterapiju. Pacientiem ar recidivējošu / refraktāru HLL 3/4 pakāpes B hepatīta infekcijas (reaktivācijas un primārās infekcijas) sastopamība bija 2% R-FC un 0% FC. Tika novērota Kapoši sarkomas progresēšana. jau esoša Kapoši sarkoma Šie gadījumi notika ar neapstiprinātām indikācijām, un lielākā daļa pacientu bija HIV pozitīvi.
Hematoloģiskas blakusparādības
Klīniskajos pētījumos, lietojot MabThera kā monoterapiju 4 nedēļas, hematoloģiskas novirzes radās daļai pacientu un parasti bija vieglas un atgriezeniskas. Par smagu (3./4. Pakāpes) neitropēniju ziņots 4,2% pacientu, anēmiju - 1,1% un trombocitopēniju - 1,7% pacientu. Divu gadu uzturošās terapijas laikā ar MabThera leikopēnija (5% vs 2%, 3/4 pakāpe) un neitropēnija (10%) vs 4%, 3/4 pakāpe) tika ziņots ar lielāku sastopamību salīdzinājumā ar novērošanu. Trombocitopēnijas biežums bija zems (salīdzinot ar CHOP 79%, R-FC 23% vsHR 12%), neitropēnija (R-CVP 24% vs CVP 14%; R-CHOP 97% vs CHOP 88%, R-FC 30% vs HR 19% iepriekš neapstrādātā HLL), pancitopēnija (R-FC 3% vs CF 1% iepriekš neapstrādātā HLL), parasti tika ziņots ar lielāku biežumu, salīdzinot ar tikai ķīmijterapiju. Tomēr lielāks neitropēnijas biežums pacientiem, kuri tika ārstēti ar MabThera un ķīmijterapiju, nebija saistīts ar lielāku infekciju un invāziju biežumu, salīdzinot ar pacientiem, kuri tika ārstēti tikai ar ķīmijterapiju. Iepriekš neārstēti un recidivējoši / refraktāri HLL pētījumi atklāja, ka 25% ārstēto pacientu lietojot R-FC, neitropēnija bija ilgstoša (definēta kā neitrofilo granulocītu skaits mazāks par 1x109 / l no 24. līdz 42. dienai pēc pēdējās devas) vai parādījās ar vēlu (pēc neitrofilu granulocītu skaita mazāk nekā 1x109 / l pēc 42. dienas) pēc pēdējās devas pacientiem, kuriem iepriekš nebija ilgstošas neitropēnijas vai kuri atveseļojās pirms 42. dienas) pēc ārstēšanas ar MabThera un CF.
Nav ziņots par anēmijas biežuma atšķirībām .. Ir ziņots par dažiem novēlotas neitropēnijas gadījumiem, kas notikuši vairāk nekā četras nedēļas pēc pēdējās MabThera infūzijas. Pirmās rindas CLL pētījumā Binet C stadijas pacientiem R-FC grupā bija vairāk nevēlamu blakusparādību nekā FC grupā (R-FC 83% vs HR 71%). Recidivējošā / ugunsizturīgā HLL pētījumā 3/4 pakāpes trombocitopēnija tika ziņota 11% pacientu RFC grupā, salīdzinot ar 9% pacientu CF grupā.
Pētījumos ar MabThera pacientiem ar Valdestroma makroglobulinēmiju pēc ārstēšanas uzsākšanas novērots pārejošs IgM līmeņa paaugstināšanās serumā, kas var būt saistīts ar hiperviskozitāti un ar to saistītiem simptomiem. Pārejošs IgM pieaugums parasti atgriežas vismaz sākotnējā līmenī mēnešus.
Sirds un asinsvadu sistēmas blakusparādības
Klīniskajos pētījumos, lietojot tikai MabThera, kardiovaskulāras reakcijas tika ziņotas 18,8% pacientu ar hipotensiju un hipertensiju kā visbiežāk ziņotie notikumi. Infūzijas laikā ziņots par 3. vai 4. pakāpes aritmiju (ieskaitot ventrikulāru un supraventrikulāru tahikardiju) un stenokardijas gadījumiem. Uzturošās terapijas laikā 3/4 pakāpes sirdsdarbības traucējumu biežums ārstētajiem pacientiem bija salīdzināms ar MabThera un novērošanu. tika ziņots par nopietnām blakusparādībām (ieskaitot priekškambaru mirdzēšanu, miokarda infarktu, kreisā kambara mazspēju, miokarda išēmiju) 3% ar MabThera ārstētu pacientu, salīdzinot ar 3. un 4. pakāpes sirds aritmiju, īpaši supraventrikulārām aritmijām, piemēram, tahikardiju un priekškambaru plandīšanos. augstāks RCHOP grupā (14 pacienti, 6,9%), salīdzinot ar CHOP grupu (3 pacienti, 1,5%). Visas šīs aritmijas radās MabThera infūzijas kontekstā vai bija saistītas ar tādiem predisponējošiem apstākļiem kā drudzis, infekcija, akūts miokarda infarkts vai jau esošas elpošanas un sirds un asinsvadu slimības. R-CHOP un CHOP grupā atšķirības netika novērotas. citu 3. un 4. pakāpes sirdsdarbības traucējumu, tai skaitā sirds mazspējas, miokarda slimības un koronāro artēriju slimības izpausmju biežumu. HLL gadījumā 3. vai 4. pakāpes sirdsdarbības traucējumu kopējā sastopamība bija zema gan pirmās rindas pētījumā (4% R-FC, 3% FC), gan recidīva / ugunsizturīgā pētījumā (4% R-FC, 4% FC) .
Elpošanas sistēmas
Ir ziņots par intersticiālas plaušu slimības gadījumiem, daži ar letālu iznākumu.
Neiroloģiskās patoloģijas
Ārstēšanas periodā (indukcijas terapijas fāze, kas sastāv no R-CHOP līdz astoņiem cikliem) četriem pacientiem (2%), kuri tika ārstēti ar R-CHOP, visiem ar kardiovaskulāriem riska faktoriem, pirmajā ārstēšanas ciklā bija cerebrovaskulāras trombembolijas nelaimes gadījumi. Citu trombembolisku notikumu biežuma ziņā starp ārstēšanas grupām nebija atšķirību. Turpretī trīs pacientiem (1,5%) CHOP grupā bija cerebrovaskulāri traucējumi, kas visi notika novērošanas periodā. HLL, kopējais 3. vai 4. pakāpes nervu sistēmas traucējumu biežums bija zems gan pirmās rindas pētījumā (4% R-FC, 4% FC), gan recidīva / ugunsizturīgā pētījumā (3% R-FC, 3% FC) .
Ir ziņots par aizmugurējās atgriezeniskās encefalopātijas sindroma (PRES) / aizmugurējās atgriezeniskās leikoencefalopātijas sindroma (RPLS) gadījumiem. Pazīmes un simptomi bija redzes traucējumi, galvassāpes, krampji un garīgā stāvokļa izmaiņas ar vai bez saistītās hipertensijas. PRES / RPLS diagnozei nepieciešams apstiprinājums ar attēlveidošana smadzeņu. Ziņotajos gadījumos ir atzīti PRES / RPLS riska faktori, tostarp pacienta vienlaikus slimības stāvoklis, hipertensija, imūnsupresīva terapija un / vai ķīmijterapija.
Kuņģa -zarnu trakta traucējumi
Ir novērota kuņģa-zarnu trakta perforācija, kas dažos gadījumos izraisīja nāvi pacientiem, kuri saņēma MabThera ne-Hodžkina limfomas ārstēšanai. Vairumā gadījumu MabThera lietoja kopā ar ķīmijterapiju.
IgG līmenis
Klīniskajā pētījumā, kurā novērtēja MabThera uzturošo terapiju recidivējošas / refraktīvas folikulāras limfomas gadījumā, vidējais IgG līmenis bija zem normas (LLN) apakšējās robežas (
Ar MabThera ārstētiem pediatriskiem pacientiem novērots neliels skaits spontānu un literatūras gadījumu, kas saistīti ar hipogammaglobulinēmiju, dažos gadījumos smagu un kam nepieciešama ilgstoša imūnglobulīna aizstājterapija. Ilgstošas B šūnu samazināšanās sekas pediatrijas pacientiem nav zināmas.
Ādas un zemādas audu bojājumi
Ļoti reti ziņots par toksiskas epidermas nekrolīzes (Laiela sindroma) un Stīvensa-Džonsona sindroma gadījumiem, dažos gadījumos ar letālu iznākumu.
Pacientu apakšpopulācijas - MabThera monoterapija
Gados vecāki pacienti (≥ 65 gadus veci):
Visu pakāpju un 3./4. Pakāpes nevēlamo blakusparādību sastopamība bija līdzīga gados vecākiem un jaunākiem pacientiem (
Lielgabarīta slimība
Pacientiem ar lielgabarīta slimību bija lielāks 3./4. Pakāpes blakusparādību biežums nekā pacientiem bez lielgabarīta slimības (25,6% vs 15,4%). Visu pakāpju blakusparādību sastopamība šajās divās grupās bija līdzīga.
Atkārtota ārstēšana
To pacientu īpatsvars, kuri ziņoja par nevēlamām blakusparādībām atkārtotas ārstēšanas laikā ar turpmākiem MabThera kursiem, bija līdzīga to pacientu daļai, kuri ziņoja par blakusparādībām sākotnējās iedarbības laikā (visas 3. un 4. pakāpes blakusparādības).
Pacientu apakšpopulācijas - kombinētā terapija ar MabThera
Gados vecāki pacienti (≥ 65 gadi)
3. un 4. pakāpes nevēlamo blakusparādību sastopamība asinīs un limfātiskajā sistēmā gados vecākiem pacientiem bija augstāka nekā jaunākiem pacientiem (
Pieredze reimatoīdā artrīta ārstēšanā
Drošības profila kopsavilkums
MabThera vispārējais drošības profils reimatoīdā artrīta gadījumā ir balstīts uz datiem, kas iegūti klīniskajos pētījumos ārstētiem pacientiem un pēcreģistrācijas uzraudzībā.
Turpmākajās sadaļās ir apkopots MabThera drošības profils pacientiem ar vidēji smagu vai smagu reimatoīdo artrītu. Klīniskajos pētījumos vairāk nekā 3100 pacientu saņēma vismaz vienu ārstēšanas kursu un tika novēroti laika posmā no 6 mēnešiem līdz vairāk nekā 5 gadiem; aptuveni 2400 pacienti saņēma divus vai vairākus ārstēšanas kursus, un vairāk nekā 1000 pacientu saņēma 5 vai vairāk kursus. Informācija par drošību, kas apkopota pēcreģistrācijas periodā, atspoguļo paredzamo blakusparādību profilu, kas jau novērots MabThera klīniskajos pētījumos (skatīt apakšpunktu 4.4).
Pacienti saņēma 2 1000 mg MabThera devas ar divu nedēļu intervālu kombinācijā ar metotreksātu (10-25 mg nedēļā). MabThera infūzijas tika ievadītas pēc 100 mg metilprednizolona intravenozas infūzijas; pacienti arī saņēma perorālu prednizona terapiju 15 dienas.
Blakusparādību saraksts tabulas veidā
Blakusparādības ir uzskaitītas 2. tabulā. Biežums ir definēts kā ļoti bieži (≥ 1/10), bieži (≥ 1/100 līdz
Visbiežāk novērotās nevēlamās blakusparādības, kuras, domājams, bija saistītas ar MabThera lietošanu, bija IRR. Kopējais IRR sastopamības biežums klīniskajos pētījumos bija 23% ar pirmo infūziju un samazinājās ar nākamajām infūzijām. Nopietni IRR bija retāk sastopami (0,5% pacientu) un pārsvarā parādījās sākotnējā cikla laikā. Papildus blakusparādībām, kas novērotas reimatoīdā artrīta klīniskajos pētījumos ar MabThera, pēcreģistrācijas periodā ziņots par progresējošu multifokālu leikoencefalopātiju (PML) un seruma slimībai līdzīgu reakciju.
2. tabula. Kopsavilkums par blakusparādībām, par kurām ziņots klīniskajos pētījumos vai pēcreģistrācijas uzraudzības laikā, kas radušās pacientiem ar reimatoīdo artrītu, kuri saņēma MabThera.
Atkārtoti cikli
Atkārtoti ārstēšanas kursi ir saistīti ar līdzīgu blakusparādību profilu, kāds novērots pēc pirmās iedarbības. Visu nevēlamo blakusparādību biežums pēc pirmās MabThera iedarbības bija augstākais pirmo 6 mēnešu laikā un pēc tam samazinājās. Tas galvenokārt attiecās uz IRR (visbiežāk pirmās ārstēšanas laikā), reimatoīdā artrīta un infekciju paasinājumu; tas viss bija biežāks pirmajos 6 ārstēšanas mēnešos.
Ar infūziju saistītas reakcijas
Klīniskajos pētījumos pēc ārstēšanas ar MabThera visbiežāk novērotās nevēlamās blakusparādības bija blakusparādības (skatīt 2. tabulu). No 3189 pacientiem, kuri tika ārstēti ar MabThera, 1135 (36%) bija vismaz viens IRR, 733/3189 (23%) pacientu pēc pirmās MabThera terapijas pirmās infūzijas radās IRR. Ar sekojošām infūzijām IRR sastopamības biežums samazinās.Klīniskos pētījumos mazāk nekā 1% (17/3189) pacientu novēroja smagu IRR. Klīniskajos pētījumos nebija vispārēju toksicitātes kritēriju (CTC) 4. pakāpes IRR un nāves gadījumu IRR dēļ. CTC 3. pakāpes notikumu un IRR īpatsvars, kas noveda pie ārstēšanas pārtraukšanas, ārstēšanas laikā samazinājās un, sākot ar 3. ciklu, bija reti. Intravenoza glikokortikoīdu premedikācija ievērojami samazināja IRR sastopamību un smagumu (skatīt 4.2. Un 4.4. Apakšpunktu). Pēcreģistrācijas periodā ziņots par nopietniem IRR gadījumiem ar letālu iznākumu.
Pētījumā, kura mērķis bija novērtēt "ātrākas MabThera infūzijas drošību pacientiem ar reimatoīdo artrītu, pacientiem ar vidēji smagu vai smagu aktīvu reimatoīdo artrītu, kuriem pirmās pētītās infūzijas laikā vai 24 stundu laikā pēc tās nebija smagas IRR, tika atļauts veikt 2 stundu intravenozu MabThera infūziju. Pacienti, kuriem anamnēzē bija smaga infūzijas reakcija uz reimatoīdā artrīta bioloģisko terapiju, netika iekļauti pētījumā. IRR sastopamība, veidi un smagums atbilda vēsturiskajiem datiem.Nopietni IRR netika novēroti.
Blakusparādību atlases apraksts
Infekcijas
Kopējais infekciju sastopamības biežums MabThera grupā bija aptuveni 94 uz 100 pacientu gadiem. Infekcijas pārsvarā bija vieglas vai vidēji smagas, un tās ietvēra galvenokārt augšējo elpceļu un urīnceļu infekcijas. Tām bija nepieciešamas IV antibiotikas tas bija apmēram 4 no 100 pacientu gadiem. Nopietnu infekciju biežums pēc atkārtotiem MabThera kursiem būtiski nepalielinājās. Klīniskajos pētījumos tika ziņots par apakšējo elpceļu infekcijām (ieskaitot pneimoniju), līdzīgu sastopamību MabThera grupās salīdzinājumā ar MabThera grupām. Progresējošas multifokālas leikoencefalopātijas gadījumi ar letālu iznākumu ir ziņots pēc MabThera lietošanas autoimūno slimību ārstēšanai. Tie ietver reimatoīdo artrītu un tādus autoimūnos stāvokļus kā indikācijas, piemēram, sistēmisku sarkano vilkēdi (SLE) un vaskulītu. Ir ziņots par B hepatīta reaktivāciju pacientiem ar ne Hodžkina limfomu, kuri saņēma MabThera kombinācijā ar citotoksisku ķīmijterapiju. (Skatīt ne-Hodžkina limfomu .) Ļoti reti ziņots arī par B hepatīta infekcijas atkārtošanos RA pacientiem, kuri saņēma MabThera (skatīt apakšpunktu 4.4).
Sirds un asinsvadu sistēmas blakusparādības
Nopietnas sirds reakcijas tika novērotas ar "biežumu 1,3 uz 100 pacienta gadiem pacientiem, kuri tika ārstēti ar MabThera, un 1,3 gadījumiem uz 100 pacientgadiem, kuri tika ārstēti ar placebo. Pacientu ar sirds reakcijām (visu vai smagu) īpatsvars nepalielinājās. dažādi cikli.
Neiroloģiski notikumi
Ir ziņots par aizmugurējās atgriezeniskās encefalopātiskā sindroma (PRES) / aizmugurējās atgriezeniskās leikoencefalopātijas sindroma (RPLS) gadījumiem. Pazīmes un simptomi bija redzes traucējumi, galvassāpes, krampji un izmainīts garīgais stāvoklis ar vai bez saistītās hipertensijas. PRES / RPLS diagnozei nepieciešams apstiprinājums, izmantojot smadzeņu attēlveidošanu. Aprakstītajiem gadījumiem bija zināmi PRES / RPLS riska faktori, tostarp pacientu pamatslimība, hipertensija, imūnsupresīvā terapija un / vai ķīmijterapija.
Neitropēnija
Pēc ārstēšanas ar MabThera tika novēroti neitropēnijas gadījumi, no kuriem lielākā daļa bija pārejoši un vieglas vai mērenas intensitātes. Neitropēnija var rasties vairākus mēnešus pēc MabThera ievadīšanas (skatīt apakšpunktu 4.4).
Placebo kontrolētos klīniskos pētījumos 0,94% (13/382) ar MabThera ārstētiem pacientiem un 0,27% (2/731) ar placebo ārstētiem pacientiem attīstījās smaga neitropēnija.
Pēcreģistrācijas periodā reti ziņots par neitropēniskiem gadījumiem, tostarp smagu un ilgstošu neitropēniju, kas dažkārt bijusi saistīta ar letālām infekcijām.
Ādas un zemādas audu bojājumi
Ļoti reti ziņots par toksiskas epidermas nekrolīzes (Laiela sindroma) un Stīvensa-Džonsona sindroma gadījumiem, dažos gadījumos ar letālu iznākumu.
Laboratorijas anomālijas
Pacientiem ar reimatoīdo artrītu, kas ārstēti ar MabThera, novērota hipogammaglobulinēmija (IgG vai IgM zem apakšējās normas robežas). Vispārējo vai smago infekciju biežums nepalielinājās pēc zema IgG vai IgM līmeņa (skatīt apakšpunktu 4.4).
Ar MabThera ārstētiem pediatriskiem pacientiem novērots neliels skaits spontānu un literatūras gadījumu, kas saistīti ar hipogammaglobulinēmiju, dažos gadījumos smagu un kam nepieciešama ilgstoša imūnglobulīna aizstājterapija. Ilgstošas B šūnu samazināšanās sekas pediatrijas pacientiem nav zināmas.
Pieredze granulomatozes gadījumā ar poliangiītu un mikroskopisku poliangiītu
Klīniskajā pētījumā par granulomatozi ar poliangiītu un mikroskopisku poliangiītu 99 pacienti tika ārstēti ar MabThera (375 mg / m2, vienu reizi nedēļā 4 nedēļas) un glikokortikoīdiem (skatīt 5.1. Apakšpunktu).
Blakusparādību saraksts tabulas veidā
3. tabulā uzskaitītās blakusparādības atspoguļo visas blakusparādības, kas radušās ar biežumu ≥ 5% MabThera grupā.
3. tabula. Nevēlamās zāļu reakcijas, kas rodas ≥ 5% pacientu, kuri saņēma MabThera un biežāk nekā salīdzinošā grupa 6 mēnešus ilgajā klīniskajā pētījumā.
Nevēlamo zāļu blakusparādību izvēle
Ar infūziju saistītas reakcijas
IRR klīniskajos pētījumos, kas attiecas uz granulomatozi ar poliangiītu un mikroskopisku poliangiītu, tika definēti kā jebkādi nevēlami notikumi, kas parādījās 24 stundu laikā pēc infūzijas, un pētnieki drošības grupā uzskatīja, ka tie ir saistīti ar infūziju. 99 pacienti tika ārstēti ar MabThera un 12% bija vismaz viens IRR. Visi IRR bija 1. vai 2. pakāpe saskaņā ar CTC. Visbiežāk sastopamā IRR bija citokīnu izdalīšanās sindroms, karstuma viļņi, rīkles kairinājums un trīce.MabThera lietoja kombinācijā ar intravenoziem glikokortikoīdiem, kas var samazināt šo notikumu biežumu un smagumu.
Infekcijas
99 pacientiem, kuri tika ārstēti ar MabThera, kopējais infekciju biežums bija aptuveni 237 uz 100 pacientu gadiem (95% TI 197-285) sešu mēnešu primārajā mērķa punktā. Infekcijas pārsvarā bija vieglas vai vidēji smagas un galvenokārt sastāvēja no elpceļu infekcijām. trakta, herpes zoster un urīnceļu infekcijas. Nopietnu infekciju biežums bija aptuveni 25 uz 100 pacientu gadiem. Visbiežāk ziņotā nopietnā infekcija MabThera grupā bija pneimonija ar biežumu 4%.
Neoplazmas
Ļaundabīgo audzēju sastopamība pacientiem, kuri tika ārstēti ar MabThera klīniskajos pētījumos, kas attiecas uz granulomatozi ar poliangiītu un mikroskopisku poliangiītu, kopīgā pētījuma beigu datumā (kad pēdējais pacients pabeidza novērošanas periodu) bija 2,00 uz 100 pacienta gadiem. Pamatojoties uz standartizēto sastopamības koeficientu, ļaundabīgo audzēju biežums, šķiet, ir līdzīgs tam, kas iepriekš tika ziņots pacientiem ar ANCA saistītu vaskulītu.
Sirds un asinsvadu sistēmas blakusparādības
Sirdsdarbības traucējumi sešu mēnešu primārajā mērķa rādītājā bija aptuveni 273 uz 100 pacientu gadiem (95 % TI 149-470). Nopietno sirdsdarbības gadījumu skaits bija 2,2 uz 100 pacientu gadiem (95 % TI 3–15) Visbiežāk ziņotā blakusparādība bija tahikardija (4%) un priekškambaru mirdzēšana (3%) (skatīt apakšpunktu 4.4).
Neiroloģiski notikumi
Ir ziņots par aizmugurējās atgriezeniskās encefalopātijas sindroma (PRES) / aizmugurējās atgriezeniskās leikoencefalopātijas sindroma (RPLS) gadījumiem. Pazīmes un simptomi bija redzes traucējumi, galvassāpes, krampji un mainīts garīgais stāvoklis ar vai bez saistītās hipertensijas. PRES / RPLS diagnozei nepieciešams apstiprinājums, izmantojot smadzeņu attēlveidošanu. Aprakstītajiem gadījumiem bija zināmi PRES / RPLS riska faktori, tostarp pacientu pamatslimība, hipertensija, imūnsupresīvā terapija un / vai ķīmijterapija.
B hepatīta reaktivācija
Pēcreģistrācijas periodā ar MabThera ārstētiem pacientiem ar granulomatozi ar poliangiītu un mikroskopisku poliangiītu ziņots par dažiem B hepatīta reaktivācijas gadījumiem, dažos gadījumos ar letālu iznākumu.
Hipogammaglobulinēmija
Pacientiem ar granulomatozi ar poliangiītu un mikroskopisku poliangiītu, kas ārstēti ar MabThera, novērota hipogammaglobulinēmija (IgA, IgG vai IgM zem apakšējās normas robežas).6 mēnešus ilgā, vairāku centru, randomizētā, dubultmaskētā, aktīvi kontrolētā ne zemākas pakāpes pētījumā MabThera grupā 27%, 58%un 51%pacientu ar normālu sākotnējo imūnglobulīna līmeni bija zems IgA līmenis, IgG un IgM attiecīgi, salīdzinot ar 25%, 50% un 46% ciklofosfamīdu grupas. Pacientiem ar zemu IgA, IgG vai IgM līmeni netika novērots paaugstināts vispārējo infekciju vai nopietnu infekciju skaits.
Neitropēnija
Daudzcentru, randomizētā, dubultmaskētā, aktīvi kontrolētā MabThera mazvērtības pētījumā granulomatozei ar poliangiītu un mikroskopisku poliangiītu 24% pacientu MabThera grupā (viens cikls) un 23% pacientu ciklofosfamīda grupā ir attīstījusies CTC 3. pakāpes vai augstāka neitropēnija. Neitropēnija nebija saistīta ar novērotu nopietnu infekciju pieaugumu pacientiem, kuri tika ārstēti ar MabThera. Klīniskajos pētījumos nav pētīta vairāku MabThera kursu ietekme uz neitropēnijas attīstību pacientiem ar granulomatozi ar poliangiītu un mikroskopisku poliangiītu.
Ādas un zemādas audu bojājumi:
Ļoti reti ziņots par toksiskas epidermas nekrolīzes (Laiela sindroma) un Stīvensa-Džonsona sindroma epizodēm, dažām ar letālu iznākumu.
Ziņošana par iespējamām blakusparādībām
Ir svarīgi ziņot par iespējamām blakusparādībām, kas radušās pēc zāļu reģistrācijas, jo tas ļauj nepārtraukti uzraudzīt zāļu ieguvuma un riska attiecību. Veselības aprūpes speciālisti tiek lūgti ziņot par visām iespējamām blakusparādībām, izmantojot valsts ziņošanas sistēmu.
04.9 Pārdozēšana
Ir ierobežota pieredze klīniskajos pētījumos ar cilvēkiem, kuri lietoja lielākas devas, nekā apstiprinātas MabThera intravenozai zāļu formai. Līdz šim lielākā cilvēkiem pārbaudītā MabThera deva ir 5000 mg (2250 mg / m2), kas pārbaudīta. pacientiem ar hronisku limfoleikozi. Citas drošības zīmes netika konstatētas.
Pacientiem, kuriem rodas pārdozēšana, nekavējoties jāpārtrauc infūzija un rūpīgi jāuzrauga.
Pēcreģistrācijas periodā ziņots par pieciem MabThera pārdozēšanas gadījumiem. Trīs no šiem gadījumiem neziņoja par nevēlamiem notikumiem. Divas nevēlamās blakusparādības, par kurām tika ziņots, bija gripai līdzīgi simptomi ar 1,8 g rituksimaba devu un letāla elpošanas mazspēja, lietojot 2 g rituksimaba.
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS
05.1 Farmakodinamiskās īpašības
Farmakoterapeitiskā grupa: pretaudzēju līdzekļi, monoklonālas antivielas, ATĶ kods: L01X C02.
Rituksimabs specifiski saistās ar CD20 transmembrānu antigēnu, kas nav glikozilēts fosfoproteīns, kas atrodams pirms B limfocītos un nobriedušos B limfocītos. Antigēns ir izteikts vairāk nekā 95% no visām ne-Hodžkina šūnu limfomas B (NHL).
CD20 ir sastopams normālās un jaunveidojošās B šūnās, bet ne asinsrades cilmes šūnās, pro-B šūnās, normālās plazmas šūnās vai citos normālos audos. Antigēns netiek internalizēts pēc antivielu saistīšanās un netiek izplatīts no šūnas virsmas. CD20 necirkulē asinīs kā brīvais antigēns un tāpēc nekonkurē ar saistīšanos ar antivielām. Rituksimaba Fab domēns saistās ar CD20 antigēnu uz B limfocītiem. . un Fc domēns var aktivizēt imūnsistēmas efektorfunkcijas, lai izraisītu B šūnu lizēšanu. Iespējamie efektoru izraisīto šūnu līzes mehānismi ietver no komplementa atkarīgu citotoksicitāti (CDC), saistoties ar C1q un no antivielām atkarīgo šūnu citotoksicitāti (ADCC) ), ko izraisa viens vai vairāki Fcy receptori uz granulocītu, makrofāgu un NK šūnu virsmas. Ir pierādīts, ka rituksimaba saistīšanās ar CD20 antigēnu uz B limfocītiem izraisa arī šūnu nāvi apoptozes rezultātā.
Pēc pirmās MabThera devas ievadīšanas perifēro B šūnu skaits nokrita zem normas. Pacientiem, kurus ārstē no hematoloģiskiem vēža veidiem, B šūnu atjaunošanās tiek uzsākta 6 mēnešu laikā pēc ārstēšanas un parasti atgriežas normālā līmenī 12 mēnešu laikā pēc terapijas pabeigšanas, lai gan dažiem pacientiem atveseļošanās var būt ilgāka (ar atveseļošanās mediānu 23 mēneši pēc indukcijas) terapija). Pacientiem ar reimatoīdo artrītu tūlītēja perifēro asiņu B šūnu skaita samazināšanās tika novērota pēc divām MabThera 1000 mg infūzijām, atdalot ar 14 dienu intervālu. Perifēro B šūnu skaits sāk pieaugt no 24. nedēļas, un vairumam pacientu no 40. nedēļas ir redzamas atveseļošanās pazīmes gan MabThera monoterapijā, gan kombinācijā ar metotreksātu. Nelielai daļai pacientu pēc pēdējās MabThera devas novēroja ilgstošu perifēro B šūnu samazināšanos 2 gadus vai ilgāk. Pacientiem ar granulomatozi ar poliangiītu vai mikroskopisku poliangiītu perifēro asiņu B šūnu skaits samazinājās līdz 2 un palika šajā līmenī lielākā daļa pacientu līdz laika punkts 6 mēneši. Lielākajai daļai pacientu (81%) 12 mēnešu laikā bija B šūnu atjaunošanās pazīmes, kuru skaits> 10 šūnas / μl, līdz 18. mēnesim sasniedzot 87% pacientu.
Klīniskā pieredze ne-Hodžkina limfomas un hroniskas limfoleikozes gadījumā
Folikulāra limfoma
Monoterapija
Sākotnējā ārstēšana reizi nedēļā 4 devām
Pivotālajā pētījumā 166 pacienti ar recidivējošu vai ķīmijizturīgu zemas pakāpes vai folikulāru B šūnu NHL saņēma 375 mg / m2 MabThera intravenozas infūzijas veidā reizi nedēļā četras nedēļas. Kopējās atbildes (ORR) procentuālā daļa populācijā, kas novērtēta saskaņā ar "nodoms ārstēt analīzi (ITT) bija 48% (95% TI 41% - 56%) ar 6% pilnīgu atbilžu (CR) un 42% daļēju atbilžu (PR). Vidējais laiks līdz progresēšanai (TTP) pacientiem, kas reaģēja uz ārstēšanu, bija 13,0 mēneši. Apakšgrupu analīzē ORR bija augstāks pacientiem ar IWF histoloģiskiem B, C un D apakštipiem, salīdzinot ar pacientiem ar IWF histoloģisko A apakštipu (58% pret 12%), pacientiem ar lielāku bojājuma diametru 7 cm (53% pret 38% ) un pacientiem ar ķīmijjutīgu recidīvu, salīdzinot ar pacientiem ar ķīmijizturīgu recidīvu (definēts kā atbildes reakcijas ilgums)
ORR pacientiem, kuri iepriekš tika ārstēti ar autologu kaulu smadzeņu transplantāciju (ABMT), bija 78% salīdzinājumā ar 43% pacientiem, kuri iepriekš nebija ārstēti ar ABMT. Vecums, dzimums, limfomas pakāpe, sākotnējā diagnoze, lielgabarīta slimības klātbūtne vai neesamība, normāls vai paaugstināts LDH , ekstranodālās slimības klātbūtnei nebija statistiski nozīmīgas ietekmes (Fišera tests) uz atbildes reakciju uz MabThera. Tika konstatēta statistiski nozīmīga korelācija starp atbildes reakcijas ātrumu un kaulu smadzeņu iesaistīšanos. 40% pacientu ar kaulu smadzeņu iesaistīšanos atbildēja, salīdzinot ar 59% pacientu bez kaulu smadzeņu iesaistīšanās (p = 0,0186). Šo secinājumu neatbalstīja tā sauktā "pakāpeniskā loģistikas regresijas" analīze, kurā kā prognostiski faktori tika identificēti šādi faktori: histoloģiskais tips, sākotnējais bcl-2 pozitivitāte, rezistence pret pēdējo ķīmijterapiju un apjomīga slimība.
Sākotnējā ārstēšana reizi nedēļā 8 devām
Daudzcentru, vienas rokas pētījumā 37 pacienti ar recidivējošu vai ķīmijizturīgu, zemas pakāpes vai folikulāru B šūnu NHL saņēma MabThera 375 mg / m2 iknedēļas intravenozas infūzijas veidā astoņas devas. ORR bija 57% (95% ticamības intervāls (TI): 41% - 73%; CR 14%, PR 43%), un vidējā TTP prognoze respondentiem bija 19,4 mēneši (diapazons no 5,3 līdz 38,9 mēnešiem).
Sākotnējā ārstēšana, apjomīga slimība, katru nedēļu 4 devas
Datu apkopojumā no 3 pētījumiem 39 pacienti ar recidivējošu vai ķīmijizturīgu NHL, lielgabarīta slimību (viens bojājums ≥ 10 cm diametrā), zemas pakāpes vai folikulāra B šūnu slimība saņēma MabThera 375 mg / m2 iknedēļas intravenozas infūzijas veidā četriem pacientiem devas. ORR bija 36% (95% TI 21% - 51%; CR 3%, PR 33%) ar vidējo TTP reaģējošiem pacientiem 9,6 mēnešus (diapazons 4,5 - 26,8 mēneši).
Atkārtota ārstēšana, katru nedēļu 4 devas
Daudzcentru vienas rokas pētījumā 58 pacienti ar recidivējošu vai ķīmijizturīgu zemas pakāpes vai folikulāru B šūnu NHL, kuri bija sasnieguši objektīvu klīnisku atbildes reakciju uz iepriekšējo MabThera terapijas kursu, tika atkārtoti ārstēti ar 375 mg / m2 MabThera iknedēļas intravenozu infūziju četrām devām. Trīs no šiem pacientiem pirms uzņemšanas bija saņēmuši divus MabThera kursus un tādējādi saņēma trešo pētījuma kursu. Divi pacienti pētījumā tika ārstēti divas reizes. Pētījumā iekļautajām 60 atkārtotām terapijām ORR bija 38% (95% TI 26% - 51%; 10% CR, 28% PR) ar vidējo TTP prognozi reaģējošiem pacientiem 17,8 mēnešus (diapazons 5, 4-26,6) . Šie dati ir labāki par TTP, kas iegūts pēc pirmā MabThera kursa (12,4 mēneši).
Sākotnējā ārstēšana kombinācijā ar ķīmijterapiju
Randomizētā atklātā klīniskajā pētījumā kopumā 322 pacienti, kuri iepriekš nebija ārstēti ar folikulāru limfomu, tika randomizēti vai nu ar CVP ķīmijterapiju (ciklofosfamīds 750 mg / m2, vinkristīns 1,4 mg / m2 līdz maksimāli 2 mg 1. dienā) un prednizolons 40 mg / m2 dienā 1.-5. Dienā) ik pēc 3 nedēļām 8 ciklus vai MabThera 375 mg / m2 kombinācijā ar CVP (R-CVP). MabThera tika ievadīts katra ārstēšanas cikla pirmajā dienā. Kopā 321 pacients (162 R-CVP, 159 CVP) saņēma terapiju un tika analizēta efektivitāte. Vidējais pacientu novērošanas ilgums bija 53 mēneši. R-CVP radīja būtisku labumu salīdzinājumā ar CVP primārajam mērķa kritērijam, t.i., laikam līdz ārstēšanas neveiksmei (27 mēneši pret 6,6 mēnešiem, p
Atšķirība starp ārstēšanas grupām kopējā dzīvildzē uzrādīja būtisku klīnisku atšķirību (p = 0,029, log-rank tests stratificēts pēc centra): 53 mēnešu izdzīvošanas rādītājs R grupas pacientiem bija 80,9%. CVP salīdzinājumā ar 71,1% pacienti CVP grupā.
Rezultāti, kas iegūti trīs citos randomizētos pētījumos, kuros tika izmantota MabThera kombinācijā ar ķīmijterapijas shēmām, kas nav CVP (CHOP, MCP, CHVP / α-interferons), arī parādīja būtiskus uzlabojumus atbildes reakcijas rādītājos, no laika atkarīgos parametros un kopējo dzīvildzi. Visu četru pētījumu svarīgākie rezultāti ir apkopoti 4. tabulā.
4. tabula Kopsavilkums par galvenajiem konstatējumiem četros randomizētos III fāzes pētījumos, kuros novērtēts MabThera ieguvums ar dažādām ķīmijterapijas shēmām folikulārajā limfomā.
EFS - izdzīvošana bez notikumiem
TTP - laiks līdz progresēšanai vai nāvei
PFS - izdzīvošana bez progresēšanas
TTF - laiks līdz ārstēšanas neveiksmei
OS procenti - izdzīvošanas rādītāji analīzes laikā
Uzturošā terapija
Iepriekš neārstēta folikulāra limfoma
Perspektīvā, atklātā starptautiskā daudzcentru III fāzes pētījumā 1193 pacienti ar iepriekš neārstētu progresējošu folikulāru limfomu saņēma indukcijas terapiju ar R-CHOP (n = 881), R-CVP (n = 268) vai R-FCM (n = 44), pamatojoties uz izmeklētāja izvēli. Uz indukcijas terapiju kopumā reaģēja 1078 pacienti, no kuriem 1018 tika randomizēti MabThera uzturēšanai (n = 505) vai novērošanai (n = 513). Abas ārstēšanas grupas bija labi līdzsvarotas attiecībā uz sākotnējām īpašībām un slimības stāvokli. Uzturošā terapija ar MabThera sastāvēja no vienas MabThera infūzijas, ievadot 375 mg / m2 ķermeņa virsmas laukuma devā ik pēc 2 mēnešiem līdz slimības progresēšanai vai līdz 2 gadiem.
Pēc vidējā novērošanas laika, kas bija 25 mēneši pēc randomizācijas, uzturošā terapija ar MabThera radīja klīniski nozīmīgu un statistiski nozīmīgu uzlabojumu pētnieka novērtētajā primārajā beigu bez slimības progresēšanas (PFS) parametrā, salīdzinot ar novērošanu pacientiem ar iepriekš neārstētu folikulāro limfomu. (5. tabula).
Ievērojams ieguvums no MabThera uzturošās terapijas tika novērots arī attiecībā uz dzīvildzi bez notikumiem (EFS), laiku līdz nākamajai anti-limfomas terapijai (TNLT), laiku līdz nākamajai ķīmijterapijai (TNCT) un kopējo atbildes reakcijas rādītāju (ORR) (5. tabula). . Primārās analīzes rezultāti tika apstiprināti ar ilgāku novērošanu (vidējais novērošanas laiks: 48 mēneši un 73 mēneši), un atjauninātie rezultāti tika pievienoti 5. tabulai, lai ilustrētu salīdzinājumu starp 25., 48. un 73. mēnešus.
5. tabula Uzturēšanas fāze: MabThera vs. novērojums pēc 73 mēnešu vidējā novērošanas laika (salīdzinot ar primārās analīzes rezultātiem, kas balstīti uz 25 mēnešu vidējo novērošanas laiku, un atjaunināto analīzi, pamatojoties uz vidējo novērošanas laiku 48 mēneši)
* Pēc apkopes / novērošanas beigām; # p-vērtības no Chi-square testa.
Galvenās vērtības atbilst vidējam novērošanas laikam 73 mēneši, slīprakstā iekavās norādītās vērtības atbilst 48 mēnešu vidējam novērošanas laikam, un iekavās norādītās vērtības atbilst 25 mēnešu vidējam novērošanas laikam analīze).
PFS: izdzīvošana bez progresēšanas; EFS: izdzīvošana bez notikumiem; OS: kopējā izdzīvošana; TNLT: laiks līdz nākamajai anti-limfomas ārstēšanai; TNCT: laiks līdz nākamajai ķīmijterapijas terapijai; ORR: kopējais reakcijas koeficients: NR: nav sasniedzams brīdī nogriezt klīniskā; VAI: koeficientu attiecība.
Uzturošā terapija ar MabThera nodrošināja pastāvīgu labumu visās pārbaudītajās apakšgrupās: dzimums (vīrietis, sieviete), vecums (= 60 gadi), FLIPI rādītājs (= 3), indukcijas terapija (R-CHOP, R-CVP vai R-FCM) un neatkarīgi atbildes reakcijas uz indukcijas terapiju (CR, CRu vai PR) kvalitāti. Uzturošās terapijas ieguvumu izpētes analīze parādīja mazāk izteiktu efektu gados vecākiem pacientiem (> 70 gadus veciem), tomēr izlases lielums bija mazs.
Recidivējoša / ugunsizturīga folikulāra limfoma
Prospektīvā, atklātā, starptautiskā, daudzcentru, III fāzes pētījumā 465 pacienti ar recidivējošu / rezistentu folikulāro limfomu tika randomizēti pirmajā fāzē, lai uzsāktu terapiju ar CHOP (ciklofosfamīds, doksorubicīns, vinkristīns un prednizolons; n = 231) o MabThera plus CHOP (R-CHOP, n = 234). Abas ārstēšanas grupas bija labi līdzsvarotas attiecībā uz sākotnējām īpašībām un slimības stāvokli. Pavisam 334 pacienti, kuri pēc indukcijas terapijas sasniedza pilnīgu vai daļēju remisiju, tika randomizēti uz otro MabThera uzturošās terapijas fāzi (n = 167) vai novērošanu (n = 167). Uzturošā terapija ar MabThera sastāvēja no vienas MabThera infūzijas pa 375 mg / m2 ķermeņa virsmas laukuma, ko ievadīja ik pēc 3 mēnešiem līdz slimības progresēšanai vai līdz diviem gadiem.
Galīgajā efektivitātes analīzē tika iekļauti visi pacienti, kuri tika randomizēti abās pētījuma daļās. Pēc 31 mēneša novērošanas laika pacientiem, kuri tika randomizēti indukcijas fāzē, R-CHOP būtiski uzlaboja pacientu ar limfomu prognozi. CHOP (skat. 6. tabulu).
6. tabula Indukcijas fāze: CHOP efektivitātes rezultātu saraksts, salīdzinot ar R-CHOP (vidējais novērošanas laiks 31 mēnesis).
1) Aprēķins tika aprēķināts ar relatīvo risku.
2) Jaunākā audzēja reakcija, ko novērtējis pētnieks. "Primārais" statistiskais "atbildes" tests bija CR tendences tests pret PR un nereaģēšanu (lpp
Saīsinājumi: NA, nav pieejams; ORR: globālo atbilžu procentuālā daļa; CR: pilnīga atbilde; PR: daļēja reakcija.
Pacientiem, kuri tika randomizēti pētījuma uzturēšanas fāzē, vidējais novērošanas laiks bija 28 mēneši no randomizācijas līdz uzturēšanai. Uzturošā ārstēšana ar MabThera izraisīja klīniski nozīmīgu un statistiski nozīmīgu primārā mērķa parametra PFS (laiks no nejaušināšanas līdz uzturēšanai līdz slimības recidīvam, slimības progresēšanai vai nāvei) uzlabošanos, salīdzinot ar novērošanu atsevišķi (p
7. tabula Uzturēšanas fāze: MabThera efektivitātes rezultātu saraksts attiecībā uz novērošanu (28 mēnešu vidējais novērošanas laiks).
NR: nav sasniegts; a: attiecas tikai uz pacientiem, kuri sasniedz CR.
MabThera uzturošās terapijas ieguvums tika apstiprināts visās analizētajās apakšgrupās neatkarīgi no indukcijas režīma (CHOP vai R-CHOP) vai atbildes reakcijas uz indukcijas ārstēšanu (CR vai PR) (7. tabula). Uzturošā terapija ar MabThera ievērojami pagarināja PFS vidējo rādītāju pacientiem, kuri reaģēja uz indukcijas terapiju ar CHOP (PFS vidējā vērtība 37,5 mēneši pret 11,6 mēnešiem, p
Izkliedēta liela B šūnu ne-Hodžkina limfoma
Randomizētā, atklātā pētījumā kopumā 399 iepriekš neārstēti gados vecāki pacienti (vecumā no 60 līdz 80 gadiem) ar difūzu lielo B šūnu limfomu saņēma standarta CHOP ķīmijterapijas kursus (ciklofosfamīds 750 mg / m2, doksorubicīns 50 mg / m2, vinkristīns 1,4 mg / m2 līdz maksimāli 2 mg, ievadot 1. dienā, un prednizolons 40 mg / m2 / dienā, ievadot 1.-5. dienā) ik pēc 3 nedēļām astoņus ciklus, vai MabThera 375 mg / m2 kopā ar CHOP (R -CHOP).
MabThera tika ievadīts ārstēšanas cikla pirmajā dienā.
Efektivitātes datu galīgajā analīzē tika iekļauti visi randomizētie pacienti (197 CHOP, 202 R-CHOP), un vidējais novērošanas ilgums bija aptuveni 31 mēnesis. Abas ārstēšanas grupas bija labi līdzsvarotas attiecībā uz slimības īpašībām un stāvokli sākotnējā stāvoklī. Galīgā analīze apstiprināja, ka ārstēšana ar R-CHOP bija saistīta ar klīniski nozīmīgu un statistiski nozīmīgu dzīves ilguma uzlabošanos bez notikumiem (primārais efektivitātes parametrs; notikumi bija nāve, recidīvs vai limfomas progresēšana vai pāreja uz jaunu anti- limfomas ārstēšana) (p = 0,0001). Kaplana-Meiera aprēķinātais vidējais ilgums bez notikumiem bija 35 mēneši R-CHOP grupā, salīdzinot ar 13 mēnešiem CHOP grupā, kas nozīmē riska samazinājumu par 41%. Pēc 24 mēnešiem kopējais dzīvildzes novērtējums bija 68,2% R-CHOP grupā, salīdzinot ar 57,4% CHOP grupā. Turpmākā kopējā izdzīvošanas ilguma analīze, kas tika veikta vidējā novērošanas ilgumā 60 mēnešus, apstiprināja R-CHOP terapijas ieguvumu salīdzinājumā ar CHOP (p = 0,0071), kas ir par 32% mazāks risks.
Visu sekundāro parametru analīze (atbildes reakcijas ātrums, dzīvildze bez slimības progresēšanas, dzīvildze bez slimībām, atbildes reakcijas ilgums) pārbaudīja R-CHOP terapijas efektivitāti salīdzinājumā ar CHOP. Pilnīga atbildes reakcija pēc 8 cikliem bija 76,2% R-CHOP grupā un 62,4% CHOP grupā (p = 0,0028). Slimības progresēšanas risks tika samazināts par 46%, bet recidīva risks - par 51%.
Visās pacientu apakšgrupās (dzimums, vecums, atbilstoši vecumam pielāgota IPI, Ann Arbor stadija, ECOG, β2-mikroglobulīns, LDH, albumīns, B simptomi, lielgabarīta slimība, ekstranodālas vietas, kaulu smadzeņu iesaistīšanās), riska attiecība bez notikumiem un kopējā dzīvildze (RCHOP salīdzinājumā ar CHOP) bija attiecīgi mazāka par 0,83 un 0,95. R-CHOP bija saistīts ar uzlabotu prognozi gan augsta, gan zema riska pacientiem saskaņā ar vecuma koriģēto IPI.
Klīniskās laboratorijas dati
No 67 pacientiem, kuriem tika veikts cilvēka antivielu pret peli (HAMA) tests, atbildes reakcija netika novērota. No 356 pacientiem, kuriem tika veikts HACA tests, 1,1% (4 pacienti) bija pozitīvi.
Hroniska limfoleikoze
Divos randomizētos atklātos pētījumos kopā 817 pacienti, kuri iepriekš nebija ārstēti ar HLL, un 552 pacienti ar recidivējošu / refraktāru HLL tika randomizēti, lai saņemtu CF ķīmijterapiju (fludarabīns 25 mg / m2, ciklofosfamīds 250 mg / m2, 1. – 3. Diena) 4 nedēļas 6 cikliem vai MabThera kombinācijā ar FC (R-FC). MabThera tika ievadīts devā 375 mg / m2 pirmā cikla laikā, vienu dienu pirms ķīmijterapijas, un devā 500 mg / m2 katra nākamā ārstēšanas cikla 1. dienā. Pacienti tika izslēgti no recidivējoša / ugunsizturīga HLL pētījuma, ja viņi iepriekš bija ārstēti ar monoklonālām antivielām vai bija rezistenti pret fludarabīnu vai jebkuru nukleozīda analogu (definēts kā nespēja sasniegt daļēju remisiju vismaz 6 mēnešus). Kopumā 810 pacienti (403 R-FC, 407 FC) pirmās rindas pētījumā (8.a tabula un 8.b tabula) un 552 pacienti (276 R-FC, 276 FC) recidivējošā / ugunsizturīgā pētījumā (9. tabula), tika analizēta efektivitāte.
Pirmās rindas pētījumā pēc vidējā novērošanas laika 48,1 mēnesis PFS mediāna bija 55 mēneši R-FC grupā un 33 mēneši FC grupā (p
Kopējā dzīvildzes analīze parādīja būtisku ieguvumu no RFC terapijas, salīdzinot ar tikai CF ķīmijterapiju (p = 0,0319, log-rank tests) (8.a tabula). PFS ieguvums tika konsekventi novērots lielākajā daļā pacientu apakšgrupu, kas tika analizētas saskaņā ar sākotnējo slimības risku (īpaši Binet AC stadijas) ) (8.b tabula).
8.a tabula Hroniskas limfoleikozes pirmās līnijas ārstēšana MabThera plus CF efektivitātes rezultātu apraksts. HR vien - 48,1 mēneša vidējais novērošanas laiks.
Atbilžu procentuālā daļa un CR procenti, kas analizēti saskaņā ar chi-square testu. NR: nav sasniegts; n.a.: nē
piemērojami.
*: Attiecas tikai uz pacientiem, kuri iegūst CR, nPR, PR.
**: attiecas tikai uz pacientiem, kuri sasniedz CR.
8.b tabula Hroniskas limfoleikozes pirmās līnijas ārstēšana Bīstamības pakāpes bez slimības progresēšanas riska attiecība atbilstoši Binet stadijai (ITT)-48,1 mēneša vidējais novērošanas laiks
CI: Uzticības intervāls.
Recidīvu / ugunsizturīgā pētījumā vidējā dzīvildze bez slimības progresēšanas (primārais parametrs) bija 30,6 mēneši R-FC grupā un 20,6 mēneši FC grupā (p = 0,0002, log-rank tests).
PFS ieguvums tika novērots gandrīz visās pacientu apakšgrupās, kuras tika analizētas pēc sākotnējā slimības riska. Ziņots par nelielu, bet nebūtisku vispārējās dzīvildzes uzlabošanos R-FC grupā, salīdzinot ar FC grupu.
9. tabula Recidivējošas / refraktāras hroniskas limfoleikozes ārstēšana - MabThera plus HR efektivitātes rezultātu apraksts tikai pret HR (vidējais novērošanas laiks 25,3 mēneši).
Atbilžu procentuālā daļa un CR procenti, kas analizēti saskaņā ar chi-square testu.
*: attiecas tikai uz pacientiem, kuri iegūst CR, nPR, PR; NR = nav sasniegts; n.a. = nav piemērojams.
**: attiecas tikai uz pacientiem, kuri sasniedz CR.
Arī citu atbalstošu pētījumu rezultāti, kuros MabThera tika lietots kombinācijā ar citām ķīmijterapijas shēmām (ieskaitot CHOP, FCM, PC, PCM, bendamustīnu un kladribīnu) iepriekš neārstētu un / vai recidivējošu pacientu ar HLL / refraktāru ārstēšanai, uzrādīja augstu procentuālo daļu. globālās atbildes reakcijas ar ieguvumiem procentos no PFS, lai gan ar nedaudz lielāku toksicitāti (īpaši mielotoksicitāti). Šie pētījumi apstiprina MabThera lietošanu kopā ar jebkuru ķīmijterapiju.
Dati no aptuveni 180 pacientiem, kas iepriekš tika ārstēti ar MabThera, parādīja klīnisko ieguvumu (ieskaitot CR) un atbalsta atkārtotu ārstēšanu ar MabThera.
Pediatriskā populācija
Eiropas Zāļu aģentūra ir atbrīvojusi no pienākuma iesniegt MabThera pētījumu rezultātus visās pediatriskās populācijas apakšgrupās ar folikulāro limfomu un hronisku limfoleikozi. Informāciju par lietošanu bērniem skatīt 4.2.
Klīniskā pieredze reimatoīdā artrīta ārstēšanā
MabThera efektivitāte un drošība reimatoīdā artrīta simptomu un pazīmju mazināšanā pacientiem ar nepietiekamu atbildes reakciju uz TNF inhibitoriem tika pierādīta galvenajā, randomizētā, kontrolētā dubultmaskētā daudzcentru pētījumā (1. pētījums).
1. pētījumā tika novērtēti 517 pacienti ar nepietiekamu atbildes reakciju vai vienas vai vairāku TNF inhibitoru zāļu nepanesamību. Piemērotajiem pacientiem bija "aktīvs reimatoīdais artrīts, kas diagnosticēts saskaņā ar Amerikas Reimatoloģijas koledžas (ACR) kritērijiem". MabThera tika ievadīts 2 intravenozas infūzijas veidā. atdala ar 15 dienu intervālu. Pacienti saņēma 2 x 1000 mg intravenozas MabThera infūzijas vai placebo kombinācijā ar MTX. Visi pacienti vienlaikus saņēma 60 mg prednizolona perorāli 2. – 7. Dienā un 30 mg 8. – 14. Dienā pēc pirmās infūzijas. Primārais mērķa kritērijs bija to pacientu īpatsvars, kuri 24. nedēļā sasniedza ACR20 atbildes reakciju. Pacientiem pēc 24 nedēļām tika novēroti ilgtermiņa mērķi, kas ietvēra radiogrāfisko novērtējumu pēc 56 nedēļām un 104 nedēļām. Šajā periodā "81% pacientu no sākotnējās placebo grupas saņēma MabThera laikā no 24. līdz 56. nedēļai, kā daļu no "atklātā" protokola pagarinājuma pētījuma.
Pētījumi ar MabThera pacientiem ar artrīta stadiju agri (pacienti, kuri iepriekš nebija ārstēti ar metotreksātu, un pacienti ar nepietiekamu atbildes reakciju uz metotreksātu, bet vēl nebija ārstēti ar TNF-alfa inhibitoriem) sasniedza savus primāros mērķa kritērijus. MabThera nav indicēts šiem pacientiem, jo drošības dati par ilgstošu ārstēšanu ar MabThera ir nepietiekami, jo īpaši attiecībā uz vēža vai PML attīstības risku.
Slimības aktivitātes rezultāti
MabThera kombinācijā ar metotreksātu ievērojami palielināja to pacientu īpatsvaru, kuriem ACR atbildes reakcija uzlabojās vismaz par 20%, salīdzinot ar pacientiem, kuri tika ārstēti tikai ar metotreksātu (10. tabula). Visos galvenajos pētījumos ieguvums no ārstēšanas bija līdzīgs pacientiem neatkarīgi no vecuma, dzimuma, ķermeņa virsmas laukuma, rases, iepriekšējo ārstēšanas gadījumu skaita vai slimības stāvokļa.
Klīniski un statistiski nozīmīgi uzlabojumi tika novēroti arī visās atsevišķās ACR reakcijas sastāvdaļās (sāpīgu un pietūkušu locītavu skaits, kopējais pacientu un ārstu novērtējums, invaliditātes indekss (HAQ), sāpju novērtējums un C reaktīvais proteīns (mg / dl)).
10. tabula Klīniskās atbildes reakcijas rezultāti 1. pētījuma primārajā parametrā (ITT populācija).
† Rezultāts pēc 24 nedēļām.
Būtiska atšķirība no placebo + MTX al laika punkts primārais: *** p ≤ 0,0001.
Pacientiem, kuri tika ārstēti ar MabThera kombinācijā ar metotreksātu, bija ievērojami lielāks DAS28 samazinājums (Slimības aktivitātes rādītājs), salīdzinot ar pacientiem, kuri tika ārstēti tikai ar metotreksātu (9. tabula). Tāpat visos pētījumos EULAR atbilde (Eiropas līga pret reimatismu) labi vai vidēji smagi tika sasniegts ievērojami vairāk pacientu, kuri tika ārstēti ar MabThera un metotreksātu nekā pacienti, kuri tika ārstēti tikai ar metotreksātu (10. tabula).
Radioloģiskā reakcija
Strukturālie locītavu bojājumi tika noteikti radioloģiski un izteikti kā izmaiņas modificētajā kopējā asā rādītājā (mTSS) un tā sastāvdaļās, erozijas rādītājā un locītavu spraugas sašaurināšanās rādītājā.
1. pētījumā, kas tika veikts pacientiem ar nepietiekamu atbildes reakciju vai nepanesību pret terapiju ar vienu vai vairākiem TNF antagonistiem, kuri saņēma MabThera kombinācijā ar metotreksātu, pacientiem 56. nedēļā radiogrāfiskā progresija bija ievērojami mazāka nekā tiem, kuri sākotnēji bija saņēmuši tikai metotreksātu. 81% pacientu, kuri sākotnēji tika ārstēti tikai ar metotreksātu, saņēma MabThera kā glābšanas terapiju laikā no 16. līdz 24. nedēļai vai kā pētījuma pagarinājumu pirms 56. nedēļas. Turklāt lielāka daļa pacientu, kuri saņēma "sākotnējo ārstēšanu ar MabThera" / MTX neuzrādīja erozīvu bojājumu progresēšanu 56 nedēļu laikā (11. tabula).
11. tabula Radioloģiskie rezultāti pēc 1 gada (mITT populācija)
150 pacienti, kuri sākotnēji tika randomizēti 1. pētījumā placebo + MTX, saņēma vismaz vienu RTX + MTX kursu
gadā.
* lpp
Ilgstoši tika novērota arī locītavu bojājumu progresēšanas ātruma kavēšana. 2 gadu radiogrāfiskā analīze 1. pētījumā parādīja, ka pacientiem, kuri saņēma MabThera kombinācijā ar metotreksātu, ievērojami samazinājās strukturālo locītavu bojājumu progresēšana, salīdzinot ar tiem, kuri lietoja tikai metotreksātu un ievērojami lielāks pacientu īpatsvars bez locītavu bojājuma progresēšanas ilgāk par 2 gadiem.
Fiziskās funkcijas un dzīves kvalitātes rezultāti
Pacientiem, kuri tika ārstēti ar MabThera, tika novērots ievērojams invaliditātes indeksa (HAQ-DI) un astēnijas (FACIT-nogurums) samazinājums, salīdzinot ar pacientiem, kuri tika ārstēti tikai ar metotreksātu. Ar MabThera ārstēto pacientu īpatsvars, kuriem bija klīniski nozīmīga minimālā atšķirība (MCID) HAQ-DI (definēts kā individuālā kopējā rādītāja samazinājums> 0,22), bija arī lielāks nekā pacientiem, kuri saņēma tikai metotreksātu. (12. tabula) .
Ir pierādīts būtisks veselības uzlabojums dzīves kvalitātes ziņā, ievērojami uzlabojoties gan SF-36 fiziskās veselības rādītājam (PHS), gan garīgās veselības rādītājam (MHS). Turklāt ievērojami lielāks pacientu īpatsvars sasniedza MCID šiem rādītājiem (12. tabula).
12. tabula Fiziskās funkcijas un dzīves kvalitātes rezultāti 24. nedēļā 1. pētījumā.
† Rezultāti 24. nedēļā.
Būtiska atšķirība no placebo uz laika punkts primārais: * lpp
MCID HAQ-DI ≥0,22, MCID SF-36 PHS> 5,42, MCID SF-36 MHS> 6,33.
Efektivitāte seropozitīviem pacientiem ar autoantivielām (RF un / vai CCP)
Reimatoīdā faktora (RF) un / vai ciklisko peptīdu citrullināta (anti-CCP) seropozitīvi pacienti, kuri tika ārstēti ar MabThera kombinācijā ar metotreksātu, uzrādīja labāku atbildes reakciju nekā pacienti, kuriem bija negatīva reakcija uz abiem.
Efektivitātes rezultāti pacientiem, kuri tika ārstēti ar MabThera, tika analizēti, pamatojoties uz autoantivielu stāvokli pirms ārstēšanas uzsākšanas. 24. nedēļā pacientiem, kuriem sākotnēji bija seropozitīvi pret RF un / vai anti-CCP, bija ievērojami lielāks ACR20 un 50 atbildes reakciju sasniegšanas līmenis nekā seronegatīviem pacientiem (p = 0,0312 un p = 0,0096) (13. tabula). Šie rezultāti tika atkārtoti 48. nedēļā, kur autoantivielu seropozitivitāte ievērojami palielināja ACR70 sasniegšanas varbūtību. 48. nedēļā seropozitīvi pacienti ir 2-3 reizes biežāk sasnieguši ACR atbildes reakciju nekā seronegatīvi pacienti. Seropozitīvajiem bija arī ievērojami lielāks DAS28 samazinājums -ESR nekā seronegatīvi pacienti.
13. tabula. Efektivitātes kopsavilkums, pamatojoties uz autoantivielu stāvokli sākotnējā stāvoklī.
Ievērojami līmeņi tika definēti kā * lpp
Ilgstoša efektivitāte ar atkārtotiem terapijas kursiem
Ārstēšana ar MabThera kombinācijā ar metotreksātu vairāku ciklu laikā ievērojami uzlaboja reimatoīdā artrīta klīniskās pazīmes un simptomus, uz ko liecina ACR, DAS28-VES un EULAR atbildes reakcija, kas bija acīmredzama visās pētītajās populācijās. Tie tika novēroti. Būtiski uzlabojumi fizisko funkciju, kā norādīts HAQ-DI rādītājā, un to pacientu procentuālo daļu, kuri sasniedza MCID HAQ-DI.
Klīniskās laboratorijas rezultāti
Klīniskajos pētījumos kopumā 392 no 3095 (12,7%) pacientiem ar reimatoīdo artrītu HACA bija pozitīvs pēc ārstēšanas ar MabThera. Lielākajai daļai pacientu HACA sākšanās nebija saistīta ar klīnisku pasliktināšanos vai paaugstinātu reakciju risku uz sekojošām infūzijām. HACA klātbūtne var būt saistīta ar infūzijas vai alerģisku reakciju pasliktināšanos pēc nākamo kursu otrās infūzijas.
Pediatriskā populācija
Eiropas Zāļu aģentūra ir atcēlusi pienākumu iesniegt MabThera pētījumu rezultātus visās pediatriskās populācijas apakšgrupās ar autoimūnu artrītu. Informāciju par lietošanu bērniem skatīt 4.2.
Klīniskā pieredze granulomatozes ar poliangiītu (Vegenera) un mikroskopiskā poliangiīta ārstēšanā Kopā tika iekļauti 197 pacienti vecumā no 15 gadiem un vecāki ar aktīvu un smagu poliangiītu ar poliangiītu (75%) un mikroskopisku poliangiītu (24%). randomizēts, dubultmaskēts, aktīvs salīdzinājuma pētījums par mazvērtību.
Pacienti tika randomizēti proporcijā 1: 1, lai saņemtu vai nu perorālu ciklofosfamīdu (2 mg / kg / dienā) 3-6 mēnešus, vai MabThera (375 mg / m2) vienu reizi nedēļā 4 nedēļas. Visi pacienti ciklofosfamīda grupā novērošanas laikā saņēma azatioprīna uzturošo terapiju. Pacienti abās rokās saņēma 1000 mg intravenozas bolus metilprednizolona (vai citas līdzvērtīgas glikokortikoīda devas) dienā 1 līdz 3 dienas, kam sekoja perorāls prednizons (1 mg / kg / dienā, nepārsniedzot 80 mg / dienā). Prednizona samazināšana tika pabeigta 6 mēnešu laikā pēc pētījuma terapijas uzsākšanas. Primārais mērķa kritērijs bija pilnīgas remisijas sasniegšana 6 mēnešu laikā, kas definēta kā Birmingemas vaskulīta aktivitāte par Vegenera granulomatozi (BVAS / WG) 0 un glikokortikoīdu terapijas neesamību. Noklusējuma nenovēršamības robeža atšķirībai starp ārstēšanu bija 20%. Pētījums parādīja, ka MabThera nav zemāka par ciklofosfamīdu pilnīgai remisijai (CR) 6 mēnešu laikā (14. tabula). Efektivitāte tika novērota gan nesen diagnosticētiem pacientiem, gan pacientiem ar recidivējošu slimību (15. tabula).
14. tabula To pacientu procentuālā daļa, kuri sasniedza pilnīgu remisiju 6 mēnešu laikā (populācija, kas paredzēta ārstēšanai *).
15. tabula Pilnīga remisija pēc 6 mēnešiem pēc slimības statusa.
Sliktākajā gadījumā attiecinājums tiek piemērots pacientiem, kuriem trūkst datu.
Pilnīga remisija pēc 12 un 18 mēnešiem
MabThera grupā 48% pacientu sasniedza CR 12 mēnešu laikā un 39% pacientu CR sasniedza 18 mēnešus. Pacientiem, kuri tika ārstēti ar ciklofosfamīdu (kam sekoja azatioprīns, lai saglabātu pilnīgu remisiju), 39% pacientu sasniedza CR pēc 12 mēnešiem un 33% pacientu sasniedza CR pēc 18 mēnešiem. No 12. līdz 18. mēnesim MabThera grupā tika novēroti 8 recidīvi, salīdzinot ar 4 ciklofosfamīda grupā.
Atkārtota ārstēšana ar MabThera
Pamatojoties uz pētnieka spriedumu, 15 pacienti saņēma otru MabThera terapijas kursu slimības aktivitātes recidīva ārstēšanai, kas notika 6 līdz 18 mēnešus pēc pirmā MabThera kursa. Ierobežotie pašreizējā pētījuma dati izslēdz jebkādus secinājumus par turpmākie MabThera kursi pacientiem ar granulomatozi ar poliangiītu un mikroskopisku poliangiītu.
Nepārtraukta imūnsupresīvā terapija var būt īpaši piemērota pacientiem, kuriem ir recidīva risks (piemēram, anamnēzē bijuši recidīvi un granulomatoze ar poliangiītu, vai pacienti ar B-šūnu atjaunošanos papildus PR3-ANCA novērošanas laikā). Kad MabThera remisija ir sasniegta, var apsvērt iespēju turpināt imūnsupresīvu terapiju, lai novērstu recidīvu. MabThera efektivitāte un drošība uzturošā terapijā nav noteikta.
Laboratoriskie testi
Kopumā 23/99 (23%) pacientu, kas tika ārstēti ar MabThera, 18 mēnešu laikā uzrādīja pozitīvu HACA. Neviens no 99 pacientiem, kuri tika ārstēti ar MabThera, skrīninga laikā nebija HACA pozitīvs. HACA attīstības klīniskā nozīme pacientiem, kas ārstēti ar MabThera, nav skaidra.
05.2 "Farmakokinētiskās īpašības
Ne-Hodžkina limfoma
Pamatojoties uz "populācijas farmakokinētikas analīzi 298 NHL pacientiem, kuri saņēma" vienu vai vairākas MabThera infūzijas kā vienu līdzekli vai kombinācijā ar CHOP terapiju (izmantotās MabThera devas no 100 līdz 500 mg / m2), tipiski populācijas aprēķini nespecifiskais klīrenss (CL1), specifiskais klīrenss (CL2) ar iespējamo B šūnu vai audzēja masas ieguldījumu un centrālā nodalījuma izkliedes tilpums (V1) bija attiecīgi 0,14 l / dienā, 0,59 l / dienā un 2,7 l. Vidējais paredzamais MabThera terminālais eliminācijas pusperiods bija 22 dienas (diapazons: 6,1-52 dienas). Sākotnējais CD19 pozitīvo šūnu skaits un izmērāmu audzēju bojājumu diametrs daļēji veicināja MabThera CL2 mainīgumu, kā redzams no 161 datiem pacientiem, kuri intravenozas infūzijas veidā saņēma 4 nedēļas devas 375 mg / m2. Pacientiem ar lielāku CD19 pozitīvu šūnu skaitu vai lielākiem audzēja bojājumiem bija augstāks CL2. Tomēr pēc CD19 korekcijas palika liela individuālo mainīguma sastāvdaļa. -pozitīvs šūnu skaits un audzēja bojājuma diametrs. V1 mainījās atkarībā no ķermeņa virsmas laukuma (Ķermeņa virsmas laukums, BSA) un CHOP terapija. Šī V1 mainība (27,1% un 19,0%), ko noteica attiecīgi BSA diapazons (1,53 līdz 2,32 m2) un vienlaicīga CHOP terapija, bija salīdzinoši neliela. Vecums, dzimums un sniegums PVO statuss neietekmēja MabThera farmakokinētiku.Šī analīze liecina, ka, visticamāk, MabThera devas pielāgošana jebkuram no novērtētajiem kovariātiem būtiski nesamazinās tā farmakokinētisko mainīgumu.
MabThera, ievadot intravenozas infūzijas veidā 375 mg / m2 devā ar nedēļas intervālu 4 devās 203 NHL pacientiem, kuri iepriekš nebija saņēmuši MabThera, pēc ceturtās infūzijas vidējais Cmax bija 486 mcg / ml (diapazons: 77,5 - 996, 6 mcg / ml). Rituksimabu varēja noteikt pacienta serumā 3 - 6 mēnešus pēc pēdējās ārstēšanas pabeigšanas.
Pēc MabThera 375 mg / m2 devas ievadīšanas i.v. ar nedēļas intervālu 8 devām 37 NHL pacientiem vidējais C palielinājās ar katru nākamo infūziju, sākot no vidējā 243 mcg / ml (diapazons: 16 - 582 mcg / ml) pēc pirmās infūzijas līdz 550 mcg / ml (diapazons) : 171 - 1177 mcg / ml) pēc astotās infūzijas.
MabThera farmakokinētiskais profils, lietojot 6 infūzijas pa 375 mg / m2 kombinācijā ar 6 CHOP ķīmijterapijas cikliem, bija līdzīgs tam, kāds tika novērots, lietojot tikai MabThera.
Hroniska limfoleikoze
MabThera tika ievadīts intravenozas infūzijas veidā, pirmā cikla devu 375 mg / m2 palielinot līdz 500 mg / m2 katrā nākamajā ciklā, 5 devām kombinācijā ar fludarabīnu un ciklofosfamīdu pacientiem ar HLL. Vidējais Cmax (N = 15) pēc piektās 500 mg / m2 infūzijas bija 408 mcg / ml (diapazons 97–764 mcg / ml), un vidējais terminālais pusperiods bija 32 dienas (diapazons 14–62 dienas).
Reimatoīdais artrīts
Pēc divām MabThera 1000 mg devas intravenozām infūzijām ar divu nedēļu starplaiku vidējais terminālais eliminācijas pusperiods bija 20,8 dienas (diapazons no 8,58 līdz 35,9 dienām), vidējais sistēmiskais klīrenss bija 0,23 l dienā (diapazons no 0,091 līdz 0,67 l / un vidējais izkliedes tilpums līdzsvara stāvoklī bija 4,6 l (diapazons no 1,7 līdz 7,51 l). To pašu datu populācija sniedza līdzīgas vidējās sistēmiskā klīrensa un eliminācijas pusperioda vērtības-0,26 l dienā un 20,4 dienas, attiecīgi. Populācijas farmakokinētikas analīzes atklāja, ka BSA un dzimums bija nozīmīgākie kovariāti, kas izskaidro farmakokinētisko parametru individuālās atšķirības. Pēc BSA pielāgošanas vīriešiem bija lielāks izkliedes tilpums un ātrāks klīrenss nekā sievietēm. Ar dzimumu saistītās farmakokinētiskās atšķirības netika uzskatītas par klīniski nozīmīgām, un devas pielāgošana nebija nepieciešama. Nav pieejami farmakokinētikas dati par pacientiem ar nieru vai aknu mazspēju.
Rituksimaba farmakokinētika tika novērtēta pēc divām intravenozām (i.v.) devām 500 mg un 1000 mg 1. un 15. dienā četros pētījumos. Visos šajos pētījumos rituksimaba farmakokinētika bija proporcionāla devai ierobežotā pētāmā devu diapazonā. Vidējais rituksimaba Cmax līmenis serumā pēc pirmās infūzijas bija no 157 līdz 171 mcg / ml 2 x 500 mg devām un no 298 līdz 298 341 mcg / ml 2 x 1000 mg devai. Pēc otrās infūzijas vidējā Cmax vērtība bija no 183 līdz 198 mcg / ml 2 µ 500 mg devai un no 355 līdz 404 mcg / ml 2 devai ir 1000 mg. Terminālā eliminācijas vidējais pusperiods bija no 15 līdz 16 dienām, lietojot 2 x 500 mg devu, un no 17 līdz 21 dienai, lietojot 2 devu, ir 1000 mg. Cmax bija no 16 līdz 19%, augstāks pēc otrās infūzijas salīdzinot ar pirmo infūziju abās devās.
Rituksimaba farmakokinētika tika novērtēta pēc divām iv. 500 mg un 1000 mg pēc pārstrādes otrajā ciklā. Rituksimaba vidējais seruma Cmax pēc pirmās infūzijas bija no 170 līdz 175 mcg / ml 2 x 500 mg devai un no 317 līdz 370 mcg / ml 2 x 1000 mg devai. Pēc otrās infūzijas vidējā Cmax vērtība bija 207 mcg / ml 2 x 500 mg devai un no 377 līdz 386 mcg / ml 2 x 1000 mg devai. Vidējais terminālais eliminācijas pusperiods pēc otrās infūzijas pēc otrā cikla bija 19 dienas 2 x 500 mg devai un 21 līdz 22 dienas 2 x 1000 mg devai. Rituksimaba farmakokinētiskie parametri abos ārstēšanas kursos bija salīdzināmi.
Farmakokinētiskie parametri pacientu grupā ar nepietiekamu reakciju uz TNF antivielām, kuri tika pakļauti vienādai dozēšanas shēmai (2 x 1000 mg iv, ar 2 nedēļu starplaiku), bija līdzīgi ar vidējo maksimālo koncentrāciju serumā 369 mcg / ml un "pusi" life "vidējais terminālis - 19,2 dienas.
Granulomatoze ar poliangiītu un mikroskopisku poliangītu 9 līdz 49 dienas). Rituksimaba vidējais klīrenss un izkliedes tilpums bija attiecīgi 0,313 l dienā (diapazons no 0,116 līdz 0,726 l dienā) un 4,50 l (diapazons no 2,25 līdz 7,39 l). Šiem pacientiem rituksimaba farmakokinētiskie parametri šķiet līdzīgi tiem, kas novēroti pacientiem ar reimatoīdo artrītu.
05.3 Preklīniskie drošības dati
Rituksimabs bija ļoti specifisks CD20 antigēnam uz B šūnām cynomolgus tie neatklāja nekādas sekas, izņemot paredzamo B šūnu izsīkumu perifērās asinīs un limfmezglu audos.
Tika veikti evolūcijas toksicitātes pētījumi ar pērtiķiem cynomolgus ar devām līdz 100 mg / kg (ārstēšana grūtniecības 20. – 50. dienā) un ir pierādījuši, ka nav pierādījumu par rituksimaba izraisītu toksisku ietekmi uz augli. farmakoloģiju, kas tika saglabāta līdz pēc dzemdībām un bija saistīta ar IgG līmeņa samazināšanos skartajiem jaundzimušajiem dzīvniekiem.B šūnu skaits šiem dzīvniekiem normalizējās 6 mēnešu laikā pēc dzimšanas un neietekmēja imunizācijas reakcijas.
Standarta testi mutagēnuma noteikšanai nav veikti, jo šie testi nav saistīti ar šo molekulu. Ilgtermiņa pētījumi ar dzīvniekiem nav veikti, lai noteiktu rituksimaba kancerogēno potenciālu.
Nav veikti īpaši pētījumi, lai noteiktu rituksimaba ietekmi uz auglību. Parasti pērtiķu toksicitātes pētījumoscynomolgus netika novērota kaitīga ietekme uz vīriešu vai sieviešu reproduktīvajiem orgāniem.
06.0 FARMACEITISKĀ INFORMĀCIJA
06.1 Palīgvielas
Nātrija citrāts
Polisorbāts 80
Nātrija hlorīds
Nātrija hidroksīds
Sālsskābe
Ūdens injekcijām
06.2 Nesaderība
Netika novērota nesaderība starp MabThera un polivinilhlorīda vai polietilēna maisiņiem, vai infūzijas iekārtām.
06.3 Derīguma termiņš
30 mēneši
Infūzijai sagatavotais MabThera šķīdums ir fiziski un ķīmiski stabils 24 stundas temperatūrā no 2 ° C līdz 8 ° C un pēc tam 12 stundas istabas temperatūrā.
No mikrobioloģiskā viedokļa sagatavotais infūziju šķīdums jāizlieto nekavējoties. Ja tas netiek lietots nekavējoties, uzglabāšanas laiks un apstākļi pirms lietošanas ir lietotāja atbildība un parasti to nedrīkst pārsniegt. 24 stundas temperatūrā temperatūrā no 2 ° C līdz 8 ° C, ja vien atšķaidīšana nav notikusi kontrolētos un apstiprinātos aseptiskos apstākļos.
06.4 Īpaši uzglabāšanas nosacījumi
Uzglabāt ledusskapī (2 ° C - 8 ° C). Uzglabāt trauku ārējā iepakojumā, lai pasargātu no gaismas.
Uzglabāšanas apstākļus pēc zāļu atšķaidīšanas skatīt apakšpunktā 6.3.
06.5 Tiešā iepakojuma veids un iepakojuma saturs
Skaidri I tipa stikla flakoni ar butilgumijas aizbāzni, kas satur 100 mg rituksimaba 10 ml. Iepakojumā 2 flakoni.
06.6 Norādījumi lietošanai un lietošanai
MabThera tiek piegādāts sterilos, konservantus nesaturošos, nepirogēnos, vienreizējas lietošanas flakonos.
Sterilos apstākļos aspirējiet vajadzīgo MabThera daudzumu un atšķaidiet līdz aprēķinātai rituksimaba koncentrācijai 1–4 mg / ml infūzijas maisiņā, kas satur sterilu, nepirogēnu nātrija hlorīda 9 mg / ml (0,9%) šķīdumu injekcijām. ) vai 5% D-glikozes ūdenī. Lai sajauktu šķīdumu, lēnām apgrieziet maisu, lai izvairītos no putu veidošanās. Jārūpējas, lai nodrošinātu sagatavoto šķīdumu sterilitāti. Tā kā zāles nesatur pretmikrobu konservantus vai bakteriostatiskus līdzekļus, jāievēro aseptikas metodes. Pirms ievadīšanas parenterāli ievadāmās zāles vizuāli jāpārbauda, vai nav daļiņu vai krāsas.
Neizlietotās zāles un šo zāļu atkritumi jāiznīcina saskaņā ar vietējiem noteikumiem.
07.0 REĢISTRĀCIJAS APLIECĪBAS ĪPAŠNIEKS
Roche Registration Limited
6 Falcon Way
Šīras parks
Welwyn Garden City
AL7 1TW
Lielbritānija
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS
EU/1/98/067/001
033315019
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS
Reģistrācijas datums: 1998. gada 2. jūnijs
Pēdējās pārreģistrācijas datums: 2008. gada 2. jūnijs
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS
11.0 RADIOZĀLĒM, PILNĪGI DATI PAR IEKŠĒJO RADIĀCIJAS DOSIMETRIJU
12.0 RADIOZĀLĒM, PAPILDU SĪKĀKI NORĀDĪJUMI PAR ĪSTENAJU SAGATAVOŠANU UN KVALITĀTES KONTROLI