Aktīvās sastāvdaļas: Lenalidomīds
Revlimid 2,5 mg cietās kapsulas
Revlimid 5 mg cietās kapsulas
Revlimid 7,5 mg cietās kapsulas
Revlimid 10 mg cietās kapsulas
Revlimid 15 mg cietās kapsulas
Revlimid 20 mg cietās kapsulas
Revlimid 25 mg cietās kapsulas
Kāpēc lieto Revlimid? Kam tas paredzēts?
Revlimid satur aktīvo vielu "lenalidomīdu". Šīs zāles pieder zāļu grupai, kas ietekmē imūnsistēmas darbību.
Revlimid lieto pieaugušajiem, lai:
- Multiplā mieloma
- Mielodisplastiskie sindromi
- Mantijas šūnu limfoma
Multiplā mieloma un Revlimid
Multiplā mieloma ir vēža veids, kas ietekmē noteiktu balto asins šūnu veidu, ko sauc par plazmas šūnām. Šīs šūnas savācas kaulu smadzenēs un nekontrolējami dalās. Tas var sabojāt kaulus un nieres.
Multiplā mieloma parasti ir neārstējama. Tomēr pazīmes un simptomi var ievērojami samazināties vai kādu laiku pazust. Šo rezultātu sauc par "atbildi".
Multiplās mielomas ārstēšanā Revlimid lieto kombinācijā ar citām zālēm.
Revlimid pacientiem ar nesen diagnosticētu multiplo mielomu
Revlimid lieto tikai nesen diagnosticētiem pacientiem, kuriem nevar veikt kaulu smadzeņu transplantāciju.
Ja esat 75 gadus vecs vai vecāks vai Jums ir vidēji smagi vai smagi nieru darbības traucējumi, ārsts pirms ārstēšanas uzsākšanas jūs rūpīgi pārbaudīs.
Jaunizveidotajiem pacientiem ir divu veidu ārstēšana:
- Revlimid kopā ar pretiekaisuma zālēm, ko sauc par deksametazonu.
- Revlimid kopā ar ķīmijterapijas zālēm, ko sauc par melfalānu, un imūnsupresīvām zālēm, ko sauc par prednizonu. Šīs citas zāles Jūs lietosiet ārstēšanas sākumā un pēc tam turpināsiet lietot Revlimid vienu pašu.
Revlimid pacientiem ar multiplo mielomu, kuriem iepriekš ir veikta vismaz viena cita veida ārstēšana
- Revlimid lieto kopā ar pretiekaisuma zālēm, ko sauc par deksametazonu.
Revlimid var apturēt multiplās mielomas pazīmju un simptomu pasliktināšanos. Ir arī pierādīts, ka tas aizkavē multiplās mielomas atjaunošanos pēc ārstēšanas.
Mielodisplastiskie sindromi un Revlimid
Mielodisplastiskie sindromi (MDS) ir daudzu dažādu asins un kaulu smadzeņu slimību kolekcija. Asins šūnas kļūst patoloģiskas un nedarbojas pareizi. Pacientiem var būt dažādas pazīmes un simptomi, tostarp zems sarkano asins šūnu skaits (anēmija), nepieciešamība pēc asins pārliešanas un infekcijas risks.
Revlimid vienu pašu lieto, lai ārstētu pieaugušus pacientus, kuriem diagnosticēts mielodisplastiskais sindroms un kuriem ir visi šie nosacījumi:
- ja Jums nepieciešama regulāra asins pārliešana, lai ārstētu zemu sarkano asins šūnu līmeni ("no pārliešanas atkarīga anēmija")
- ja Jums ir "kaulu smadzeņu šūnu anomālija, ko sauc par" izolētu 5q dzēšanas citoģenētisku anomāliju ". Tas nozīmē, ka jūsu organisms neražo pietiekami daudz veselīgu asins šūnu
- ja citas iepriekš lietotās ārstēšanas metodes nav piemērotas vai nav pietiekami efektīvas.
Revlimid var palielināt veselo sarkano asins šūnu skaitu, ko organisms ražo, samazinot patoloģisko šūnu skaitu:
- Tas var samazināt nepieciešamo asins pārliešanas skaitu. Pārliešana var nebūt nepieciešama.
Mantijas šūnu limfoma un Revlimid
Mantijas šūnu limfoma ir limfātisko audu (imūnsistēmas daļa) vēzis, kas ietekmē balto asins šūnu veidu, ko sauc par B limfocītiem. Mantijas šūnu limfomas gadījumā B limfocīti aug nekontrolēti un uzkrājas limfas audos, kaulu smadzenēs vai asinis.
Revlimid lieto atsevišķi, lai ārstētu pieaugušus pacientus, kuriem diagnosticēta iepriekš neārstēta mantijas šūnu limfoma.
Kā Revlimid darbojas
Revlimid iedarbojas uz ķermeņa imūnsistēmu un tieši uz audzēju vairākos veidos:
- apturot vēža šūnu attīstību
- apturot asinsvadu augšanu, kas ved asinis uz audzēja šūnām
- stimulējot daļu imūnsistēmas uzbrukt vēža šūnām.
Kontrindikācijas Revlimid nedrīkst lietot
Nelietojiet Revlimid
- Ja esat grūtniece vai domājat, ka esat grūtniece, vai plānojat grūtniecību, jo Revlimid var kaitēt nedzimušam bērnam (skatīt 2. sadaļu "Brīdinājumi un piesardzība lietošanā" un "Grūtniecība un zīdīšanas periods").
- Ja pastāv grūtniecības iestāšanās iespēja, ja vien neveicat visus nepieciešamos pasākumus, lai izvairītos no grūtniecības (skatīt 2. sadaļu "Brīdinājumi un piesardzība lietošanā" un "Grūtniecība un zīdīšanas periods"). Ja pastāv grūtniecības iestāšanās iespēja, ārsts atzīmēs un ar katru recepti apstiprinās, ka ir veikti nepieciešamie pasākumi, lai izvairītos no grūtniecības.
- Ja Jums ir alerģija pret lenalidomīdu vai kādu citu (6. punktā minēto) šo zāļu sastāvdaļu. Ja domājat, ka Jums ir alerģija, jautājiet padomu savam ārstam.
Ja kaut kas no iepriekš minētā attiecas uz Jums, nelietojiet Revlimid. Ja rodas šaubas, konsultējieties ar ārstu.
Piesardzība lietošanā Kas jāzina pirms Revlimid lietošanas
Pirms ārstēšanas uzsākšanas pastāstiet ārstam, ja:
- Jums agrāk ir bijušas asins recekļu epizodes, jo ārstēšanas laikā palielinās asins recekļu veidošanās risks vēnās un artērijās
- ir kādas infekcijas pazīmes, piemēram, klepus vai drudzis
- ja Jums ir nieru darbības traucējumi - ārsts var mainīt Revlimid devu
- ja Jums ir bijis sirdslēkme, ir bijis asins receklis vai ja jūs smēķējat, Jums ir augsts asinsspiediens vai augsts holesterīna līmenis
- ir liels audzēja slogs visā ķermenī, tostarp kaulu smadzenēs. Tas var izraisīt slimību, kurā audzēji sadalās un izraisa neparastu ķimikāliju līmeni asinīs, kas var izraisīt nieru mazspēju (šo slimību sauc par audzēju). līzes sindroms ")
- ārstēšanas laikā ar talidomīdu ir bijusi alerģiska reakcija, piemēram, izsitumi, nieze, pietūkums, reibonis vai apgrūtināta elpošana
Ja kaut kas no iepriekš minētā attiecas uz Jums, pastāstiet ārstam pirms ārstēšanas uzsākšanas.
Ja Jums ir mielodisplastiskie sindromi, visticamāk attīstīsies progresējošāka slimība, ko sauc par akūtu mieloleikozi (AML). Turklāt Revlimid loma AML attīstības varbūtībā nav zināma. Ārsts var lūgt jums veikt dažus testus, lai pārbaudītu pazīmes, kas varētu precīzāk paredzēt AML attīstības iespējamību ārstēšanas laikā ar Revlimid.
Analīze un kontrole
Pirms ārstēšanas ar Revlimid un tās laikā Jums tiks veiktas regulāras asins analīzes, jo Revlimid var samazināt to asins šūnu skaitu, kas aizsargā jūs pret infekcijām (baltās asins šūnas) un asins recēšanu (trombocītus). Ārsts lūgs jums veikt asins analīzi:
- pirms ārstēšanas
- katru nedēļu pirmajās 8 ārstēšanas nedēļās (pacientiem ar mantijas šūnu limfomu tas notiks ik pēc 2 nedēļām 3. un 4. ciklā un pēc tam katra cikla sākumā)
- vismaz reizi mēnesī pēc tam.
Ārsts var pārbaudīt jūsu ādas izmaiņas, piemēram, sarkanus plankumus vai izsitumus.
Atkarībā no asins analīžu rezultātiem un vispārējā stāvokļa ārsts var izlemt pielāgot Revlimid devu vai pārtraukt ārstēšanu. Ja esat nesen diagnosticēts pacients, ārsts var arī novērtēt ārstēšanu, pamatojoties uz jūsu vecumu un citiem jau esošiem apstākļiem.
Asins ziedošana
Jūs nedrīkstat ziedot asinis lenalidomīda terapijas laikā un vienu nedēļu pēc ārstēšanas pārtraukšanas.
Bērni un pusaudži
Revlimid nav ieteicams lietot bērniem un pusaudžiem līdz 18 gadu vecumam.
Mijiedarbība Kādas zāles vai pārtikas produkti var mainīt Revlimid iedarbību
Pastāstiet ārstam vai medmāsai par visām zālēm, kuras lietojat, pēdējā laikā esat lietojis vai varētu lietot, ieskaitot zāles, ko var iegādāties bez receptes, un augu izcelsmes zāles. Tas ir tāpēc, ka Revlimid var ietekmēt dažu citu zāļu iedarbību un dažas citas zāles. kā Revlimid darbojas ..
Īpaši pastāstiet ārstam vai medmāsai, ja lietojat kādas no šīm zālēm:
- dažas zāles, ko lieto grūtniecības novēršanai, piemēram, perorālie kontracepcijas līdzekļi, jo tās var vairs nebūt efektīvas
- dažas zāles sirds slimību ārstēšanai, piemēram, digoksīns
- dažas zāles, ko lieto asins šķidrināšanai, piemēram, varfarīns
Brīdinājumi Ir svarīgi zināt, ka:
Grūtniecība, zīdīšanas periods un kontracepcija - informācija sievietēm un vīriešiem
Grūtniecība
Sievietēm, kuras lieto Revlimid
- Jūs nedrīkstat lietot Revlimid, ja esat grūtniece, jo šīs zāles ir kaitīgas nedzimušam bērnam.
- Ārstēšanas laikā ar Revlimid nedrīkst iestāties grūtniecība. Ja pastāv grūtniecības iespēja, jums jāizmanto efektīvas kontracepcijas metodes (skatīt sadaļu "Kontracepcija").
- Ja Revlimid lietošanas laikā Jums iestājas grūtniecība, ārstēšana nekavējoties jāpārtrauc un jāinformē ārsts.
Vīriešiem, kuri lieto Revlimid
- Ja jūsu partnerim iestājas grūtniecība Revlimid lietošanas laikā, nekavējoties informējiet par to ārstu. Tāpat partnerim ieteicams sazināties ar ārstu.
- Turklāt jums jāizmanto efektīvas kontracepcijas metodes (skatīt sadaļu "Kontracepcija").
Barošanas laiks
Revlimid lietošanas laikā nedrīkst barot bērnu ar krūti, jo nav zināms, vai šīs zāles nonāk mātes pienā.
Kontracepcija
Sievietēm, kas lieto Revlimid
Pirms ārstēšanas uzsākšanas jums jājautā ārstam, vai pastāv iespēja palikt stāvoklī, pat ja uzskatāt, ka tas ir maz ticams.
Ja pastāv grūtniecības iestāšanās iespēja
- Jums būs jāveic grūtniecības testi ārsta uzraudzībā (pirms katras ārstēšanas, ik pēc 4 nedēļām ārstēšanas laikā un 4 nedēļas pēc ārstēšanas beigām), izņemot gadījumus, kad ir apstiprināts, ka olvadi ir sagriezti un aizvērti, lai novērstu olas nenokļūst dzemdē (sterilizācija, sasienot caurulītes)
- Jums jāizmanto efektīvas kontracepcijas metodes 4 nedēļas pirms ārstēšanas uzsākšanas, ārstēšanas laikā un līdz 4 nedēļām pēc ārstēšanas pārtraukšanas.Ārsts ieteiks Jums piemērotas kontracepcijas metodes.
Vīriešiem, kuri lieto Revlimid
Revlimid nonāk cilvēka spermā. Ja pastāv iespēja, ka jūsu partneris ir stāvoklī vai iestājas grūtniecība un viņa neizmanto efektīvas kontracepcijas metodes, ārstēšanas laikā un vienu nedēļu pēc ārstēšanas beigām jālieto prezervatīvi, pat ja Jums ir veikta vazektomija.
Transportlīdzekļu vadīšana un mehānismu apkalpošana
Nevadiet transportlīdzekli un neapkalpojiet mehānismus, ja jūtat reiboni, nogurumu, miegainību, reiboni vai redzes miglošanos.
Revlimid satur laktozi
Revlimid satur laktozi. Ja ārsts ir teicis, ka Jums ir “dažu cukuru nepanesamība, pirms Revlimid lietošanas konsultējieties ar ārstu.
Deva, lietošanas veids un laiks Kā lietot Revlimid: Devas
Revlimid jāievada veselības aprūpes speciālistiem, kuriem ir pieredze multiplās mielomas vai mielodisplastisko sindromu un mantijas šūnu limfomas ārstēšanā.
- Lietojot multiplās mielomas ārstēšanai, Revlimid lieto kombinācijā ar citām zālēm (skatīt 1. punktu “Kas ir Revlimid un kādam nolūkam to lieto”).
- Lietojot mielodisplastisko sindromu un mantijas šūnu limfomas ārstēšanai, Revlimid lieto atsevišķi.
Vienmēr lietojiet Revlimid vienu pašu vai Revlimid kombinācijā ar citām zālēm, vienmēr precīzi ievērojot ārsta norādījumus. Ja rodas šaubas, konsultējieties ar ārstu vai farmaceitu.
Ja Jūs lietojat Revlimid kombinācijā ar citām zālēm, lūdzu, skatiet šo zāļu lietošanas instrukcijas, lai iegūtu plašāku informāciju par to lietošanu un iedarbību.
Ārstēšanas cikls
- Revlimid un zāles, kas Jums jālieto kombinācijā ar Revlimid, tiek lietotas dažas dienas 4 nedēļu laikā (28 dienas).
- Katru 28 dienu periodu sauc par "ārstēšanas ciklu".
- Atkarībā no menstruāciju dienas jūs lietosiet vienu vai vairākas zāles. Tomēr dažās dienās jūs nelietojat zāles.
- Kad katrs 28 dienu cikls ir pabeigts, nākamo 28 dienu laikā jāsāk jauns "cikls".
Revlimid deva
Pirms ārstēšanas uzsākšanas ārsts jums pateiks:
- Revlimid devu
- citu zāļu devu, kas jālieto kombinācijā ar Revlimid, ja tas ir parakstīts
- kurās ārstēšanas cikla dienās lietot katru medikamentu.
Ārsts var novērot izmaiņas uz ādas, piemēram, sarkanus plankumus vai izsitumus.
Ārsts var arī izlemt mainīt Revlimid vai citu zāļu devu ārstēšanas laikā, pamatojoties uz asins analīžu rezultātiem un vispārējo stāvokli (skatīt 2. sadaļu "Kas jāzina pirms Revlimid lietošanas").
Kā un kad lietot Revlimid
- Kapsulas jānorij veselas, vēlams, uzdzerot ūdeni.
- Nepārtrauciet, neatveriet un nesakošļājiet kapsulas.
- Kapsulas var lietot kopā ar ēdienu vai bez tā.
- Jums Revlimid jālieto noteiktajās dienās aptuveni vienā un tajā pašā laikā.
Lai izņemtu kapsulu no blistera, nospiediet tikai vienu kapsulas pusi, izspiežot to caur alumīnija foliju. Nespiediet uz kapsulas centra, pretējā gadījumā tā var salūzt.
Ārstēšanas ilgums ar Revlimid
Revlimid lieto ārstēšanas ciklos, kas ilgst 28 dienas (skatīt “Ārstēšanas cikls” iepriekš). Jums jāturpina ārstēšanas kursi, līdz ārsts Jums liks pārtraukt ārstēšanu.
Ja esat aizmirsis lietot Revlimid
Ja esat aizmirsis lietot Revlimid parastajā laikā e
- ir pagājušas mazāk nekā 12 stundas: nekavējoties ieņemiet kapsulu
- ir pagājušas vairāk nekā 12 stundas: nelietojiet aizmirsto kapsulu, bet nākamo lietojiet nākamajā dienā parastajā laikā.
Ja jums ir kādi jautājumi par šo zāļu lietošanu, jautājiet savam ārstam vai farmaceitam.
Pārdozēšana Ko darīt, ja esat lietojis pārāk daudz Revlimid
Ja esat lietojis Revlimid vairāk nekā noteikts, nekavējoties informējiet ārstu.
Blakusparādības Kādas ir Revlimid blakusparādības?
Tāpat kā citas zāles, šīs zāles var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas.
Nopietnas blakusparādības, kas var skart vairāk nekā 1 no 10 cilvēkiem
Revlimid var samazināt balto asins šūnu skaitu, kas cīnās ar infekcijām, un asins šūnas, kas veicina asins recēšanu (trombocīti), kas var izraisīt asiņošanas traucējumus, piem. deguna asiņošana un zilumi. Revlimid var izraisīt arī asins recekļu veidošanos vēnās (trombozi).
Tādēļ jums nekavējoties jāmeklē medicīniskā palīdzība, ja Jums rodas kāda no šīm blakusparādībām:
- drudzis, drebuļi, iekaisis kakls, klepus, čūlas mutē vai jebkādi citi infekcijas simptomi (arī asinsritē (sepse))
- asiņošana vai zilumi, ja nav brūču
- sāpes krūtīs vai kājās
- elpas trūkums.
Ja Jums rodas kāda no iepriekš minētajām blakusparādībām, lūdzu, nekavējoties informējiet par to ārstu.
Citas blakusparādības ir uzskaitītas zemāk
Ir svarīgi atzīmēt, ka nelielam skaitam pacientu var attīstīties cita veida vēzis, un iespējams, ka šis risks var palielināties, ārstējoties ar Revlimid; tādēļ ārstam, izrakstot Revlimid, rūpīgi jāizvērtē ieguvums un risks.
Ļoti bieži sastopamas blakusparādības var rasties vairāk nekā 1 no 10 cilvēkiem:
- Sarkano asins šūnu skaita samazināšanās (anēmija), kas var izraisīt nogurumu un nespēku
- Aizcietējums, caureja, slikta dūša, ādas apsārtums, izsitumi, vemšana, muskuļu krampji, muskuļu sāpes, kaulu sāpes, locītavu sāpes, nogurums, vispārējs pietūkums, ieskaitot roku un kāju pietūkumu
- Drudzis un gripas simptomi, tai skaitā drudzis, muskuļu sāpes, galvassāpes, ausu sāpes un drebuļi
- Nejutīgums, tirpšana vai dedzinoša sajūta uz ādas, sāpes rokās vai kājās, reibonis, trīce, garšas izmaiņas
- Sāpes krūtīs, kas izstaro rokas, kaklu, žokli, muguru vai vēderu, ar svīšanas sajūtu un elpas trūkumu, sliktu dūšu vai vemšanu, kas var būt sirdslēkmes simptomi (miokarda infarkts)
- Apetītes samazināšanās
- Zems kālija līmenis asinīs
- Sāpes kājās (kas var būt trombozes simptoms), sāpes krūtīs vai elpas trūkums (kas var būt asins recekļu simptomi plaušās, ko sauc par plaušu emboliju)
- Jebkura veida infekcijas
- Plaušu un augšējo elpceļu infekcija, elpas trūkums
- Neskaidra redze
- Neskaidra redze (katarakta)
- Nieru problēmas
- Izmaiņas proteīnā asinīs, kas var izraisīt artēriju pietūkumu (vaskulīts)
- Paaugstināts cukura līmenis asinīs (diabēts)
- Galvassāpes
- Sausa āda
- Sāpes vēderā
- Garastāvokļa izmaiņas, miega traucējumi
Biežas blakusparādības var rasties līdz 1 no 10 cilvēkiem:
- Deguna blakusdobumu infekcija
- Asiņošana no smaganām, kuņģa vai zarnām
- Paaugstinātas sāpes, audzēja izmērs, apsārtums ap audzēju
- Asinsspiediena paaugstināšanās vai pazemināšanās, lēna, ātra vai neregulāra sirdsdarbība
- Ādas tumšums
- Izsitumi, ādas plaisāšana, lobīšanās vai lobīšanās
- Nātrene, nieze, pastiprināta svīšana, dehidratācija
- Sāpes mutē ar čūlām, sausa mute, apgrūtināta rīšana
- Vēdersāpes
- Urīna veidošanās daudz vairāk vai mazāk nekā parasti (kas var būt nieru mazspējas simptoms), asinis urīnā
- Elpas trūkums, īpaši guļus stāvoklī (kas var būt sirds mazspējas simptoms)
- Grūtības iegūt erekciju
- Insults, ģībonis
- Muskuļu vājums
- Locītavu pietūkums
- Izmaiņas vairogdziedzera hormonu asinīs, zems kalcija, fosfāta vai magnija līmenis asinīs
- Depresija
- Kurlums
- Nenormāli aknu darbības testi
- Līdzsvara traucējumi, kustību grūtības
- Zvana ausīs (troksnis ausīs)
- Dzelzs pārslodze
- Slāpes
- Apjukums
- Zobu sāpes
- Svara zudums.
Retākas blakusparādības var rasties līdz 1 no 100 cilvēkiem:
- Asiņošana galvaskausa iekšpusē
- Asinsrites problēmas
- Redzes zudums
- Dzimumtieksmes zudums (libido)
- Bagātīga urīna plūsma ar sāpēm un vājumu kaulos, kas varētu būt nieru darbības traucējumu simptomi (Fanconi sindroms)
- Sāpes vēderā, vēdera uzpūšanās vai caureja, kas var būt resnās zarnas iekaisuma simptomi (ko sauc par kolītu vai tiflītu)
- Daudz vairāk vai mazāk urīna veidošanās nekā parasti, kas var būt simptoms kāda veida nieru problēmām (ko sauc par nieru kanāliņu nekrozi)
- Ādas krāsas izmaiņas, jutība pret saules gaismu
- Daži ādas vēža veidi
- Nātrene, izsitumi, acu, mutes vai sejas pietūkums, apgrūtināta elpošana vai nieze, kas var būt alerģiskas reakcijas simptomi.
Retas blakusparādības var rasties līdz 1 no 1000 cilvēkiem:
- Smaga alerģiska reakcija, kas var sākties kā izsitumi vienā vietā, bet izplatīties ar plašu ādas zudumu visā ķermenī (Stīvensa-Džonsona sindroms un / vai toksiska epidermas nekrolīze).
- Audzēja sabrukšanas sindroms - vielmaiņas komplikācijas, kas var rasties audzēja ārstēšanas laikā un dažreiz pat bez ārstēšanas. Šīs komplikācijas izraisa mirstošu vēža šūnu sabrukšanas produkti, un tās var ietvert šādas komplikācijas: izmaiņas hematoloģiskajos parametros; augstas kālija, fosfora un urīnskābes vērtības; un zemas kalcija vērtības, kas līdz ar to noved pie nieru darbības, sirdsdarbības ātruma, krampju un dažreiz nāves izmaiņām.
Biežums nav zināms: biežumu nevar noteikt pēc pieejamiem datiem:
- Pēkšņas vai vieglas, bet pastiprinošas sāpes vēdera augšdaļā un / vai mugurā, kas saglabājas dažas dienas, iespējams, ar sliktu dūšu, vemšanu, drudzi un paātrinātu pulsu.Šie simptomi var rasties aizkuņģa dziedzera iekaisuma dēļ.
- Sēkšana, elpas trūkums vai sauss klepus, kas varētu būt simptomi, ko izraisa plaušu audu iekaisums.
- Dzeltenīga ādas, gļotādu vai acu krāsas maiņa (dzelte), gaiši izkārnījumi, tumšs urīns, ādas nieze, izsitumi, sāpes vai vēdera pietūkums. Tie var būt aknu bojājuma simptomi (aknu slimība).
- Ir novēroti reti muskuļu sabrukšanas gadījumi (sāpes, vājums vai muskuļu pietūkums), kas var izraisīt nieru darbības traucējumus (rabdomiolīzi), daži no tiem, lietojot Revlimid kopā ar statīnu (holesterīna līmeni pazeminošu zāļu veidu).
- Slimība, kas skar ādu un ko izraisa mazo asinsvadu iekaisums, locītavu sāpes un drudzis (leikocitoklastiskais vaskulīts).
- Kuņģa vai zarnu sienas pasliktināšanās, kas var izraisīt ļoti nopietnas infekcijas.Pastāstiet ārstam, ja Jums ir stipras sāpes vēderā, drudzis, slikta dūša, vemšana, asinis izkārnījumos vai izmaiņas zarnu paradumos.
Ziņošana par blakusparādībām
Ja Jums rodas jebkādas blakusparādības, konsultējieties ar ārstu, farmaceitu vai medmāsu. Tas attiecas arī uz iespējamām blakusparādībām, kas nav minētas šajā lietošanas instrukcijā. Jūs varat ziņot par blakusparādībām arī tieši, izmantojot valsts pielikumā sniegto ziņošanas sistēmu. sniedziet vairāk informācijas par šo zāļu drošumu.
Derīguma termiņš un saglabāšana
- Uzglabāt šīs zāles bērniem neredzamā un nepieejamā vietā.
- Nelietot šīs zāles pēc derīguma termiņa beigām, kas norādīts uz blistera un kastītes pēc “Derīgs līdz”. Derīguma termiņš attiecas uz norādītā mēneša pēdējo dienu.
- Šīm zālēm nav nepieciešami īpaši uzglabāšanas apstākļi.
- Nelietojiet šīs zāles, ja pamanāt iepakojumus, kas ir bojāti vai kuriem ir redzamas viltošanas pazīmes.
- Neizmetiet zāles kanalizācijā vai sadzīves atkritumos. Jautājiet farmaceitam, kā izmest zāles, kuras vairs nelietojat. Tas palīdzēs aizsargāt vidi.
Termiņš "> Cita informācija
Ko Revlimid satur
Revlimid 2,5 mg cietās kapsulas:
- Aktīvā viela ir lenalidomīds. Katra kapsula satur 2,5 mg lenalidomīda.
- Citas sastāvdaļas ir:
- kapsulas saturs: bezūdens laktoze, mikrokristāliskā celuloze, kroskarmelozes nātrijs un magnija stearāts
- kapsulas apvalks: želatīns, titāna dioksīds (E171), indigokarmīns (E132) un dzeltenais dzelzs oksīds (E172)
- burtu tinte: šellaks, propilēnglikols, kālija hidroksīds un melnais dzelzs oksīds (E172).
Revlimid 5 mg cietās kapsulas:
- Aktīvā viela ir lenalidomīds. Katra kapsula satur 5 mg lenalidomīda.
- Citas sastāvdaļas ir:
- kapsulas saturs: bezūdens laktoze, mikrokristāliskā celuloze, kroskarmelozes nātrijs un magnija stearāts
- kapsulas apvalks: želatīns un titāna dioksīds (E171)
- burtu tinte: šellaks, propilēnglikols, kālija hidroksīds un melnais dzelzs oksīds (E172).
Revlimid 7,5 mg cietās kapsulas:
- Aktīvā viela ir lenalidomīds. Katra kapsula satur 7,5 mg lenalidomīda.
- Citas sastāvdaļas ir:
- kapsulas saturs: bezūdens laktoze, mikrokristāliskā celuloze, kroskarmelozes nātrijs un magnija stearāts
- kapsulas apvalks: želatīns, titāna dioksīds (E171), dzeltenais dzelzs oksīds (E172)
- burtu tinte: šellaks, propilēnglikols, kālija hidroksīds un melnais dzelzs oksīds (E172).
Revlimid 10 mg cietās kapsulas:
- Aktīvā viela ir lenalidomīds. Katra kapsula satur 10 mg lenalidomīda.
- Citas sastāvdaļas ir:
- kapsulas saturs: bezūdens laktoze, mikrokristāliskā celuloze, kroskarmelozes nātrijs un magnija stearāts
- kapsulu sagatavošana: želatīns, titāna dioksīds (E171), indigokarmīns (E132) un dzeltenais dzelzs oksīds (E172)
- burtu tinte: šellaks, propilēnglikols, kālija hidroksīds un melnais dzelzs oksīds (E172).
Revlimid 15 mg cietās kapsulas:
- Aktīvā viela ir lenalidomīds. Katra kapsula satur 15 mg lenalidomīda.
- Citas sastāvdaļas ir:
- kapsulas saturs: bezūdens laktoze, mikrokristāliskā celuloze, kroskarmelozes nātrijs un magnija stearāts
- kapsulas apvalks: želatīns, titāna dioksīds (E171) un indigokarmīns (E132)
- burtu tinte: šellaks, propilēnglikols, kālija hidroksīds un melnais dzelzs oksīds (E172).
Revlimid 20 mg cietās kapsulas:
- Aktīvā viela ir lenalidomīds. Katra kapsula satur 20 mg lenalidomīda.
- Citas sastāvdaļas ir:
- kapsulas saturs: bezūdens laktoze, mikrokristāliskā celuloze, kroskarmelozes nātrijs un magnija stearāts
- kapsulas apvalks: želatīns, titāna dioksīds (E171), indigokarmīns (E132) un dzeltenais dzelzs oksīds (E172)
- burtu tinte: šellaks, propilēnglikols, kālija hidroksīds un melnais dzelzs oksīds (E172).
Revlimid 25 mg cietās kapsulas:
- Aktīvā viela ir lenalidomīds. Katra kapsula satur 25 mg lenalidomīda.
- Citas sastāvdaļas ir:
- kapsulas saturs: bezūdens laktoze, mikrokristāliskā celuloze, kroskarmelozes nātrijs un magnija stearāts
- kapsulas apvalks: želatīns un titāna dioksīds (E171)
- burtu tinte: šellaks, propilēnglikols, kālija hidroksīds un melnais dzelzs oksīds (E172).
Revlimid ārējais izskats un iepakojums
Revlimid 2,5 mg cietās kapsulas ir zili zaļas / baltas, ar apzīmējumu "REV 2,5 mg".
Kapsulas tiek piegādātas iepakojumos, katrā ir viens vai trīs blisteri. Katrā blisterī ir septiņas kapsulas, kopā 7 vai 21 kapsula iepakojumā.
Revlimid 5 mg cietās kapsulas ir baltas, ar apzīmējumu "REV 5 mg".
Kapsulas tiek piegādātas iepakojumos, katrā ir viens vai trīs blisteri. Katrā blisterī ir septiņas kapsulas, kopā 7 vai 21 kapsula iepakojumā.
Revlimid 7,5 mg cietās kapsulas ir gaiši dzeltenas / baltas, ar apzīmējumu "REV 7,5 mg".
Kapsulas tiek piegādātas iepakojumos, katrā ir trīs blisteri. Katrā blisterī ir septiņas kapsulas, kopā 21 kapsula iepakojumā.
Revlimid 10 mg cietās kapsulas ir zili zaļas / gaiši dzeltenas, ar apzīmējumu "REV 10 mg".
Kapsulas tiek piegādātas iepakojumos, katrā ir trīs blisteri. Katrā blisterī ir septiņas kapsulas, kopā 21 kapsula iepakojumā.
Revlimid 15 mg cietās kapsulas ir gaiši zilas / baltas ar marķējumu "REV 15 mg".
Kapsulas tiek piegādātas iepakojumos, katrā ir trīs blisteri. Katrā blisterī ir septiņas kapsulas, kopā 21 kapsula iepakojumā.
Revlimid 20 mg cietās kapsulas ir zili zaļas / gaiši zilas, ar apzīmējumu "REV 20 mg".
Kapsulas tiek piegādātas iepakojumos, katrā ir trīs blisteri. Katrā blisterī ir septiņas kapsulas, kopā 21 kapsula iepakojumā.
Revlimid 25 mg cietās kapsulas ir baltas, ar apzīmējumu "REV 25 mg".
Kapsulas tiek piegādātas iepakojumos, katrā ir trīs blisteri. Katrā blisterī ir septiņas kapsulas, kopā 21 kapsula iepakojumā.
Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī. Pašlaik pieejamā informācija var nebūt atjaunināta.
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija.
01.0 ZĀĻU NOSAUKUMS -
REVLIMID 10 MG CIETAS KAPSULAS
▼ Zāles, uz kurām attiecas papildu uzraudzība. Tas ļaus ātri identificēt jaunu drošības informāciju. Veselības aprūpes speciālistus lūdz ziņot par jebkādām iespējamām blakusparādībām. Informāciju par to, kā ziņot par blakusparādībām, skatīt 4.8.
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS -
Katra kapsula satur 10 mg lenalidomīda.
Palīgvielas ar zināmu iedarbību:
Katra kapsula satur 294 mg bezūdens laktozes.
Pilnu palīgvielu sarakstu skatīt apakšpunktā 6.1.
03.0 ZĀĻU FORMA -
Cieta kapsula.
Zili zaļas / gaiši dzeltenas kapsulas, izmērs 0,21,7 mm, ar apzīmējumu "REV 10 mg".
04.0 KLĪNISKĀ INFORMĀCIJA -
04.1 Terapeitiskās indikācijas -
Multiplā mieloma
Revlimid ir paredzēts pieaugušu pacientu ārstēšanai ar iepriekš neārstētu multiplo mielomu, kuriem nav piemērota transplantācija (skatīt 4.2. Apakšpunktu).
Revlimid kombinācijā ar deksametazonu ir indicēts pieaugušu pacientu ar multiplo mielomu ārstēšanai, kuri iepriekš saņēmuši vismaz vienu terapiju.
Mielodisplastiskie sindromi
Revlimid ir paredzēts pacientu ārstēšanai, kuriem ir no pārliešanas atkarīga anēmija zema vai vidēja 1 riska pakāpes mielodisplastisko sindromu (MDS) dēļ, kas saistīti ar izolētu 5q dzēšanas citoģenētisku anomāliju, ja citas ārstēšanas iespējas ir nepietiekamas vai nepietiekamas.
Mantijas šūnu limfoma
Revlimid ir paredzēts pieaugušu pacientu ārstēšanai ar recidivējošu vai ugunsizturīgu mantijas šūnu limfomu (skatīt 4.4. Un 5.1. Apakšpunktu).
04.2 Devas un lietošanas veids -
Ārstēšana ar Revlimid jāuzrauga ārstam, kam ir pieredze vēža terapijas lietošanā (skatīt apakšpunktu 4.4, kariotips).
Devas
Nesen diagnosticēta multiplā mieloma
Lenalidomīds kombinācijā ar deksametazonu līdz slimības progresēšanai ne-pacientiem piemērots transplantācijai
Ārstēšanu ar lenalidomīdu nedrīkst sākt, ja absolūtais neitrofilo leikocītu skaits (Absolūti
Neitrofilu skaits, ANC) ir
Ieteicamā deva
Ieteicamā lenalidomīda sākuma deva ir 25 mg iekšķīgi vienu reizi dienā atkārtotu 28 dienu ciklu 1.-21. Ieteicamā deksametazona deva ir 40 mg iekšķīgi vienu reizi dienā atkārtotu 28 dienu ciklu 1., 8., 15. un 22. dienā. Pacienti var turpināt terapiju ar lenalidomīdu un deksametazonu, līdz attīstās slimības progresēšana vai nepanesamība.
Devu var turpināt vai mainīt, pamatojoties uz klīniskajiem un laboratorijas rezultātiem (skatīt apakšpunktu 4.4). Pacientiem, kas vecāki par 75 gadiem, deksametazona sākuma deva ir 20 mg dienā katra 28 dienu ārstēšanas cikla 1., 8., 15. un 22. dienā. Ieteicamā lenalidomīda deva pacientiem ar vidēji smagiem nieru darbības traucējumiem ir 10 mg vienu reizi dienā.
Ieteicamā devas pielāgošana ārstēšanas laikā un pēc ārstēšanas atsākšanas
Kā apkopots zemāk esošajās tabulās, devu pielāgošana ir ieteicama 3. vai 4. pakāpes trombocitopēnijas un neitropēnijas ārstēšanai vai jebkuras citas 3. vai 4. pakāpes toksicitātes ārstēšanai, kas, domājams, ir saistīta ar lenalidomīdu.
• Devas samazināšanas līmeņi
• Trombocitopēnija
a Ja rodas devu ierobežojoša toksicitāte (Devu ierobežojoša toksicitāte, DLT)> Cikla 15. diena, lenalidomīda lietošana tiks pārtraukta vismaz uz atlikušo pašreizējo 28 dienu ciklu.
• Neitropēnija
Neitropēnijas gadījumā ārstam jāapsver augšanas faktoru izmantošana pacientu ārstēšanā.
Ja lenalidomīda deva ir samazināta hematoloģiskas DLT dēļ, pēc ārstējošā ārsta ieskatiem lenalidomīda devu var atkal ievadīt nākamajā augstākajā devā (līdz sākuma devai), ja, turpinot lenalidomīda / deksametazona terapiju, uzlabojās kaulu smadzenes funkcija (DLT trūkums vismaz 2 secīgos ciklos un ANC ≥ 1500 / mcl, ar trombocītu skaitu ≥ 100 000 / mcl, jauna cikla sākumā ar pašreizējo devu).
Lenalidomīds kombinācijā ar melfalānu un prednizonu, kam seko uzturošā monoterapija pacienti, kuri nav piemēroti transplantācijai
Ārstēšanu ar lenalidomīdu nedrīkst uzsākt, ja ir ANC
Ieteicamā deva
Ieteicamā sākumdeva ir lenalidomīds 10 mg dienā perorāli atkārtotu 28 dienu ciklu 1-21 dienās līdz 9 cikliem, melfalāns 0,18 mg / kg perorāli 28 dienu atkārtotu ciklu 1.-4. Dienā, prednizons 2 mg / dienā kg iekšķīgi atkārtotu 28 dienu ciklu 1.-4. Pacienti, kuri pabeidz 9 ciklus vai nepanesības dēļ nevar pabeigt kombinēto terapiju, jāārstē ar lenalidomīda monoterapiju, 10 mg dienā perorāli, atkārtotu ciklu 1.-21. Dienā-28 dienas līdz slimības progresēšanai. Devu var turpināt vai mainīt, pamatojoties uz klīniskajiem un laboratorijas rezultātiem (skatīt apakšpunktu 4.4).
Ieteicamā devas pielāgošana ārstēšanas laikā un pēc ārstēšanas atsākšanas
Kā apkopots zemāk esošajās tabulās, devas pielāgošana ir ieteicama 3. vai 4. pakāpes trombocitopēnijas vai neitropēnijas ārstēšanai vai jebkuras citas 3. vai 4. pakāpes toksicitātes ārstēšanai, kas, domājams, ir saistīta ar lenalidomīdu.
• Devas samazināšanas līmeņi
Ja neitropēnija ir vienīgā toksicitāte jebkurā devā, pievienojiet granulocītu koloniju stimulējošo faktoru (G-CSF) un saglabājiet lenalidomīda devu..
• Trombocitopēnija
• Neitropēnija
a Ja subjekts nav saņēmis G-CSF terapiju, sāciet G-CSF terapiju. Nākamā cikla 1. dienā pēc vajadzības turpiniet GCSF un saglabājiet melfalāna devu, ja neitropēnija bija vienīgā DLT. Pretējā gadījumā samaziniet vienu devas līmeni nākamā cikla sākumā.
Neitropēnijas gadījumā jāapsver augšanas faktoru izmantošana pacientu ārstēšanā.
Multiplā mieloma ar vismaz vienu iepriekšēju terapiju
Ieteicamā deva
Ieteicamā sākumdeva ir 25 mg lenalidomīda perorāli vienu reizi dienā atkārtotu 28 dienu ciklu 1.-21. Ieteicamā deksametazona deva ir 40 mg iekšķīgi vienu reizi dienā katra 28 dienu cikla 1. – 4., 9. – 12. Un 17. – 20. Dienā pirmajos 4 terapijas ciklos un 40 mg vienu reizi dienā pēc tam. ik pēc 28 dienām.
Devu var turpināt vai mainīt, pamatojoties uz klīniskajiem un laboratorijas rezultātiem (skatīt apakšpunktu 4.4). Ārstiem rūpīgi jāizvērtē lietojamā deksametazona deva, ņemot vērā pacienta stāvokli un slimības stāvokli.
Ārstēšanu ar lenalidomīdu nedrīkst sākt, ja ANC ir plazmas šūnu kaulu smadzenes, ja trombocītu skaits ir
Ieteicamā devas pielāgošana ārstēšanas laikā un pēc ārstēšanas atsākšanas
Kā apkopots zemāk esošajās tabulās, devas pielāgošana ir ieteicama 3. vai 4. pakāpes neitropēnijas vai trombocitopēnijas ārstēšanai vai jebkuras 3. vai 4. pakāpes toksicitātes ārstēšanai, kas, domājams, ir saistīta ar lenalidomīdu.
• Devas samazināšanas līmeņi
• Trombocitopēnija
• Neitropēnija
Neitropēnijas gadījumā jāapsver augšanas faktoru izmantošana pacientu ārstēšanā.
Mielodisplastiskie sindromi
Ārstēšanu ar lenalidomīdu nedrīkst uzsākt, ja ir ANC
Ieteicamā deva
Ieteicamā sākuma deva ir 10 mg lenalidomīda perorāli vienu reizi dienā atkārtotu 28 dienu ciklu 1.-21. Devu var turpināt vai mainīt, pamatojoties uz klīniskajiem un laboratorijas rezultātiem (skatīt apakšpunktu 4.4).
Ieteicamā devas pielāgošana ārstēšanas laikā un pēc ārstēšanas atsākšanas
Kā apkopots zemāk esošajās tabulās, devas pielāgošana ir ieteicama 3. vai 4. pakāpes neitropēnijas vai trombocitopēnijas ārstēšanai vai jebkuras 3. vai 4. pakāpes toksicitātes ārstēšanai, kas, domājams, ir saistīta ar lenalidomīdu.
• Devas samazināšanas līmeņi
Pacientiem, kuri sāk lietot 10 mg devu un kuriem ir trombocitopēnija vai neitropēnija:
• Trombocitopēnija
• Neitropēnija
Lenalidomīda darbības apturēšana
Pacientiem, kuriem 4 mēnešu laikā pēc terapijas uzsākšanas nav vismaz vieglas eritroidās atbildes reakcijas, ko pierāda transfūzijas prasību samazināšanās par vismaz 50%, vai, ja netiek veikta pārliešana, hemoglobīna līmeņa paaugstināšanās par 1 g / dl, jāpārtrauc lenalidomīda lietošana ārstēšana.
Mantijas šūnu limfoma
Ieteicamā deva
Ieteicamā sākumdeva ir 25 mg lenalidomīda perorāli vienu reizi dienā atkārtotu 28 dienu ciklu 1.-21.
Analīzi turpina vai maina, pamatojoties uz klīniskajiem un laboratorijas rezultātiem (skatīt apakšpunktu 4.4).
Ieteicamā devas pielāgošana ārstēšanas laikā un pēc ārstēšanas atsākšanas
Kā apkopots zemāk esošajās tabulās, devu pielāgošana ir ieteicama 3. vai 4. pakāpes neitropēnijas vai trombocitopēnijas ārstēšanai vai jebkuras 3. vai 4. pakāpes toksicitātes ārstēšanai, kas, domājams, ir saistīta ar lenalidomīdu.
• Devas samazināšanas līmeņi
1 - Valstīs, kur ir pieejamas 2,5 mg kapsulas.
• Trombocitopēnija
• Neitropēnija
• Audzēja uzliesmojuma reakcija
Ārstēšanu ar lenalidomīdu var turpināt pacientiem ar Audzēja uzliesmojuma reakcija, 1. vai 2. pakāpes atlaišanas atlīdzība, bez pārtraukuma vai izmaiņām, pēc ārsta ieskatiem. Pacientiem ar 3. vai 4. pakāpes TFR ārstēšana ar lenalidomīdu jāpārtrauc, līdz TFR tiek samazināts līdz ≤ 1. pakāpei; Simptomu ārstēšanai pacientus var ārstēt saskaņā ar 1. un 2. pakāpes TFR vadlīnijām (skatīt apakšpunktu 4.4).
Visi pacienti
Citu 3. vai 4. pakāpes toksisko efektu gadījumā, kas, domājams, ir saistīti ar lenalidomīdu, ārstēšana jāpārtrauc un jāsāk ar nākamo mazāko devu tikai tad, ja toksicitāte pēc ārsta ieskatiem ir samazinājusies līdz ≤ 2. pakāpei.
2. vai 3. pakāpes ādas izsitumu gadījumā jāapsver lenalidomīda lietošanas pārtraukšana vai pārtraukšana. Ārstēšana ar lenalidomīdu jāpārtrauc, ja rodas angioneirotiskā tūska, 4. pakāpes izsitumi, eksfoliatīvi vai bullozi izsitumi vai ja ir aizdomas par Stīvensu-Džonsonu (SSJ) vai toksisku epidermu nekrolīzi (NET), un šo reakciju dēļ to nedrīkst atsākt pēc lietošanas pārtraukšanas.
Īpašas populācijas
Pediatriskā populācija
Revlimid nedrīkst lietot bērniem un pusaudžiem no dzimšanas līdz 18 gadu vecumam drošības apsvērumu dēļ (skatīt apakšpunktu 4.4).
Gados vecāki pacienti
Pašlaik pieejamie farmakokinētikas dati ir aprakstīti 5.2. Lenalidomīdu klīniskajos pētījumos lietoja pacientiem ar multiplo mielomu līdz 91 gada vecumam, pacientiem ar mielodisplastiskiem sindromiem līdz 95 gadu vecumam un pacientiem ar mantijas šūnu limfomu līdz 88 gadu vecumam (skatīt 5.1. Apakšpunktu).
Nesen diagnosticētiem multiplās mielomas pacientiem, kuri ir sasnieguši 75 gadu vecumu un vecāki, kuri tika ārstēti ar lenalidomīdu, bija biežāk sastopamas nopietnas blakusparādības un blakusparādības, kuru dēļ ārstēšana tika pārtraukta (skatīt 4.4. Apakšpunktu). pirms ārstēšanas uzsākšanas rūpīgi jāizvērtē (skatīt apakšpunktu 4.4).
• Nesen diagnosticēta multiplā mieloma
Pacientiem, kas vecāki par 75 gadiem, kuri tiek ārstēti ar lenalidomīdu kombinācijā ar deksametazonu, deksametazona sākuma deva ir 20 mg dienā katra 28 dienu ārstēšanas cikla 1., 8., 15. un 22. dienā.
Pacientiem pēc 75 gadu vecuma, kuri tiek ārstēti ar lenalidomīdu kombinācijā ar melfalānu un prednizonu, devas pielāgošana netiek ierosināta.
Klīniskajos pētījumos ar nesen diagnosticētu multiplo mielomu pacientiem, kas nav piemēroti transplantācijai, kombinētā lenalidomīda terapija pacientiem, kas vecāki par 75 gadiem, bija mazāk panesama nekā jaunākiem cilvēkiem. Šo pacientu vidū to pacientu daļa, kuri pārtrauca ārstēšanu nepanesības dēļ (3. vai 4. pakāpes blakusparādības un nopietnas blakusparādības), bija augstāka nekā pacientiem vecumā
• Multiplā mieloma, kas iepriekš ārstēta ar vismaz vienu terapiju
Pacientu procentuālā daļa ar multiplo mielomu vecumā no 65 gadiem būtiski neatšķīrās starp lenalidomīda / deksametazona un placebo / deksametazona grupām. Kopumā netika novērotas atšķirības starp drošību un efektivitāti starp šiem pacientiem un jaunākiem pacientiem, lai gan nevar izslēgt lielāku vecāku pacientu noslieci.
• Mielodisplastiskie sindromi
Pacientiem ar mielodisplastiskiem sindromiem, kuri tika ārstēti ar lenalidomīdu, netika novērota vispārēja drošuma un efektivitātes atšķirība starp pacientiem, kas vecāki par 65 gadiem, un jaunākiem pacientiem.
• Mantijas šūnu limfoma
Pacientiem ar mantijas šūnu limfomu, kuri tika ārstēti ar lenalidomīdu, netika novērota vispārēja drošuma un efektivitātes atšķirība starp 65 gadus veciem un vecākiem pacientiem un pacientiem līdz 65 gadu vecumam.
Tā kā gados vecākiem pacientiem, visticamāk, ir nieru darbības traucējumi, īpaša piesardzība jāievēro, izvēloties devu, un piesardzības nolūkos jāveic nieru darbības kontrole.
Pacienti ar nieru mazspēju
Lenalidomīds būtiski izdalās caur nierēm; pacientiem ar augstāku nieru mazspējas pakāpi terapijas panesamība var mainīties (skatīt apakšpunktu 4.4). Īpaša uzmanība jāpievērš devas izvēlei un ieteicams kontrolēt nieru darbību.
Pacientiem ar vieglu nieru mazspēju un multiplo mielomu, mielodisplastiskiem sindromiem vai mantijas šūnu limfomu deva nav jāpielāgo. Pacientiem ar vidēji smagu vai smagu nieru mazspēju vai nieru slimību beigu stadijā, terapijas sākumā un visā ārstēšanas laikā ieteicams pielāgot devu. Nav III fāzes klīniskās izpētes pieredzes pacientiem ar beigu stadijas nieru slimību (ESRD). ) (CLcr dialīze).
• Multiplā mieloma
1 Pēc 2 cikliem devu var palielināt līdz 15 mg vienu reizi dienā, ja pacients nereaģē uz ārstēšanu, bet panes zāles.
2 Valstīs, kur ir pieejamas 7,5 mg kapsulas.
• Mielodisplastiskie sindromi
* Ieteicamie devas samazināšanas līmeņi ārstēšanas laikā un pēc terapijas atsākšanas, lai pārvaldītu 3. vai 4. pakāpes neitropēniju vai trombocitopēniju vai citu 3. vai 4. pakāpes toksicitāti, ko uzskata par saistītu ar lenalidomīdu, kā aprakstīts iepriekš.
• Mantijas šūnu limfoma
1 Pēc 2 cikliem devu var palielināt līdz 15 mg vienu reizi dienā, ja pacients nereaģē uz ārstēšanu, bet panes zāles.
2 Valstīs, kur ir pieejamas 7,5 mg kapsulas.
Pēc lenalidomīda terapijas uzsākšanas turpmāka lenalidomīda devas pielāgošana pacientiem ar nieru darbības traucējumiem jābalsta uz ārstēšanas panesamību katram pacientam, kā aprakstīts iepriekš.
Pacienti ar aknu darbības traucējumiem
Lenalidomīds nav oficiāli pētīts pacientiem ar aknu darbības traucējumiem, un nav īpašu devu ieteikumu.
Lietošanas veids
Iekšķīgai lietošanai.
Revlimid kapsulas jālieto norādītajās dienās, aptuveni tajā pašā laikā. Kapsulas nedrīkst atvērt, salauzt vai košļāt. Kapsulas jānorij veselas, vēlams, uzdzerot ūdeni, kopā ar ēdienu vai bez tā. Pacients var lietot aizmirsto devu, ja tas ir mazāk nekā 12 stundas pēc paredzētā lietošanas laika. Ja, no otras puses, tas ir vairāk nekā 12 stundas, pacients nedrīkst lietot aizmirsto devu, bet jāgaida ierastā deva nākamās dienas laiks, lai ieņemtu nākamo devu.
Ieteicams izdarīt spiedienu tikai uz vienu kapsulas pusi, lai to izņemtu no blistera, tādējādi samazinot deformācijas vai salaušanas risku.
04.3 Kontrindikācijas -
• Paaugstināta jutība pret aktīvo vielu vai jebkuru no 6.1. Apakšpunktā uzskaitītajām palīgvielām.
• Sieviete stāvoklī.
• sievietes reproduktīvā vecumā, ja vien nav izpildīti visi Grūtniecības profilakses programmas nosacījumi (skatīt apakšpunktus 4.4 un 4.6).
04.4 Īpaši brīdinājumi un piesardzība lietošanā -
Piesardzības pasākumi grūtniecības gadījumā
Lenalidomīds ir strukturāli saistīts ar talidomīdu-aktīvo vielu ar zināmu teratogēnu iedarbību uz cilvēkiem, kas izraisa smagus dzīvībai bīstamus iedzimtus defektus. Lenalidomīds pērtiķiem izraisīja malformācijas, kas līdzīgas talidomīda aprakstītajām (skatīt 4.6. Un 5.3. Apakšpunktu). Lenalidomīda teratogēna iedarbība Tas ir paredzēts cilvēkiem grūtniecības laikā.
Grūtniecības profilakses programmas nosacījumi ir jāievēro visiem pacientiem, ja vien nav pārliecinošu pierādījumu tam, ka pacients nevar palikt stāvoklī.
Kritēriji, lai konstatētu, ka sieviete nav reproduktīvā vecumā
Tiek uzskatīts, ka sieviete vai vīrieša partneris var palikt stāvoklī, ja vien viņa neatbilst vismaz vienam no šādiem kritērijiem:
• Vecums ≥ 50 gadi un dabiska amenoreja * ≥ 1 gads
• Ginekologa apstiprināta priekšlaicīga olnīcu mazspēja
• Iepriekšēja divpusēja salpingo-ooforektomija vai histerektomija
• XY genotips, Tērnera sindroms, dzemdes agenēze.
* Amenoreja pēc pretvēža terapijas vai zīdīšanas laikā neizslēdz iespējamo auglību.
Orientācija
Lenalidomīds ir kontrindicēts sievietēm reproduktīvā vecumā, ja vien nav izpildīti visi šie nosacījumi:
• Pacients apzinās, ka ir gaidāms teratogēns risks auglim
• Pacients apzinās nepieciešamību bez pārtraukuma izmantot efektīvas kontracepcijas metodes 4 nedēļas pirms ārstēšanas uzsākšanas, visu ārstēšanas laiku un līdz 4 nedēļām pēc ārstēšanas beigām.
• Pat amenorejas klātbūtnē reproduktīvā vecumā pacientam jāievēro visi ieteikumi efektīvai kontracepcijai
• Pacientam jāspēj ievērot efektīvus kontracepcijas pasākumus
• Pacients ir informēts un apzinās iespējamās grūtniecības sekas un nepieciešamību nekavējoties meklēt medicīnisko palīdzību, ja pastāv grūtniecības risks
• Pacients apzinās nepieciešamību sākt ārstēšanu, tiklīdz pēc negatīva grūtniecības testa ir izdalīts lenalidomīds
• Pacients apzinās nepieciešamību un piekrīt veikt grūtniecības testus ik pēc 4 nedēļām, izņemot gadījumus, kad apstiprināta sterilizācija ar olvadu ligāciju
• Pacients atzīst, ka viņa apzinās riskus un nepieciešamos piesardzības pasākumus, kas saistīti ar lenalidomīda lietošanu
Vīriešiem, kuri lieto lenalidomīdu, farmakokinētikas pētījumi parādīja, ka ārstēšanas laikā lenalidomīda spermā ir ļoti zems līmenis un tas nav nosakāms veselīgu personu spermā 3 dienas pēc vielas lietošanas pārtraukšanas (skatīt 5.2. Punktu). Piesardzības nolūkos visiem vīriešu dzimuma pacientiem, kuri lieto lenalidomīdu, jāatbilst šādiem nosacījumiem:
• Jāapzinās paredzamais teratogēniskais risks seksuālu aktivitāšu gadījumā ar grūtnieci vai reproduktīvā vecumā
• Jāapzinās nepieciešamība lietot prezervatīvus seksuālas darbības gadījumā ar grūtnieci vai potenciāli auglīgu sievieti, kura ārstēšanas laikā un 1 nedēļu pēc devas apturēšanas un / vai ārstēšanas neizmanto efektīvu kontracepciju (pat ja vīrietim ir veikta vazektomija) pārtraukšana.
• Jāapzinās, ka, ja partnerim iestājas grūtniecība, kamēr pacients lieto Revlimid vai neilgi pēc Revlimid terapijas pārtraukšanas, viņam par to nekavējoties jāinformē ārsts un jānosūta partneris pie speciālista vai teratologa, kurš var novērtēt situāciju un sniegt atzinumu.
Sievietēm reproduktīvā vecumā ārstam jānodrošina, ka:
• Pacients atbilst Grūtniecības profilakses programmas prasībām, ieskaitot apstiprinājumu, ka viņai ir atbilstošs izpratnes līmenis
• Pacients ir pieņēmis iepriekš minētos nosacījumus
Kontracepcija
Sievietēm reproduktīvā vecumā 4 nedēļas pirms terapijas, terapijas laikā un līdz 4 nedēļām pēc terapijas ar lenalidomīdu jāizmanto efektīva kontracepcijas metode, kā arī devas pārtraukšanas gadījumā, ja vien pacients neapņemas ievērot "absolūtu un nepārtrauktu atturēšanos, apstiprinātu mēnesi". Ja efektīva kontracepcijas terapija vēl nav sākta, pacients jānosūta pie ārsta speciālista, lai izveidotu efektīvu kontracepcijas metodi.
Tālāk ir sniegti piemērotu kontracepcijas metožu piemēri:
• Augu
• Levonorgestrelu atbrīvojošā intrauterīnā sistēma (IUS)
• Medroksiprogesterona acetāta depo
• Olvadu sterilizācija
• dzimumakts tikai ar vīrieti, kuram ir veikta vazektomija; vazektomija jāapstiprina ar divām negatīvām spermas analīzēm
• tikai progestīnu saturošas tabletes ovulācijas inhibēšanai (piemēram, desogestrels)
Tā kā ir palielināts venozās trombembolijas risks pacientiem ar multiplo mielomu, kuri lieto lenalidomīdu kombinācijā, un mazākā mērā pacientiem ar mielodisplastiskiem sindromiem un mantijas šūnu limfomu, lietojot tikai lenalidomīdu, perorālo kontracepcijas līdzekļu lietošana nav ieteicama. arī 4.5. Ja pacients pašlaik lieto kombinētos perorālos kontracepcijas līdzekļus, viņai dzimstības kontroles metode jāaizstāj ar kādu no iepriekš minētajām. Venozās trombembolijas risks saglabājas 4-6 nedēļas pēc kombinēto perorālo kontracepcijas līdzekļu lietošanas pārtraukšanas. Vienlaicīgas deksametazona terapijas laikā var samazināties kontracepcijas steroīdu efektivitāte (skatīt apakšpunktu 4.5).
Levonorgestrelu atbrīvojošie intrauterīnie implanti un sistēmas ir saistītas ar paaugstinātu infekcijas risku, ievietojot to, kā arī neregulāru asiņošanu no maksts. Jāapsver antibiotiku profilakse, īpaši pacientiem ar neitropēniju.
Vara atbrīvojošas intrauterīnās ierīces parasti nav ieteicamas, ņemot vērā iespējamo infekcijas risku no ievietošanas brīža un menstruālā asins zuduma dēļ, kas var nelabvēlīgi ietekmēt pacientus ar neitropēniju vai trombocitopēniju.
Grūtniecības tests
Saskaņā ar vietējo praksi pacientiem reproduktīvā vecumā grūtniecības testi ar minimālo jutību 25 mIU / ml jāveic ārsta uzraudzībā, kā aprakstīts turpmāk. Šis pienākums attiecas arī uz pacientiem reproduktīvā vecumā, kuri praktizē absolūtu un nepārtrauktu atturēšanos. Ideālā gadījumā grūtniecības tests, recepte un zāļu izsniegšana jāveic vienā dienā. Lenalidomīds jāizsniedz pacientiem reproduktīvā vecumā 7 dienu laikā pēc izrakstīšanas.
Pirms ārstēšanas uzsākšanas
Kad pacients ir lietojis efektīvu kontracepcijas līdzekli vismaz 4 nedēļas, konsultācijas laikā, kurā izrakstīts lenalidomīds, vai 3 dienas pirms ārsta apmeklējuma, jāveic medicīniski kontrolēts grūtniecības tests. Pārbaudei jāpārliecinās, ka pirms ārstēšanas ar lenalidomīdu uzsākšanas pacients nav stāvoklī.
Pēcpārbaude un ārstēšanas beigas
Medicīniski kontrolēts grūtniecības tests jāatkārto ik pēc 4 nedēļām, ieskaitot 4 nedēļas pēc ārstēšanas beigām, izņemot gadījumus, kad ir apstiprināta olvadu sterilizācija. Šie grūtniecības testi jāveic tajā pašā dienā, kad izrakstījis ārsts, vai 3 dienas pirms ārsta apmeklējuma.
Vīriešu kārtas pacienti
Ārstēšanas laikā lenalidomīda spermā ir ļoti zems līmenis, un tas nav nosakāms veselīgu personu spermā 3 dienas pēc zāļu lietošanas pārtraukšanas (skatīt 5.2. Apakšpunktu). Piesardzības nolūkos un ņemot vērā īpašas pacientu grupas ar ilgstošu eliminācijas laiku, piemēram, pacientiem ar nieru darbības traucējumiem, visiem vīriešiem, kuri lieto lenalidomīdu, visā ārstēšanas laikā jāizmanto prezervatīvi, vienlaikus pārtraucot ārstēšanu. terapija, ja jūsu partneris ir stāvoklī vai reproduktīvā vecumā un neizmanto efektīvu kontracepciju (pat ja vīrietim ir veikta vazektomija).
Papildu piesardzība lietošanā
Pacientiem jāiesaka nekad nedot šīs zāles citiem cilvēkiem un ārstēšanas beigās atdot neizlietotās kapsulas farmaceitam.
Pacientiem nevajadzētu ziedot asinis lenalidomīda terapijas laikā un vismaz vienu nedēļu pēc ārstēšanas pārtraukšanas.
Izglītības materiāli, recepšu un izsniegšanas ierobežojumi
Lai palīdzētu pacientiem izvairīties no augļa pakļaušanas lenalidomīda iedarbībai, reģistrācijas apliecības īpašnieks nodrošinās ārstniecības darbiniekiem izglītojošus materiālus, lai pastiprinātu brīdinājumus par paredzamo lenalidomīda teratogenitāti, pirms terapijas uzsākšanas konsultētu par kontracepciju un sniegtu norādījumus par grūtniecības testa nepieciešamību. . Ārstam jāinformē pacienti vīrieši un sievietes par teratogēno risku un stingriem grūtniecības novēršanas pasākumiem, kā noteikts Grūtniecības profilakses programmā, un jānodrošina pacientiem atbilstoša izglītojoša bukleta, pacienta karte un / vai līdzvērtīgs instruments, ievērojot pasākumus, kas īstenoti plkst. valsts līmenī. Sadarbībā ar katru valsts kompetento iestādi ir ieviesta valsts izplatīšanas kontroles sistēma. Šī sistēma paredz pacienta kartes un / vai līdzvērtīga instrumenta izmantošanu, recepšu un izsniegšanas kontroli, kā arī detalizētu datu vākšanu. attiecībā uz indikāciju, lai rūpīgi kontrolētu lietošanu ārpus marķējuma ideālā gadījumā grūtniecības pārbaudei, receptes izsniegšanai un zāļu izsniegšanai vajadzētu notikt tajā pašā dienā. Lenalidomīds jāizsniedz pacientiem reproduktīvā vecumā 7 dienu laikā no izrakstīšanas dienas un pēc "negatīva grūtniecības testa rezultāta, kas veikts ārsta uzraudzībā.
Papildu īpaši brīdinājumi un piesardzība lietošanā
Sirds un asinsvadu sistēmas traucējumi
Miokarda infarkts
Miokarda infarkta gadījumi ir novēroti pacientiem, kuri saņēma lenalidomīdu, īpaši pacientiem ar zināmiem riska faktoriem, un pirmo 12 mēnešu laikā, ja to lietoja kombinācijā ar deksametazonu. Pacienti ar zināmiem riska faktoriem, ieskaitot tos, kuriem iepriekš bijusi tromboze, rūpīgi jānovēro un jārīkojas, lai samazinātu visus maināmos riska faktorus (piemēram, smēķēšanu, hipertensiju un hiperlipidēmiju).
Venozas un arteriālas trombemboliskas parādības
Pacientiem ar multiplo mielomu lenalidomīda un deksametazona kombinācija ir saistīta ar paaugstinātu vēnu trombembolijas (galvenokārt dziļo vēnu trombozes un plaušu embolijas) un arteriālās trombembolijas (galvenokārt miokarda infarkta un cerebrovaskulāru notikumu) risku. Venoza trombembolija novērota mazāk. lietojot kopā ar lenalidomīdu kombinācijā ar melfalānu un prednizonu nesen diagnosticētas multiplās mielomas gadījumā un kā monoterapiju mielodisplastisko sindromu gadījumā Skatīt 4.5 un 4.8 apakšpunktu.
Pacientiem ar mielodisplastiskiem sindromiem un mantijas šūnu limfomu ārstēšana tikai ar lenalidomīdu ir saistīta arī ar vēnu trombembolijas risku (galvenokārt dziļo vēnu trombozi un plaušu emboliju), bet mazākā mērā nekā pacientiem ar multiplo mielomu - skatīt 4.5. 4.8.
Tādēļ pacienti ar zināmiem trombembolijas riska faktoriem - ieskaitot iepriekšēju trombozi - rūpīgi jānovēro. Jāveic pasākumi, lai samazinātu visus maināmos riska faktorus (piemēram, smēķēšanu, hipertensiju un hiperlipidēmiju). Šiem pacientiem trombozes risku var palielināt arī vienlaicīga eritropoētisko līdzekļu lietošana vai trombembolijas anamnēze. Tādēļ pacientiem ar multiplo mielomu, kuri lieto lenalidomīdu un deksametazonu, ieteicams lietot eritropoētiskos līdzekļus vai citus līdzekļus, kas var palielināt trombozes risku, piemēram, hormonu aizstājterapija. Ja hemoglobīna koncentrācija palielinās virs 12 g / dl, eritropoētisko līdzekļu lietošana jāpārtrauc.
Pacientiem un ārstiem jāapzinās nepieciešamība pievērst uzmanību trombembolijas pazīmēm un simptomiem. Pacientiem jāmeklē medicīniskā palīdzība, ja parādās tādi simptomi kā elpas trūkums, sāpes krūtīs, apakšējo vai augšējo ekstremitāšu pietūkums. Profilaktiskos nolūkos jāiesaka lietot antitrombotiskas zāles, īpaši pacientiem ar papildu trombozes riska faktoriem.Lēmums par profilaktisku antitrombotisku pasākumu pieņemšanu jāpieņem pēc rūpīga katra pacienta riska faktoru izvērtēšanas.
Ja pacientam rodas kāds trombembolisks notikums, ārstēšana jāpārtrauc un jāsāk standarta antikoagulantu terapija. Kad pacients ir stabilizējies ar antikoagulāciju un visas trombembolijas komplikācijas ir izzudušas, ārstēšanu ar lenalidomīdu var atsākt ar sākotnējo devu pēc ieguvuma un riska novērtējuma. Ārstēšanas laikā ar lenalidomīdu pacientam jāturpina antikoagulācijas terapija.
Neitropēnija un trombocitopēnija
Galvenās lenalidomīda devu ierobežojošās toksicitātes ir neitropēnija un trombocitopēnija. Lai uzraudzītu iespējamo citopēnijas rašanos, pirmajās 8 ārstēšanas nedēļās sākotnēji reizi nedēļā jāveic pilnīgs asins šūnu skaits, ieskaitot balto asins šūnu skaitu, ieskaitot diferenciālo, trombocītu skaitu, hemoglobīnu un hematokrītu. Lenalidomīds un pēc tam reizi mēnesī Pacientiem ar mantijas šūnu limfomu novērošanas grafiks jāveic ik pēc 2 nedēļām 3. un 4. ciklā un pēc tam katra cikla sākumā. Var būt nepieciešama devas samazināšana (skatīt 4.2. Apakšpunktu). Neitropēnijas gadījumā ārstam jāapsver augšanas faktoru izmantošana pacientu vadībā. Pacientiem jāiesaka nekavējoties ziņot par drudža epizodēm. Ieteicama piesardzība, lietojot lenalidomīdu vienlaikus ar citiem mielosupresantiem.
• Nesen diagnosticēta multiplā mieloma pacientiem, kuri ārstēti ar lenalidomīdu kombinācijā ar mazu deksametazona devu
4. pakāpes neitropēnija tika novērota mazākā mērā lenalidomīda kombinācijā ar mazām deksametazona devām, salīdzinot ar salīdzinošo grupu (8,5% Rd [nepārtraukta ārstēšana] un Rd18 [ārstēšana 18 četru nedēļu ciklos], salīdzinot ar 15 % melfalāna / prednizona / talidomīda grupā, skatīt apakšpunktu 4.8). 4. pakāpes febrilās neitropēnijas epizodes atbilda salīdzinājuma grupai (0,6% pacientu, kuri tika ārstēti ar lenalidomīdu / deksametazonu Rd un Rd18, salīdzinot ar 0,7% pacientu melfalāna / prednizona / talidomīda grupā, skatīt 4.8. Apakšpunktu). Pacientiem jāiesaka nekavējoties ziņot par drudža epizodēm, un var būt nepieciešama devas samazināšana (skatīt 4.2. Apakšpunktu).
3. vai 4. pakāpes trombocitopēnija Rd un Rd18 grupās tika novērota mazākā mērā nekā salīdzinājuma grupā (attiecīgi 8,1% pret 11,1%). Pacientiem un ārstiem jāievēro asiņošanas pazīmes un simptomi, tostarp petehijas un deguna asiņošana, īpaši pacientiem, kuri vienlaikus tiek ārstēti un var izraisīt asiņošanu (skatīt apakšpunktu 4.8, Asiņošanas traucējumi).
• Nesen diagnosticēta multiplā mieloma pacientiem, kuri ārstēti ar lenalidomīdu kombinācijā ar melfalānu un prednizonu
Klīniskajos pētījumos pacientiem ar nesen diagnosticētu multiplo mielomu lenalidomīda kombinācija ar melfalānu un prednizonu ir saistīta ar lielāku 4. pakāpes neitropēnijas biežumu (34,1% pacientu melfalāna, prednizona un lenalidomīda grupā, kam seko lenalidomīds [MPR + R] un melfalānu, prednizonu un lenalidomīdu, kam sekoja placebo [MPR + p], salīdzinot ar 7,8% pacientu, kuri tika ārstēti ar MPp + p; skatīt 4.8. apakšpunktu). R / MPR + p, salīdzinot ar 0,0% pacientiem, kuri tika ārstēti ar MPp + p; skatīt apakšpunktu 4.8).
Pacientiem ar multiplo mielomu lenalidomīda kombinācija ar melfalānu un prednizonu ir saistīta ar lielāku 3. un 4. pakāpes trombocitopēnijas sastopamību (40,4% pacientiem, kuri ārstēti ar MMR + R / MMR + p, salīdzinot ar 13,7% pacientiem, kuri ārstēti ar MPp + p; skatīt apakšpunktu 4.8) Pacientiem un ārstiem jābūt uzmanīgiem par asiņošanas pazīmēm un simptomiem, ieskaitot petehijas un deguna asiņošanu, īpaši pacientiem, kuri vienlaikus tiek ārstēti ar zālēm, kas palielina noslieci uz asiņošanu (skatīt apakšpunktu 4.8, Asiņošanas traucējumi).
• Multiplā mieloma ar vismaz vienu iepriekšēju terapiju
Pacientiem ar multiplo mielomu, kuri saņem vismaz vienu iepriekšēju terapiju, lenalidomīda un deksametazona kombinācija ir saistīta ar lielāku 4. pakāpes neitropēnijas biežumu (5,1% pacientu, kuri tika ārstēti ar lenalidomīdu / deksametazonu, salīdzinot ar 0,6% pacientu, kuri tika ārstēti ar placebo / deksametazonu; 4. pakāpes febrilās neitropēnijas epizodes tika novērotas reti (0,6% pacientu, kuri tika ārstēti ar lenalidomīdu / deksametazonu, salīdzinot ar 0,0% pacientu, kuri tika ārstēti ar placebo / deksametazonu; skatīt apakšpunktu 4.8) Pacientiem jāiesaka nekavējoties ziņot par drudža epizodēm. Var būt nepieciešama devas samazināšana (skatīt 4.2. Apakšpunktu). Neitropēnijas gadījumā ārstiem jāapsver augšanas faktoru izmantošana pacientu ārstēšanā.
Pacientiem ar multiplo mielomu lenalidomīda un deksametazona kombinācija ir saistīta ar biežāku 3. un 4. pakāpes trombocitopēnijas sastopamību (attiecīgi 9,9% un 1,4%, lielāks 3. pakāpes trombocitopēnijas biežums). 3. un 4. pakāpe (9.9%) un 1,4% pacientu, kuri tika ārstēti attiecīgi ar lenalidomīdu / deksametazonu, salīdzinot ar 2,3% un 0,0% pacientu, kuri tika ārstēti ar placebo / deksametazonu; skatīt 4.8. apakšpunktu.) vienlaikus ārstēti ar zālēm, kas var izraisīt asiņošanu (skatīt apakšpunktu 4.8, Asiņošanas traucējumi).
• Mielodisplastiskie sindromi
Pacientiem ar mielodisplastiskiem sindromiem ārstēšana ar lenalidomīdu ir saistīta ar lielāku 3. un 4. pakāpes neitropēnijas un trombocitopēnijas biežumu nekā pacientiem, kas ārstēti ar placebo (skatīt 4.8. Apakšpunktu).
• Mantijas šūnu limfoma
Pacientiem ar mantijas šūnu limfomu ārstēšana ar lenalidomīdu ir saistīta ar lielāku 3. un 4. pakāpes neitropēnijas biežumu nekā pacientiem ar kontroles grupu (skatīt 4.8. Apakšpunktu).
Infekcija ar neitropēniju vai bez tās
Vairāki mielomas pacienti ir pakļauti infekcijām, tostarp pneimonijai. Ārstēšanas laikā ar lenalidomīdu kombinācijā ar deksametazonu tika novērots lielāks infekciju biežums nekā ar MPT. Neitropēnijas kontekstā ≥ 3. Pakāpes infekcijas radās mazāk nekā trešdaļai pacientu. Pacienti ar zināmiem infekcijas riska faktoriem rūpīgi jānovēro. Visiem pacientiem jāiesaka nekavējoties konsultēties ar savu ārstu, kad parādās pirmās infekcijas pazīmes (piemēram, klepus, drudzis utt.), Lai varētu nekavējoties iejaukties, lai samazinātu slimības smagumu.
Nieru mazspēja
Lenalidomīds būtiski izdalās caur nierēm. Tādēļ pacientiem ar nieru mazspēju īpaša uzmanība jāpievērš devas izvēlei un ieteicams kontrolēt nieru darbību (skatīt 4.2. Apakšpunktu).
Vairogdziedzera darbības traucējumi
Ir novēroti hipotireozes un hipertireozes gadījumi. Pirms ārstēšanas uzsākšanas ieteicams optimāli kontrolēt blakusslimības, kas ietekmē vairogdziedzera darbību. Sākotnēji un ārstēšanas laikā ieteicams kontrolēt vairogdziedzera darbību.
Perifēra neiropātija
Lenalidomīds ir strukturāli saistīts ar talidomīdu, kas, kā zināms, izraisa smagu perifēro neiropātiju. Ilgstoši lietojot lenalidomīdu nesen diagnosticētas multiplās mielomas ārstēšanai, netika novērota perifērās neiropātijas palielināšanās.
Audzēja uzliesmojuma reakcija un audzēja līzes sindroms
Tā kā lenalidomīdam piemīt pretaudzēju aktivitāte, rodas audzēja sabrukšanas sindroma komplikācijas (Audzēja līzes sindroms, TLS). TLS un Audzēja uzliesmojuma reakcija (TFR) parasti novēroja pacientiem ar hronisku limfoleikozi (CLL) un retāk pacientiem ar limfomu, kas ārstēti ar lenalidomīdu. Ārstēšanas laikā ar lenalidomīdu ziņots par TLS gadījumiem ar letālu iznākumu. Pacienti, kuriem ir TLS un TFR risks, ir tie, kuriem pirms ārstēšanas ir augsts audzēja slogs. Uzsākot ārstēšanu ar lenalidomīdu, šiem pacientiem jāievēro piesardzība. Šādus pacientus ieteicams rūpīgi uzraudzīt, īpaši pirmā cikla vai devas palielināšanas laikā, un veikt atbilstošus piesardzības pasākumus. Retos gadījumos ir ziņots par TLS pacientiem ar MM, kas ārstēti ar lenalidomīdu, bet nav ziņots par gadījumiem pacientiem ar MDS ārstēts ar lenalidomīdu.
Audzēja masa
• Mantijas šūnu limfoma
Lenalidomīdu nav ieteicams lietot pacientiem ar augstu audzēja slodzi, ja ir pieejamas alternatīvas ārstēšanas iespējas.
Agrīna nāve
Pētījumā MCL-002 bija acīmredzams agrīnu nāves gadījumu skaita pieaugums (20 nedēļu laikā). Pacientiem ar augstu sākotnējo audzēja slodzi ir lielāks agrīnas nāves risks: lenalidomīda grupā bija 16/81 (20%) agrīnas nāves gadījumu un 2/28 (7%) priekšlaicīgas nāves gadījumu kontroles grupā. Līdz 52 nedēļām attiecīgie skaitļi bija 32/81 (40%) un 6/28 (21%) (skatīt 5.1. Apakšpunktu).
Blakusparādības
Pētījumā MCL-002 1. ārstēšanas cikla laikā 11/81 (14%) pacienti ar augstu audzēja slodzi tika atcelti no terapijas ar lenalidomīdu, salīdzinot ar 1/28 (4%) kontroles grupā. Galvenais iemesls ārstēšanas pārtraukšanai pacientiem ar augstu audzēja slodzi 1. ārstēšanas cikla laikā lenalidomīda grupā bija saistīts ar nevēlamiem notikumiem, 7/11 (64%).
Tādēļ pacienti ar augstu audzēja slodzi rūpīgi jānovēro, vai nav nevēlamu blakusparādību (skatīt 4.8. Apakšpunktu), ieskaitot visas pazīmes Audzēja uzliesmojuma reakcija (TFR). Devas pielāgošanu TFR gadījumā skatīt 4.2.
Paaugstināta audzēja masa tika definēta kā vismaz viens bojājums ≥ 5 cm diametrā vai 3 bojājumi ≥ 3 cm.
Audzēja uzliesmojuma reakcija
• Mantijas šūnu limfoma
Ieteicama rūpīga TFR uzraudzība un novērtēšana. Pacientiem ar paaugstinātu MIPI (Mantela šūnu limfomas starptautiskais prognozes indekss) pie diagnozes vai slimības, kurai raksturīgas lielas audzēja masas (vismaz viens bojājums, kas garākajā diametrā ir ≥ 7 cm), var būt TFR risks. Tur Audzēja uzliesmojuma reakcija var simulēt slimības progresēšanu (PD). Pacienti MCL-002 un MCL-001 pētījumos, kuriem bija 1. un 2. pakāpes TFR, tika ārstēti ar kortikosteroīdiem, nesteroīdiem pretiekaisuma līdzekļiem (NPL) un / vai narkotiskiem pretsāpju līdzekļiem TFR simptomu ārstēšanai. Lēmums par TFR terapeitisko pasākumu pieņemšanu jāpieņem pēc "rūpīga katra pacienta klīniskās izvērtēšanas" (skatīt 4.2. Apakšpunktu).
Alerģiskas reakcijas
Pacientiem, kas ārstēti ar lenalidomīdu, ziņots par alerģisku / paaugstinātas jutības reakciju gadījumiem (skatīt apakšpunktu 4.8). Ieteicams rūpīgi uzraudzīt pacientus, kuriem iepriekš ir bijušas alerģiskas reakcijas pret talidomīdu, jo literatūrā ir ziņots par iespējamu krustenisko reakciju starp lenalidomīdu un talidomīdu.
Smagas ādas reakcijas
Ir ziņots par SSJ un NET gadījumiem. Ārstēšana ar lenalidomīdu jāpārtrauc eksfoliatīvu vai bullozu izsitumu gadījumā vai ja ir aizdomas par SSJ vai NET, un šo reakciju dēļ to nedrīkst atsākt pēc pārtraukšanas. Atkarībā no smaguma pakāpes jāapsver iespēja pārtraukt vai pārtraukt lenalidomīda lietošanu citām ādas reakcijām.
Laktozes nepanesamība
Revlimid kapsulas satur laktozi. Šīs zāles nevajadzētu lietot pacientiem ar retu iedzimtu galaktozes nepanesību, Lapp laktāzes deficītu vai glikozes-galaktozes malabsorbciju.
Neizmantotās kapsulas
Pacientiem jāiesaka nekad nedot šīs zāles citiem cilvēkiem un pēc ārstēšanas beigām atdot neizlietotās kapsulas farmaceitam.
Otrie primārie audzēji
Otro primāro audzēju palielināšanās (Otrā pamatskola Ļaundabīgs audzējs, SPM) mielomas slimniekiem, kuri iepriekš ārstēti ar lenalidomīdu / deksametazonu (3,98 uz 100 cilvēku gadiem), salīdzinot ar kontrolgrupām (1,38 uz 100 cilvēku gadiem). Neinvazīvie SPM sastāv no bazālo šūnu vai plakanšūnu karcinomas.
Lielākā daļa invazīvo SPM bija cieti audzēji.
Klīniskajos pētījumos ar nesen diagnosticētiem multiplās mielomas pacientiem, kuri nav piemēroti transplantācijai, pacientiem, kuri tika ārstēti ar lenalidomīdu kombinācijā ar melfalānu un prednizonu, tika novērota 4,9 reizes lielāka hematoloģiskā PMS (AML, MDS) sastopamības biežuma palielināšanās (1,75 reizes) 100 personas gadi), salīdzinot ar melfalānu kombinācijā ar prednizonu (0,36 uz 100 uz cilvēka gadu).
Pacientiem, kuri tika ārstēti ar lenalidomīdu (9 cikli) kombinācijā ar melfalānu un prednizonu (1,57 uz 100 cilvēku gadiem), salīdzinot ar melfalānu kombinācijā ar prednizonu (0,74 uz 100 uz 100 personas gadi).
Pacientiem, kuri tika ārstēti ar lenalidomīdu kombinācijā ar deksametazonu līdz progresēšanai vai 18 mēnešus, hematoloģiskās PMS sastopamības biežums (0,16 uz 100 cilvēku gadiem) nepalielinājās, salīdzinot ar talidomīdu kombinācijā ar melfalānu un prednizonu (0,79 uz 100 cilvēku gadiem). .
Pacientiem, kuri tika ārstēti ar lenalidomīdu kombinācijā ar deksametazonu līdz progresēšanai vai 18 mēnešus (1,58 uz 100 cilvēku gadiem), salīdzinot ar talidomīdu kombinācijā ar melfalānu un prednizonu (1,19 reizes uz 100), tika novērots 1,3 reizes lielāks cietā PMS sastopamības biežuma pieaugums personas gadi).
Klīniskajos pētījumos ar nesen diagnosticētiem multiplās mielomas pacientiem, kuriem ir tiesības veikt transplantāciju, pacientiem, kuri tika ārstēti ar lenalidomīdu, tūlīt pēc lielas melfalāna devas un autologu cilmes šūnu transplantācijas tika novērots palielināts hematoloģiskās PMS sastopamības biežums (Autologā cilmes šūnu transplantācija, ASCT), salīdzinot ar placebo ārstētiem pacientiem (attiecīgi 1,27 līdz 1,56 un 0,46 līdz 0,53 uz 100 cilvēku gadiem). Klīniskos pētījumos novēroti ļaundabīgu B šūnu audzēju (ieskaitot Hodžkina limfomu) gadījumi bija pacienti, kuri tika ārstēti ar lenalidomīdu pēc ASCT.
Hematoloģiskās PMS risks jāapsver pirms ārstēšanas uzsākšanas ar Revlimid kombinācijā ar melfalānu vai tūlīt pēc lielas melfalāna un ASCT devas. Ārstiem rūpīgi jāizvērtē pacienti pirms ārstēšanas un tās laikā, izmantojot standarta vēža skrīningu PMS, un jāuzsāk ārstēšana, kā norādīts.
Progresēšana līdz akūtai mieloleikozei (AML) mielodisplastiskā sindroma (MDS) gadījumā zems vai vidējs-1
• Kariotips
Sākotnējie mainīgie, ieskaitot sarežģītas citoģenētiskas novirzes, ir saistīti ar progresēšanu līdz AML pacientiem, kas atkarīgi no pārliešanas, ar izolētām 5q dzēšanas anomālijām. Apvienojot divus klīniskos pētījumus, kas veikti ar Revlimid ar zema vai vidēja riska 1 MDS, pacientiem ar sarežģītām citoģenētiskām novirzēm bija vislielākais kumulatīvais progresēšanas risks līdz AML, kas novērtēts 2 gadu laikā (38,6%). Aprēķinātais 2 gadu progresēšanas līmenis līdz AML pacientiem ar izolētu 5q dzēšanas anomāliju bija 13,8%, salīdzinot ar 17,3% pacientiem ar izolētu 5q dzēšanas anomāliju un vienu "papildu citoģenētisku anomāliju".
Līdz ar to Revlimid ieguvuma / riska attiecība nav zināma, ja MDS ir saistīta ar izolētu 5q dzēšanas anomāliju un sarežģītām citoģenētiskām novirzēm.
• TP53 statuss
TP53 mutācija ir sastopama 20-25% MDS pacientu ar zema riska 5q izolētu dzēšanas anomāliju, un tā ir saistīta ar lielāku AML progresēšanas risku. "Klīniskā pētījuma (MDS-004) post-hoc analīzē, kas tika veikta ar Revlimid ar zema vai vidēja riska 1 MDS, paredzamais 2 gadu progresēšanas ātrums līdz AML bija 27,5% pacientiem ar pozitīvu IHC-p53 (1 % spēcīgas kodolkrāsas nogriešana, izmantojot p53 proteīna imūnhistoķīmisko novērtējumu kā aizstājēju TP53 mutācijas statusam) un 3,6% pacientiem ar IHC-p53 negatīvu (p = 0,0038) (skatīt 4.8. apakšpunktu).
Progresēšana uz citiem ļaundabīgiem audzējiem mantijas šūnu limfomas gadījumā
Mantijas šūnu limfomas gadījumā potenciāls risks ir AML, ļaundabīgi B šūnu audzēji un nemelanomas ādas vēzis (NMSC).
Aknu darbības traucējumi
Pacientiem, kuri tika ārstēti ar lenalidomīdu kombinētā terapijā, tika novēroti aknu mazspējas gadījumi, arī ar letālu iznākumu: akūta aknu mazspēja, toksisks hepatīts, citolītisks hepatīts, holestātisks hepatīts un jaukts citolītiskais / holestātiskais hepatīts. Smagas zāļu izraisītas hepatotoksicitātes mehānismi joprojām nav zināmi, lai gan dažos gadījumos riska faktori var būt jau esoša vīrusu aknu slimība, paaugstināts sākotnējais aknu enzīmu līmenis un, iespējams, ārstēšana ar antibiotikām.
Bieži tika novērotas novirzes aknu darbības testos, un tās parasti bija asimptomātiskas un atgriezeniskas, pārtraucot ārstēšanu. Kad parametri ir atgriezušies sākotnējās vērtībās, var apsvērt ārstēšanas atsākšanu ar mazāku devu.
Lenalidomīds izdalās caur nierēm. Pacientiem ar nieru mazspēju ir svarīgi pielāgot devu, lai izvairītos no plazmas līmeņa sasniegšanas, kas varētu palielināt nozīmīgāku hematoloģisku blakusparādību vai hepatotoksicitātes risku. Ieteicama aknu darbības kontrole, īpaši iepriekšējas vai vienlaikus aknu vīrusu infekcijas gadījumā vai ja lenalidomīdu lieto kombinācijā ar zālēm, par kurām zināms, ka tās ir saistītas ar aknu darbības traucējumiem.
Pacienti ar nesen diagnosticētu multiplo mielomu
Pacientiem, kas vecāki par 75 gadiem, ISS stadija (3. vai 4. pakāpes nevēlamas blakusparādības, nopietnas blakusparādības, ārstēšanas pārtraukšana) bija lielāks nepanesamības līmenis (Starptautiskā posmu sistēma) III, veiktspējas statuss (PS) ≤ 2 novērtēts saskaņā ar ECOG kritērijiem (Austrumu kooperatīvā onkoloģijas grupa) vai CLcr
Katarakta
Katarakta biežāk novērota pacientiem, kuri ārstēti ar lenalidomīdu kombinācijā ar deksametazonu, īpaši ilgstošas lietošanas gadījumā. Ieteicams periodiski kontrolēt redzes spējas.
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi -
Eritropoētiskie līdzekļi vai citi līdzekļi, kas var palielināt trombozes risku, piemēram, hormonu aizstājterapija, piesardzīgi jālieto pacientiem ar multiplo mielomu, kuri lieto lenalidomīdu un deksametazonu (skatīt 4.4. Un 4.8. Apakšpunktu). lietojot lenalidomīdu un deksametazonu (skatīt 4.4. un 4.8. apakšpunktu).
Perorālie kontracepcijas līdzekļi
Nav veikti mijiedarbības pētījumi ar perorālajiem kontracepcijas līdzekļiem. Lenalidomīds nav enzīmu induktors. Studijā in vitro ar cilvēka hepatocītiem, lenalidomīds, pārbaudīts dažādās koncentrācijās, neizraisīja CYP1A2, CYP2B6, CYP2C9, CYP2C19 un CYP3A4 / 5. Tādēļ, ja lenalidomīdu lieto vienu pašu, nav paredzama indukcija, kas noved pie zāļu, tostarp hormonālo kontracepcijas līdzekļu, efektivitātes samazināšanās. Tomēr ir zināms, ka deksametazons ir vājš vai mērens CYP3A4 induktors un, iespējams, ietekmē citus enzīmus un transporta proteīnus. Nav izslēgts, ka ārstēšanas laikā var samazināties perorālo kontracepcijas līdzekļu efektivitāte.
Jāveic efektīvi pasākumi, lai izvairītos no grūtniecības (skatīt 4.4. Un 4.6. Apakšpunktu).
Varfarīns
Vienlaicīga 10 mg lenalidomīda devu lietošana neietekmēja R- un S-varfarīna vienas devas farmakokinētiku. Vienlaicīga 25 mg varfarīna devas lietošana neietekmēja lenalidomīda farmakokinētiku. Tomēr nav zināms, vai klīniskās lietošanas laikā (vienlaicīga ārstēšana ar deksametazonu) pastāv "mijiedarbība". Deksametazons ir vājš vai mērens enzīmu induktors, un tā ietekme uz varfarīnu nav zināma. Ārstēšanas laikā ieteicams rūpīgi kontrolēt varfarīna koncentrāciju.
Digoksīns
Vienlaicīga 10 mg lenalidomīda lietošana dienā palielināja digoksīna koncentrāciju plazmā par 14% (0,5 mg, vienreizēja deva) ar TI (ticamības intervāls) 90% [0,52% -28,2%]. Nav zināms, vai efekts atšķirtos terapeitiskajā situācijā (lielākas lenalidomīda devas un vienlaicīga ārstēšana ar deksametazonu). Tādēļ ārstēšanas laikā ar lenalidomīdu ieteicams kontrolēt digoksīna koncentrāciju.
Statīni
Ja statīnus lieto kopā ar lenalidomīdu, palielinās rabdomiolīzes risks, kas var būt tikai piedeva. Ir nepieciešama pastiprināta klīniskā un laboratoriskā uzraudzība, īpaši pirmajās ārstēšanas nedēļās.
Deksametazons
Vienlaicīga vai vairāku deksametazona devu (40 mg dienā) lietošana klīniski būtiski neietekmē lenalidomīda (25 mg dienā) daudzkārtējo devu farmakokinētiku.
Mijiedarbība ar P-glikoproteīnu (P-gp) inhibitoriem
In vitro, Lenalidomīds ir P-gp substrāts, bet nav P-gp inhibitors. Vairāku spēcīga P-gp inhibitora, hinidīna (600 mg, divas reizes dienā) vai vidējas darbības P-gp inhibitora / substrāta temsirolīma (25 mg) vairāku devu vienlaicīga lietošana klīniski būtiski neietekmē lenalidomīda farmakokinētiku (25 mg) Vienlaicīga lenalidomīda lietošana nemaina temsirolīma farmakokinētiku.
04.6 Grūtniecība un zīdīšanas periods -
Sievietes reproduktīvā vecumā / Kontracepcija vīriešiem un sievietēm
Sievietēm reproduktīvā vecumā jāizmanto efektīva kontracepcijas metode. Ja ārstēšanas laikā ar lenalidomīdu iestājas grūtniecība, terapija jāpārtrauc un pacientam jādodas pie speciālista vai pieredzes teratoloģijā, kurš var novērtēt situāciju un sniegt atzinumu. Ja vīrieša partneris, kas lieto lenalidomīdu, ir stāvoklī, partnerim jāiesaka doties pie speciālista ārsta vai ārsta ar pieredzi teratoloģijā, kurš var novērtēt situāciju un sniegt atzinumu.
Ārstēšanas laikā lenalidomīda spermā ir ļoti zems līmenis, un tas nav nosakāms veselīgu personu spermā 3 dienas pēc zāļu lietošanas pārtraukšanas (skatīt 5.2. Apakšpunktu). Piesardzības nolūkos un ņemot vērā īpašas pacientu grupas ar ilgstošu eliminācijas laiku, piemēram, pacientiem ar nieru darbības traucējumiem, visiem vīriešiem, kuri lieto lenalidomīdu, jāizmanto prezervatīvi visu ārstēšanas laiku, devas pārtraukšanas laikā un līdz vienai nedēļai pēc terapijas pārtraukšanas, ja jūsu partneris ir stāvoklī vai reproduktīvā vecumā un neizmanto nekādas kontracepcijas metodes.
Grūtniecība
Lenalidomīds ir strukturāli saistīts ar talidomīdu-aktīvo vielu ar zināmu teratogēnu iedarbību uz cilvēkiem, kas izraisa smagus dzīvībai bīstamus iedzimtus defektus.
Lenalidomīds pērtiķiem izraisīja malformācijas, kas līdzīgas tām, kas aprakstītas talidomīdam (skatīt apakšpunktu 5.3). Tādēļ ir sagaidāma lenalidomīda teratogēna iedarbība, un lenalidomīds ir kontrindicēts grūtniecības laikā (skatīt apakšpunktu 4.3).
Barošanas laiks
Tā kā nav zināms, vai lenalidomīds izdalās cilvēka mātes pienā, lenalidomīda terapijas laikā ieteicams pārtraukt zīdīšanu.
Auglība
Auglības pētījumā ar žurkām, lietojot lenalidomīda devas līdz 500 mg / kg (aptuveni 200 līdz 500 reizes lielākas par 25 mg un 10 mg devām, ko lietoja cilvēki un aprēķināja, pamatojoties uz ķermeņa virsmas laukumu), netika konstatēta nelabvēlīga ietekme uz auglība vai toksicitāte mātei.
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus -
Lenalidomīdam ir viegla vai mērena ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus. Ārstēšanas laikā ar lenalidomīdu ziņots par nogurumu, reiboni, miegainību, reiboni un neskaidru redzi. Tāpēc, vadot transportlīdzekļus vai apkalpojot mehānismus, ieteicams ievērot piesardzību.
04.8 Nevēlamās blakusparādības -
Drošības profila kopsavilkums
Nesen diagnosticēta multiplā mieloma pacientiem, kuri ārstēti ar lenalidomīdu kombinācijā ar mazām deksametazona devām
Visbiežāk novērotās (≥ 5%) nopietnās blakusparādības, lietojot lenalidomīdu kombinācijā ar mazu deksametazona devu (Rd un Rd18), salīdzinot ar melfalānu, prednizonu un talidomīdu (MPT), bija:
• Pneimonija (9,8%)
• Nieru mazspēja (ieskaitot akūtu) (6,3%)
Blakusparādības, kas biežāk novērotas, lietojot Rd vai Rd18 nekā MPT, bija: caureja (45,5%), nogurums (32,8%), muguras sāpes (32,0%), astēnija (28,2%), bezmiegs (27,6%), izsitumi (24,3%) , samazināta ēstgriba (23,1%), klepus (22,7%), drudzis (21,4%) un muskuļu spazmas (20,5%).
Nesen diagnosticēti multiplās mielomas pacienti, kuri tika ārstēti ar lenalidomīdu kombinācijā ar melfalānu un prednizonu
Visbiežāk novērotās nopietnās blakusparādības (≥ 5%), lietojot melfalānu, prednizonu un lenalidomīdu, kam seko uzturošā terapija ar lenalidomīdu (MPR + R) vai melfalānu, prednizonu un lenalidomīdu, kam seko placebo (MPR + p), salīdzinot ar melfalānu, prednizonu un placebo, kam sekoja placebo (MPp + p), bija:
• Febrilā neitropēnija (6,0%)
• Anēmija (5,3%)
Blakusparādības, kas biežāk novērotas, lietojot MPR + R vai MPR + p nekā MPp + p, bija: neitropēnija (83,3%), anēmija (70,7%), trombocitopēnija (70,0%), leikopēnija (38,8%), aizcietējums (34,0 %), caureja (33,3%), izsitumi (28,9%), drudzis (27,0%), perifēra tūska (25,0%), klepus (24,0%), samazināta ēstgriba (23,7%) un astēnija (22,0%).
Multiplā mieloma ar vismaz vienu iepriekšēju terapiju
Divos III fāzes placebo kontrolētos pētījumos 353 pacienti ar multiplo mielomu tika pakļauti kombinētai lenalidomīda / deksametazona terapijai un 351-kombinētai placebo / deksametazona terapijai.
Visnopietnākās blakusparādības, kas biežāk novērotas, lietojot lenalidomīda / deksametazona kombināciju nekā placebo / deksametazona kombinācija, bija:
• Venozā trombembolija (dziļo vēnu tromboze, plaušu embolija) (skatīt apakšpunktu 4.4)
• 4. pakāpes neitropēnija (skatīt apakšpunktu 4.4).
Blakusparādības, kas biežāk novērotas, lietojot lenalidomīdu un deksametazonu, salīdzinot ar placebo un deksametazonu, kombinējot klīniskos pētījumus par multiplo mielomu (MM-009 un MM-010), bija nogurums (43,9%), neitropēnija (42,2%), aizcietējums ( 40,5%), caureja (38,5%), muskuļu krampji (33,4%), anēmija (31,4%), trombocitopēnija (21,5%) un izsitumi (21,2%).
Mielodisplastiskie sindromi
Revlimid vispārējais drošības profils pacientiem ar mielodisplastiskiem sindromiem ir balstīts uz datiem no kopumā 286 pacientiem, kas iekļauti II un III fāzes pētījumā (skatīt 5.1. Apakšpunktu). II fāzē visi 148 pacienti tika ārstēti ar lenalidomīdu. III fāzes pētījumā 69 pacienti tika ārstēti ar 5 mg lenalidomīda, 69 pacienti tika ārstēti ar 10 mg lenalidomīda, bet 67 pacienti pētījuma dubultmaskētā fāzē saņēma placebo.
Lielākajai daļai blakusparādību bija tendence parādīties pirmo 16 lenalidomīda terapijas nedēļu laikā.
Nopietnas blakusparādības ir šādas:
• Venozā trombembolija (dziļo vēnu tromboze, plaušu embolija) (skatīt apakšpunktu 4.4)
• 3. vai 4. pakāpes neitropēnija, febrilā neitropēnija un 3. vai 4. pakāpes trombocitopēnija (skatīt apakšpunktu 4.4).
Visbiežāk novērotās blakusparādības, kas III fāzes pētījumā lenalidomīda grupās parādījās biežāk nekā kontroles grupā (placebo), bija neitropēnija (76,8%), trombocitopēnija (46,4%), caureja (34,8%), aizcietējums ( 19,6%), slikta dūša (19,6%), nieze (25,4%), izsitumi (18,1%), nogurums (18,1%) un muskuļu spazmas (16,7%).
Mantijas šūnu limfoma
Revlimid vispārējais drošības profils pacientiem ar mantijas šūnu limfomu ir balstīts uz datiem no 254 pacientiem, kas iekļauti randomizētā, kontrolētā II fāzes pētījumā MCL-002 (skatīt 5.1. Apakšpunktu).
Turklāt papildu pētījumā MCL-001 novērotās nevēlamās zāļu blakusparādības (ADR) tika iekļautas 3. tabulā.
Visbiežāk novērotās nopietnās blakusparādības pētījumā MCL-002 (ar vismaz 2 procentu punktu starpību) lenalidomīda grupā salīdzinājumā ar kontroles grupu bija:
• Neitropēnija (3,6%)
• Plaušu embolija (3,6%)
• Caureja (3,6%)
Visbiežāk novērotās blakusparādības, kas pētījumā MCL-002 lenalidomīda grupā bija sastopamas biežāk nekā kontroles grupā, bija neitropēnija (50,9%), anēmija (28,7%), caureja (22,8%), nogurums (21,0%) , aizcietējums (17,4%), drudzis (16,8%) un izsitumi (ieskaitot alerģisku dermatītu) (16,2%).
Pētījumā MCL-002 bija acīmredzams agrīnu nāves gadījumu skaita pieaugums (20 nedēļu laikā). Pacientiem ar augstu sākotnējo audzēja slodzi ir lielāks agrīnas nāves risks: 16/81 (20%) agrīnās nāves gadījumi lenalidomīda grupā un 2/28 (7%) agrīnie nāves gadījumi kontroles grupā. Līdz 52 nedēļām attiecīgie skaitļi bija 32/81 (39,5%) un 6/28 (21%) (skatīt 5.1. Apakšpunktu).
1. ārstēšanas cikla laikā 11/81 (14%) pacientu ar augstu audzēja slodzi tika atcelti no terapijas ar lenalidomīdu, salīdzinot ar 1/28 (4%) kontroles grupā. Galvenais iemesls ārstēšanas pārtraukšanai pacientiem ar augstu audzēja slodzi 1. ārstēšanas cikla laikā lenalidomīda grupā bija saistīts ar nevēlamiem notikumiem, 7/11 (64%).
Paaugstināta audzēja masa tika definēta kā vismaz viens bojājums ≥ 5 cm diametrā vai 3 bojājumi ≥ 3 cm.
Kopsavilkums nevēlamo blakusparādību saraksts
Kombinētās terapijas kopsavilkuma tabula
Blakusparādības, kas novērotas pacientiem, kuri ārstēti ar multiplo mielomu, ir uzskaitītas zemāk pēc orgānu sistēmas klasēm un biežuma. Katrā sastopamības biežuma klasē blakusparādības ir uzskaitītas to smaguma pakāpes samazināšanās secībā. Biežums ir definēts šādi: ļoti bieži (≥ 1/10); bieži (≥ 1/100,
Šī tabula tika apkopota, pamatojoties uz datiem, kas savākti multiplās mielomas pētījumos ar kombinēto terapiju. Dati nav atjaunināti, ņemot vērā ilgāku ārstēšanas ilgumu lenalidomīdu saturošās grupās, kas turpinājās līdz slimības progresēšanai, salīdzinot ar salīdzinošajām grupām pivotālajos multiplās mielomas pētījumos (skatīt 5.1. Apakšpunktu).
Blakusparādības tika ievietotas tabulas atbilstošajā kategorijā saskaņā ar augstāko sastopamības biežumu, kas novērots jebkurā no galvenajiem klīniskajiem pētījumiem.
1. tabula. Nevēlamās blakusparādības, par kurām ziņots klīniskajos pētījumos pacientiem ar multiplo mielomu, kuri tika ārstēti ar lenalidomīdu kombinācijā ar deksametazonu vai ar melfalānu un prednizonu
^ Skatīt 4.8. Sadaļu Izvēlēto blakusparādību apraksts
* Klīniskajos pētījumos pacientiem ar mielomu, kas iepriekš tika ārstēti ar lenalidomīdu / deksametazonu, tika novērots plakanšūnu ādas vēzis, salīdzinot ar kontrolgrupām
** Plakanšūnu ādas vēzis tika novērots klīniskajā pētījumā ar nesen diagnosticētiem mielomas slimniekiem ar lenalidomīdu / deksametazonu, salīdzinot ar kontrolgrupām
Kopsavilkuma tabula monoterapijai
Blakusparādības, kas novērotas pacientiem, kuri ārstēti ar mielodisplastiskiem sindromiem un mantijas šūnu limfomu, ir uzskaitītas zemāk pēc orgānu sistēmas un biežuma.
Katrā sastopamības biežuma klasē blakusparādības ir uzskaitītas to smaguma pakāpes samazināšanās secībā. Biežums ir definēts kā: ļoti bieži (≥ 1/10); bieži (≥ 1/100,
Turpmākās tabulas ir apkopotas, pamatojoties uz datiem, kas savākti galveno monoterapijas pētījumu laikā mielodisplastisko sindromu un mantijas šūnu limfomas gadījumā.
Blakusparādības tika ievietotas atbilstošajā kategorijā šajās tabulās saskaņā ar augstāko sastopamības biežumu, kas novērots jebkurā no galvenajiem klīniskajiem pētījumiem.
2. tabula. Nevēlamās blakusparādības, par kurām ziņots klīniskajos pētījumos ar lenalidomīdu ārstētiem pacientiem ar mielodisplastiskiem sindromiem
^ Skatīt 4.8. Sadaļu Izvēlēto blakusparādību apraksts
♦ Nevēlamās blakusparādības, kas novērotas kā nopietnas mielodisplastisko sindromu klīniskajos pētījumos.
≈ garastāvokļa izmaiņas tika novērotas kā bieži sastopama nopietna blakusparādība III fāzes mielodisplastisko sindromu pētījumā; netika ziņots par 3. vai 4. pakāpes nevēlamu notikumu.
Algoritms, ko izmanto, lai ievadītu zāļu aprakstu: visas zāļu blakusparādības (ADR), kas fiksētas III fāzes pētījuma algoritmā, ir iekļautas Eiropas zāļu aprakstā. Attiecībā uz šīm blakusparādībām tika veikta papildu kontrole par blakusparādību biežumu, kas iegūts ar II fāzes pētījuma algoritmu, un, ja blakusparādību biežums II fāzes pētījumā bija augstāks nekā reģistrēts III fāzes pētījumā, notikums tika iekļauts Eiropas CPR tādā biežumā, kāds novērots II fāzes pētījumā.
Mielodisplastisko sindromu gadījumā izmantotais algoritms:
• III fāzes pētījums ar mielodisplastiskiem sindromiem (dubultmaskētā drošuma populācija, atšķirība starp 5/10 mg lenalidomīda un placebo sākotnējās dozēšanas shēmas gadījumā, sastopama vismaz 2 pacientiem))
o Visas nevēlamās blakusparādības, kas novērotas ārstēšanas laikā ≥ 5% pacientu, kuri tika ārstēti ar lenalidomīdu, un vismaz 2% atšķirība starp procentiem starp lenalidomīdu un placebo
o Visas 3. vai 4. pakāpes nevēlamās blakusparādības, kas novērotas ārstēšanas laikā 1% pacientu, kuri tika ārstēti ar lenalidomīdu, un vismaz 1% procentuālā atšķirība starp lenalidomīdu un placebo
o Visas nopietnas blakusparādības, kas novērotas ārstēšanas laikā 1% pacientu, kuri tika ārstēti ar lenalidomīdu, un vismaz 1% atšķirība procentos starp lenalidomīdu un placebo
• II fāzes pētījums par mielodisplastiskiem sindromiem
o Visas nevēlamās blakusparādības, kas radušās ārstēšanas laikā ≥ 5% pacientu, kuri tika ārstēti ar lenalidomīdu. lenalidomīds
3. tabula. Nevēlamās blakusparādības, par kurām ziņots klīniskajos pētījumos pacientiem ar apvalka šūnu limfomu, kas ārstēti ar lenalidomīdu
^ Skatīt 4.8. Sadaļu Izvēlēto blakusparādību apraksts
♦ Mantijas šūnu limfomas klīniskajos pētījumos novērotās blakusparādības bija nopietnas.
Mantijas šūnu limfomas algoritms:
• II fāzes kontrolēts pētījums ar mantijas šūnu limfomu
o Visas blakusparādības, kas novērotas ārstēšanas laikā ≥ 5% pacientu lenalidomīda grupā, un vismaz 2% atšķirība starp lenalidomīda un kontroles grupas procentiem
o Visas 3. vai 4. pakāpes nevēlamās blakusparādības, kas novērotas ārstēšanas laikā ≥ 1% pacientu lenalidomīda grupā, un vismaz 1,0% atšķirība starp lenalidomīda un kontroles grupas procentiem
o Visas nopietnas blakusparādības, kas ārstēšanas laikā radās ≥ 1% pacientu lenalidomīda grupā, un vismaz 1,0% atšķirība starp lenalidomīda un kontroles grupas procentiem
• II fāzes vienas rokas pētījums ar mantijas šūnu limfomu
o Visas blakusparādības, kas novērotas ārstēšanas laikā ≥ 5% pacientu
o par visām 3. vai 4. pakāpes blakusparādībām, kas radušās ārstēšanas laikā, ziņots 2 vai vairāk pacientiem
Pēcreģistrācijas blakusparādību kopsavilkuma tabula
Papildus iepriekš minētajām blakusparādībām, kas konstatētas galvenajos klīniskajos pētījumos, ir apkopota šī tabula, pamatojoties uz datiem, kas iegūti pēcreģistrācijas periodā.
4. tabula. Blakusparādības, par kurām ziņots pēcreģistrācijas periodā pacientiem, kuri tika ārstēti ar lenalidomīdu
^ Skatīt 4.8. Sadaļu Izvēlēto blakusparādību apraksts
Izvēlēto blakusparādību apraksts
Teratogenitāte
Lenalidomīds ir strukturāli saistīts ar talidomīdu-aktīvo vielu ar zināmu teratogēnu iedarbību uz cilvēkiem, kas izraisa smagus dzīvībai bīstamus iedzimtus defektus. Lenalidomīds pērtiķiem izraisīja malformācijas, kas līdzīgas talidomīda aprakstītajām (skatīt 4.6. Un 5.3. Apakšpunktu). Lenalidomīda teratogēna iedarbība Tas ir paredzēts cilvēkiem grūtniecības laikā.
Neitropēnija un trombocitopēnija
• Nesen diagnosticēti multiplās mielomas pacienti, kuri tika ārstēti ar lenalidomīdu kombinācijā ar mazu deksametazona devu
Pacientiem ar nesen diagnosticētu multiplo mielomu lenalidomīda kombinācija ar mazu deksametazona devu ir saistīta ar samazinātu 4. pakāpes neitropēnijas biežumu (8,5% Rd un Rd18, salīdzinot ar 15% MPT). 4. pakāpes febrilā neitropēnija tika novērota reti. (0,6%, salīdzinot ar 0,7% MPT).
Pacientiem ar nesen diagnosticētu multiplo mielomu lenalidomīda kombinācija ar mazu deksametazona devu ir saistīta ar samazinātu 3. un 4. pakāpes trombocitopēnijas sastopamību (8,1% Rd un Rd18, salīdzinot ar 11% MPT).
• Nesen diagnosticēti multiplās mielomas pacienti, kuri tika ārstēti ar lenalidomīdu kombinācijā ar melfalānu un prednizonu
Pacientiem ar nesen diagnosticētu multiplo mielomu lenalidomīda kombinācija ar melfalānu un prednizonu ir saistīta ar lielāku 4. pakāpes neitropēnijas biežumu (34,1% MMR + R / MPR + p, salīdzinot ar 7,8% MPp + p). tika novērota 4. pakāpes febrilā neitropēnija (1,7% MPR + R / MPR + p, salīdzinot ar 0,0% MPp + p).
Pacientiem ar nesen diagnosticētu multiplo mielomu lenalidomīda kombinācija ar melfalānu un prednizonu ir saistīta ar lielāku 3. un 4. pakāpes trombocitopēnijas sastopamību (40,4% pacientu, kuri tika ārstēti ar MMR + R / MMR + p, salīdzinot ar 13,7% pacientu). apstrādāts ar MPp + p).
• Multiplā mieloma ar vismaz vienu iepriekšēju terapiju
Pacientiem ar multiplo mielomu lenalidomīda un deksametazona kombinācija ir saistīta ar lielāku 4. pakāpes neitropēnijas biežumu (5,1% ar lenalidomīdu / deksametazonu ārstēto pacientu, salīdzinot ar 0,6% ar placebo / deksametazonu ārstēto pacientu. 4. pakāpes febrilas neitropēnijas epizodes tika novērotas reti ( 0,6% pacientu, kuri tika ārstēti ar lenalidomīdu / deksametazonu, salīdzinot ar 0,0% pacientu, kuri tika ārstēti ar placebo / deksametazonu).
Pacientiem ar multiplo mielomu lenalidomīda un deksametazona kombinācija ir saistīta ar lielāku 3. un 4. pakāpes trombocitopēnijas biežumu (attiecīgi 9,9% un 1,4% pacientu, kuri tika ārstēti ar lenalidomīdu / deksametazonu, salīdzinot ar 2,3% un 0,0% pacientiem, kas ārstēti ar placebo / deksametazonu).
• Mielodisplastiskie sindromi
Pacientiem ar mielodisplastiskiem sindromiem lenalidomīds ir saistīts ar lielāku 3. vai 4. pakāpes neitropēnijas biežumu (74,6% ar lenalidomīdu ārstēto pacientu salīdzinājumā ar 14,9% ar placebo ārstētajiem pacientiem III fāzes pētījumā). 3. vai 4. pakāpes febrilās neitropēnijas epizodes tika novērotas 2,2% pacientu, kuri tika ārstēti ar lenalidomīdu, salīdzinot ar 0,0% pacientu, kuri tika ārstēti ar placebo. Lenalidomīds ir saistīts ar lielāku 3. vai 4. pakāpes trombocitopēnijas sastopamību (37% ar lenalidomīdu ārstētiem pacientiem salīdzinājumā ar 1,5% ar placebo ārstētiem pacientiem III fāzes pētījumā).
• Mantijas šūnu limfoma
Pacientiem ar mantijas šūnu limfomu lenalidomīds ir saistīts ar lielāku 3. vai 4. pakāpes neitropēnijas biežumu (43,7% pacientu, kuri tika ārstēti ar lenalidomīdu, salīdzinot ar 33,7% pacientu kontroles grupā III fāzes pētījumā). 3. vai 4. pakāpes febrilās neitropēnijas epizodes tika novērotas 6,0% pacientu, kuri tika ārstēti ar lenalidomīdu, salīdzinot ar 2,4% pacientu kontroles grupā.
Venozā trombembolija
Paaugstināts dziļo vēnu trombozes (DVT) un plaušu embolijas (PE) risks ir saistīts ar lenalidomīda un deksametazona lietošanu pacientiem ar multiplo mielomu un mazākā mērā pacientiem, kas ārstēti ar melfalānu un prednizonu vai kā monoterapiju pacientiem ar mielodisplastiskā un apvalka šūnu limfoma, kas ārstēta ar lenalidomīdu (skatīt 4.5. apakšpunktu). Šiem pacientiem trombozes risku var palielināt arī vienlaicīga eritropoētisko līdzekļu lietošana vai DVT anamnēzē.
Miokarda infarkts
Miokarda infarkta gadījumi novēroti pacientiem, kuri lieto lenalidomīdu, īpaši tiem, kuriem ir zināmi riska faktori.
Asiņošanas traucējumi
Asiņošanas traucējumi ir uzskaitīti dažādās klasifikācijās atkarībā no iesaistītā orgāna: asins un limfātiskās sistēmas patoloģijas; nervu sistēmas patoloģijas (intrakraniāla asiņošana); elpošanas, krūšu kurvja un videnes patoloģijas (deguna asiņošana); kuņģa -zarnu trakta patoloģijas (asiņošana no smaganām, hemoroīdi, asiņošana taisnās zarnās); nieru un urīnceļu patoloģijas (hematūrija); traumas, saindēšanās un procesuālas komplikācijas (kontūzija); asinsvadu patoloģijas (ekhimoze).
Alerģiskas reakcijas
Ir ziņots par alerģisku / paaugstinātas jutības reakciju gadījumiem. Literatūrā ir ziņots par iespējamu krustenisko reakciju starp lenalidomīdu un talidomīdu.
Smagas ādas reakcijas
Ir ziņots par SSJ un NTE gadījumiem. Pacientiem, kuriem anamnēzē bija smagi izsitumi, kas saistīti ar ārstēšanu ar talidomīdu, nedrīkst lietot lenalidomīdu.
Otrie primārie audzēji
* Klīniskajos pētījumos ar mielomas slimniekiem, kuri iepriekš tika ārstēti ar lenalidomīdu / deksametazonu, salīdzinot ar kontrolēm, kas galvenokārt sastāv no bazālo šūnu vai plakanšūnu ādas vēža.
Akūta mieloīdā leikēmija
• Multiplā mieloma
Klīniskajos pētījumos ar nesen diagnosticētu multiplo mielomu pacientiem, kuri tika ārstēti ar lenalidomīdu kombinācijā ar melfalānu, vai neilgi pēc lielas melfalāna un ASCT devas tika novēroti AML gadījumi (skatīt apakšpunktu 4.4). Šis pieaugums netika novērots klīniskajos pētījumos nesen diagnosticētiem multiplās mielomas pacientiem, kuri tika ārstēti ar lenalidomīdu kombinācijā ar mazu deksametazona devu, salīdzinot ar talidomīdu kombinācijā ar melfalānu un prednizonu.
• Mielodisplastiskie sindromi
Sākotnējie mainīgie, ieskaitot sarežģītas citoģenētiskas anomālijas un TP53 mutāciju, ir saistīti ar progresēšanu līdz AML pacientiem, kas atkarīgi no pārliešanas, ar izolētām 5q dzēšanas anomālijām (skatīt apakšpunktu 4.4). Kumulatīvais progresēšanas risks līdz AML, kas aprēķināts 2 gadu laikā, bija 13,8% pacientiem ar izolētu 5q dzēšanas anomāliju, salīdzinot ar 17,3% pacientiem ar izolētu 5q dzēšanas anomāliju un vienu "papildu citoģenētisku anomāliju", un 38,6% pacientiem ar sarežģītu kariotipu.
"Klīniskā pētījuma post-hoc analīzē, kas tika veikta ar Revlimid mielodisplastisko sindromu gadījumā, aprēķinātais 2 gadu progresēšanas ātrums līdz AML bija 27,5% IHC-p53 pozitīviem pacientiem un 3,6% IHC-p53 pozitīviem pacientiem. IHC- p53 negatīvs (p = 0,0038). IHC-p53 pozitīviem pacientiem tika novērots zemāks progresēšanas ātrums līdz AML tiem, kuri sasniedza transfūzijas neatkarības reakciju (11,1%), salīdzinot ar nereaģējošiem pacientiem (34,8%).
Aknu darbības traucējumi
Pēcreģistrācijas periodā novērotas šādas blakusparādības (biežums nav zināms): akūta aknu mazspēja un holestāze (abas dzīvībai bīstamas), toksisks hepatīts, citolītisks hepatīts, jaukts citolītiskais / holestātiskais hepatīts.
Rabdomiolīze
Ir novēroti reti rabdomiolīzes gadījumi, daži no tiem, lietojot lenalidomīdu kopā ar statīnu.
Vairogdziedzera darbības traucējumi
Ir novēroti hipotireozes un hipertireozes gadījumi (skatīt apakšpunktu 4.4 Vairogdziedzera darbības traucējumi).
Audzēja uzliesmojuma reakcija un audzēja līzes sindroms
Pētījumā MCL-002 aptuveni 10% ar lenalidomīdu ārstēto pacientu novēroja TFR, salīdzinot ar 0% kontroles grupā. Lielākā daļa notikumu notika 1. ciklā, visi tika uzskatīti par saistītiem ar ārstēšanu, un lielākā daļa ziņojumu bija 1. vai 2. pakāpe. Pacienti ar augstu MIPI diagnozes laikā un slimību, kurai raksturīga liela audzēja masa (vismaz viens bojājums, kura garums ir ≥ 7 cm) ) sākotnēji var būt TFR risks. Pētījumā MCL-002 tika ziņots par TLS vienam pacientam katrā no divām ārstēšanas grupām. MCL-001 atbalsta pētījumā aptuveni 10% pacientu bija TFR; visi ziņojumi bija 1. vai 2. pakāpes smaguma pakāpes, un visi tika uzskatīti par saistītiem ar ārstēšanu. Lielākā daļa notikumu notika 1. ciklā. Pētījumā MCL-001 netika ziņots par TLS (skatīt apakšpunktu 4.4).
Kuņģa -zarnu trakta traucējumi
Ārstēšanas ar lenalidomīdu laikā novērotas kuņģa -zarnu trakta perforācijas, kas var izraisīt septiskas komplikācijas un var būt saistītas ar letālu iznākumu.
Ziņošana par iespējamām blakusparādībām
Ir svarīgi ziņot par iespējamām blakusparādībām, kas radušās pēc zāļu reģistrācijas, jo tas ļauj nepārtraukti uzraudzīt zāļu ieguvuma un riska attiecību. Veselības aprūpes speciālistus lūdz ziņot par visām iespējamām blakusparādībām, izmantojot valsts ziņošanas sistēmu. .
04.9 Pārdozēšana -
Nav īpašas pieredzes par lenalidomīda pārdozēšanas ārstēšanu pacientiem, lai gan devas noteikšanas pētījumos daži pacienti tika pakļauti devām līdz 150 mg, un vienas devas pētījumos daži pacienti tika pakļauti devām līdz 400 mg. Šajos pētījumos devu ierobežojošai toksicitātei bija hematoloģisks raksturs. Pārdozēšanas gadījumā ieteicama atbalstoša terapija.
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS -
05.1 "Farmakodinamiskās īpašības -
Farmakoterapeitiskā grupa: citi imūnsupresanti.
ATĶ kods: L04 AX04.
Darbības mehānisms
Lenalidomīda darbības mehānisms ietver pretvēža, antiangiogēnas, eritropoētiskas un imūnmodulējošas īpašības. Konkrēti, lenalidomīds kavē specifisku asinsrades audzēja šūnu (ieskaitot MM vēža plazmas šūnas un šūnas ar 5. hromosomas dzēšanu) proliferāciju., uzlabo T šūnu mediēto imunitāti un dabiskās slepkavas (NK) šūnas un palielina NKT šūnu skaitu; kavē angioģenēzi, bloķējot endotēlija šūnu migrāciju un adhēziju un mikrokuģu veidošanos; palielina augļa hemoglobīna veidošanos ar CD34 + asinsrades cilmes šūnām un kavē monocītu proinflammatorisku citokīnu (piemēram, TNF-α un IL-6) veidošanos.
MDS ar izolētu 5q dzēšanas anomāliju ir pierādīts, ka lenalidomīds selektīvi inhibē patoloģisko klonu, palielinot Del (5q) šūnu apoptozi.
Lenalidomīds tieši saistās ar cereblonu, kas ir cullin-RING E3 ubikvitīna ligāzes enzīmu kompleksa sastāvdaļa, kas ietver dezoksiribonukleīnskābes (DNS) bojājumus saistošo proteīnu 1 (DDB1,DNS bojājumus saistošs proteīns-1), Cullin 4 (CUL4) un izkaušanas regulatoru 1 (Roc1). Lenalidomīda klātbūtnē cereblons saistās ar substrāta proteīniem Aiolos un Ikaros, kas ir limfoīdās transkripcijas faktori, izraisot to izplatību ubikvitinācijā un pēc tam noārdīšanos, kā rezultātā rodas citotoksiska un imūnmodulējoša iedarbība.
Klīniskā efektivitāte un drošība
Lenalidomīds tika novērtēts divos III fāzes pētījumos ar nesen diagnosticētu multiplo mielomu un divos III fāzes pētījumos ar recidivējošu ugunsizturīgu multiplo mielomu, kā aprakstīts turpmāk.
Es Un L vai m nesen diagnosticēts daudzkārtējs
Lenalidomīds kombinācijā ar deksametazonu pacientiem, kuri nav piemēroti cilmes šūnu transplantācijai
Lenalidomīda efektivitāte un drošība tika novērtēta daudzcentru, nejaušinātā, atklātā, trīs roku III fāzes pētījumā (MM-020) pacientiem, kuri bija 65 gadus veci vai vecāki, vai, ja jaunāki par 65 gadiem, kuri nebija piemēroti cilmes šūnu transplantācijai pacienta lēmuma dēļ vai cilmes šūnu transplantācijas nepieejamības dēļ izmaksu vai citu iemeslu dēļ. Pētījumā (MM-020) lenalidomīdu un deksametazonu (Rd) salīdzināja 2 dažādus ārstēšanas ilgumus (piemēram, līdz slimības progresēšanai [Rd grupa] vai līdz astoņpadsmit 28 dienu cikliem [72 nedēļas, Rd18 grupa]) ar melfalānu, prednizonu un talidomīds (MPT) līdz divpadsmit 42 dienu (72 nedēļu) cikliem. Pacienti tika randomizēti (1: 1: 1) vienā no 3 ārstēšanas grupām. Randomizējot, pacienti tika stratificēti pēc vecuma (≤ 75 gadi vs> 75 gadi), stadijas (ISS I un II posms pret III stadiju) un valsts.
Pacienti Rd un Rd18 grupās saņēma 25 mg lenalidomīda vienu reizi dienā 28 dienu ciklu 1. līdz 21. dienā saskaņā ar protokola grupu. 40 mg deksametazona ievadīja vienu reizi dienā katra 28 dienu ārstēšanas cikla 1., 8., 15. un 22. dienā. Sākotnējā deva un režīms Rd un Rd18 tika pielāgoti vecumam un nieru funkcijai (skatīt 4.2. Apakšpunktu). Pacienti> 75 gadus veci saņēma deksametazona devu 20 mg vienu reizi dienā katras 28 dienas 1., 8., 15. un 22. dienā. ārstēšanas cikls Visiem pacientiem pētījuma laikā tika veikta antikoagulantu profilakse (zemas molekulmasas heparīns, varfarīns, heparīns, neliela aspirīna deva).
Primārais efektivitātes parametrs pētījumā bija dzīvildze bez slimības progresēšanas (Progresēšana Bezmaksas izdzīvošana, PFS). Kopumā pētījumā tika iekļauti 1623 pacienti: 535 pacienti tika randomizēti pēc Rd, 541 pacients tika randomizēts pēc Rd18 un 547 pacienti tika randomizēti MPT. Pacientu demogrāfiskās un ar slimībām saistītās īpašības sākotnēji bija labi līdzsvarotas visās 3 grupās.Kopumā pētāmajiem bija progresējoša slimība: no visiem pētījuma dalībniekiem 41% bija ISS III stadijā, 9% bija smagi nieru darbības traucējumi (kreatinīna klīrenss [CLcr]).
Atjauninātajā PFS, PFS2 un vispārējās dzīvildzes (OS) analīzē, izmantojot 2014. gada 3. marta beigu datumu, kur visu izdzīvojušo pacientu vidējais novērošanas laiks bija 45,5 mēneši, pētījuma rezultāti ir parādīti 5. tabula.
5. tabula. Kopējo efektivitātes datu kopsavilkums
AMT = anti-mielomas terapija; CI = ticamības intervāls; CR = pilnīga reakcija; d = mazas deksametazona devas; HR = bīstamības koeficients; IMWG = Starptautiskā mielomas darba grupa; IRAC = Neatkarīgas atbildes sprieduma komiteja; M = melfalāns; max = maksimums; min = minimums; NS = nav novērtējams; OS = kopējā izdzīvošana; P = prednizons; PFS = dzīvildze bez progresēšanas; PR = daļēja reakcija; R = lenalidomīds; Rd = Rd ievadīts līdz dokumentētai slimības progresēšanai; Rd18 = Rd ievadīts ≥ 18 ciklus; SE = standarta kļūda; T = talidomīds; VGPR = optimāla daļēja reakcija; vs = pret.
a Mediāna ir balstīta uz Kaplana-Meiera novērtējumu.
b 95% TI par vidējo.
c Pamatojoties uz Cox proporcionālo apdraudējumu modeli, kurā salīdzinātas bīstamības funkcijas, kas saistītas ar norādītajām apstrādes grupām.
d p vērtība ir balstīta uz nenoteiktu žurnāla ranga testu par Kaplan-Meiera līkņu atšķirībām starp norādītajām ārstēšanas grupām.
e Izpētes parametrs (PFS2)
f Mediāna ir vienfaktoru statistika bez saīsinājuma korekcijas.
g Uzlabots novērtētās atbildes novērtējums pētījuma ārstēšanas fāzē (katras atbildes kategorijas definīcijai Datu beigu datums = 2013. gada 24. maijs).
h Izslēgšanas datums = 2013. gada 24. maijs
Lenalidomīds kombinācijā ar melfalānu un prednizonu, kam seko uzturošā monoterapija pacienti, kuri nav piemēroti transplantācijai
Lenalidomīda (MPR) drošums un efektivitāte tika novērtēta daudzcentru, randomizētā, dubultmaskētā, 3-roku III fāzes pētījumā (MM-015) 65 gadus veciem un vecākiem pacientiem ar kreatinīna līmeni serumā. 75 gadi) un stadijā (ISS I un II posms pret III posmu).
Šajā pētījumā tika pētīta MMR kombinētās terapijas izmantošana (melfalāns 0,18 mg / kg iekšķīgi atkārtotu 28 dienu ciklu 1. – 4. Dienā; prednizons 2 mg / kg iekšķīgi atkārtotu 28 dienu ciklu 1. – 4. Dienā; un lenalidomīds 10 mg / dienā iekšķīgi atkārtotu 28 dienu ciklu 1.-21. dienā), indukcijas terapijai-ne vairāk kā 9 cikli. Pacienti, kuri bija pabeiguši 9 ciklus vai nevarēja pabeigt 9 ciklus nepanesības dēļ, pārgāja uz uzturošā monoterapija, kas tika sākta ar 10 mg lenalidomīda iekšķīgi atkārtotu 28 dienu ciklu 1.-21. dienā, līdz slimība progresēja
Pētījuma primārais efektivitātes parametrs bija dzīvildze bez slimības progresēšanas (PFS). Kopumā pētījumā tika iekļauti 459 pacienti: 152 pacienti pēc nejaušības principa pēc MMR + R, 153 pacienti pēc nejaušības principa pēc MMR + p un 154 pacienti pēc nejaušības principa pēc MPp + p . Sākotnēji pacientu demogrāfiskās un ar slimībām saistītās īpašības bija labi līdzsvarotas visās 3 grupās; jo īpaši aptuveni 50% pacientu, kas tika iekļauti katrā grupā, bija šādas pazīmes: ISS III stadija un kreatinīna klīrenss
"PFS, PFS2 un OS analīzē, izmantojot 2013. gada aprīļa beigu datumu, kura vidējais novērošanas laiks visiem izdzīvojušajiem bija 62,4 mēneši, pētījuma rezultāti ir parādīti 6. tabulā.
6. tabula. Kopējo efektivitātes datu kopsavilkums
CI = ticamības intervāls; CR = pilnīga reakcija; HR = bīstamības koeficients; M = melfalāns; NS = nav novērtējams; OS = kopējā izdzīvošana; p = placebo; P = prednizons;
PD = progresējoša slimība; PR = daļēja reakcija; R = lenalidomīds; SD = stabila slimība; VGPR = optimāla daļēja reakcija.
a Mediāna ir balstīta uz Kaplana-Meiera novērtējumu.
¤ PFS2 (izpētes parametrs) visiem pacientiem (ITT) tika definēts kā laiks no randomizācijas līdz trešās līnijas anti-mielomas terapijas uzsākšanai vai nāve jebkura iemesla dēļ visiem randomizētajiem pacientiem
Atbalstoši pētījumi ar nesen diagnosticētu multiplo mielomu
Atklāts, randomizēts, daudzcentru III fāzes pētījums (ECOG E4A03) tika veikts 445 pacientiem ar nesen diagnosticētu multiplo mielomu; 222 pacienti tika randomizēti lenalidomīda / mazas deksametazona devas grupā, bet 223 pacienti tika izvēlēti pēc lenalidomīda / standarta deksametazona grupas. Pacienti, kuri tika randomizēti lenalidomīda / deksametazona standarta devas grupā, saņēma lenalidomīdu 25 mg dienā 1. līdz 21. dienā, ik pēc 28 dienām, kā arī deksametazonu 40 mg dienā 1. līdz 4., 9. līdz 12. un 17. dienā 20, ik pēc 28 dienām, pirmajiem četriem cikliem. Pacienti, kuri tika randomizēti lenalidomīda / mazas deksametazona devas grupai, saņēma lenalidomīdu 25 mg dienā 1. līdz 21. dienā, ik pēc 28 dienām, kā arī deksametazona mazas devas 40 mg dienā 1., 8., 15. un 22. dienā, katra 28 dienas . Lenalidomīda / mazas deksametazona devas grupā 20 pacientiem (9,1%) tika pārtraukta vismaz viena deva, salīdzinot ar 65 pacientiem (29,3%) lenalidomīda / standarta deksametazona grupā.
Post-hoc analīzē zemākā mirstība tika novērota 6,8% lenalidomīda / deksametazona devas grupā (15/220), salīdzinot ar 19,3% (43/223) lenalidomīda / devas deksametazona standarta devu. mielomas pacientu populācija, ar vidējo novērošanu 72,3 nedēļas.
Tomēr, ilgstoši novērojot, kopējās dzīvildzes atšķirībām par labu mazām lenalidomīda / deksametazona devām ir tendence samazināties.
Multiplā mieloma ar vismaz vienu iepriekšēju terapiju
Lenalidomīda efektivitāte un drošība tika novērtēta divos III fāzes daudzcentru, randomizētos, dubultmaskētos, placebo kontrolētos, paralēlas grupas (MM-009 un MM-010) pētījumos par lenalidomīdu kombinācijā ar deksametazonu, salīdzinot ar deksametazona monoterapiju iepriekš ārstētiem pacientiem ar multiplā mieloma. No 353 pacientiem, kas tika iekļauti pētījumos MM-009 un MM-010, kuri tika ārstēti ar lenalidomīdu / deksametazonu, 45,6% bija 65 gadus veci vai vecāki. No 704 pacientiem, kas tika novērtēti pētījumos MM-009 un MM-010, 44,6% bija 65 gadus veci vai vecāki.
Abos pētījumos pacienti no lenalidomīda / deksametazona (len / des) grupas saņēma 25 mg lenalidomīda iekšķīgi vienu reizi dienā 1. līdz 21. dienā un identiska izskata placebo kapsulu vienu reizi dienā. No 22. līdz 28. dienai no katra 28 dienu cikla. placebo / deksametazona (placebo / des) grupa paņēma 1 kapsulu placebo katra 28 dienu cikla 1. līdz 28. dienā. Abas grupas pacienti lietoja 40 mg deksametazona iekšķīgi vienu reizi dienā 1. līdz 4., 9. līdz 12. dienā un
17 līdz 20 no katra 28 dienu cikla pirmajos 4 terapijas ciklos. Pēc pirmajiem 4 terapijas kursiem deksametazona deva tika samazināta līdz 40 mg vienu reizi dienā katra 28 dienu cikla 1. līdz 4. dienā. Abos pētījumos ārstēšana bija jāturpina līdz slimības progresēšanai. Abos pētījumos bija atļauts pielāgot devu. pamatojoties uz klīniskajiem un laboratorijas rezultātiem.
Abos pētījumos primārais efektivitātes parametrs bija laiks līdz slimības progresēšanai (TTP, laiks progresēšanai). Kopumā pētījumā MM-009 tika novērtēti 353 pacienti: 177 lenalidomīda / deksametazona grupā un 176 pacienti placebo / deksametazona grupā. Kopumā pētījumā MM-010 tika novērtēts 351 pacients: 176-lenalidomīda / deksametazona grupā un 175-placebo / deksametazona grupā.
Abos pētījumos lenalidomīda / deksametazona un placebo / deksametazona grupām bija salīdzināmas sākotnējās demogrāfiskās un ar slimību saistītās īpašības. Abām pacientu grupām vidējais vecums bija 63 gadi, un vīriešu un sieviešu pacientu attiecība bija salīdzināma.Austrumu kooperatīvā onkoloģijas grupa), gan iepriekšējo terapiju skaits, gan veids abās grupās bija salīdzināmi.
Analīzes pagaidu iepriekš plānots abiem pētījumiem, parādīja, ka lenalidomīda / deksametazona kombinētā terapija uzrādīja statistiski nozīmīgu uzlabojumu (p
Paplašināta novērošanas efektivitātes analīze tika veikta vidēji 130,7 nedēļas. 7. tabulā parādīti pēcpārbaudes efektivitātes analīzes rezultāti-kopīgi pētījumi MM-009 un MM-010.
Šajā apvienotajā pagarinātajā novērošanas analīzē vidējais TTP bija 60,1 nedēļa (95% TI: 44,3, 73,1) pacientiem, kuri tika ārstēti ar lenalidomīdu / deksametazonu (N = 353), salīdzinot ar vidēji 20, 1 nedēļu (95% TI: 17,7, 20,3) pacientiem, kas ārstēti ar placebo / deksametazonu (N = 351). Vidējā dzīvildze bez progresēšanas bija 48,1 nedēļa (95% TI: 36,4, 62,1) pacientiem, kuri tika ārstēti ar lenalidomīdu / deksametazonu, salīdzinot ar vidējo laiku 20,0 nedēļas (95% TI: 16, 1, 20,1) pacientiem, kuri tika ārstēti ar placebo / deksametazonu . Vidējais ārstēšanas ilgums bija 44,0 nedēļas (min: 0,1, maksimums: 254,9) lenalidomīdam / deksametazonam un 23,1 nedēļa (min: 0,3, maks .: 238,1) placebo / deksametazonam. Abos pētījumos pilnīgas atbildes reakcijas (CR, pilnīga atbilde), daļēja reakcija (PR, daļēja reakcija) un kopējā atbildes reakcija (CR + PR) lenalidomīda / deksametazona grupā saglabājās ievērojami augstāka nekā deksametazona / placebo grupā. Kopējā pētījuma vidējā kopējā dzīvildze kopīgo pētījumu paplašinātajā novērošanas analīzē pacientiem, kuri tika ārstēti ar lenalidomīdu / deksametazonu, ir 164,3 nedēļas (95% TI: 145,1, 192,6), salīdzinot ar 136,4 nedēļām (95% TI: 113,1, 161,7) pacientiem, kuri ārstēti ar neskatoties uz to, ka 170 no 351 pacientam, kuri tika randomizēti placebo / deksametazona terapijai, pēc slimības progresēšanas vai pēc akluma saņēma lenalidomīda terapiju, apvienotā kopējā dzīvildzes analīze parādīja statistiski nozīmīgu izdzīvošanas priekšrocību lenalidomīda / deksametazona grupai salīdzinājumā ar placebo. / deksametazona grupa (bīstamības attiecība = 0,833, 95% TI = [0,687, 1,009], p = 0,045).
7. tabula. Efektivitātes analīžu rezultātu kopsavilkums pagarinātās novērošanas beigu datumā-Kopīgie pētījumi MM-009 un MM-010 (attiecīgie beigu datumi: 2008. gada 23. jūlijs un 2008. gada 2. marts)
a: Divpusēja vienfaktoru analīze, kurā salīdzinātas izdzīvošanas līknes starp ārstēšanas grupām. b: divpusējs hī kvadrāta tests ar nepārtrauktības korekciju.
Mielodisplastiskie sindromi
Divos pamatpētījumos lenalidomīda efektivitāte un drošība tika novērtēta pacientiem ar transfūziju atkarīgu anēmiju, kam bija zems vai vidēja riska 1 mielodisplastiskais sindroms, kas saistīts ar 5q dzēšanas citoģenētisko anomāliju ar vai bez citām citoģenētiskām novirzēm. , randomizēts, dubultmaskēts, placebo kontrolēts, 3-roku, divu devu perorāls lenalidomīda (10 mg un 5 mg) un placebo pētījums (MDS-004); un II fāzes daudzcentru, viena grupa, atklāta, lenalidomīds (10 mg) (MDS-003).
Turpmāk sniegtie rezultāti atspoguļo ārstēšanās nodomu populāciju, kas pētīta MDS-003 un MDS-004; apakšpopulācijas ar izolētu 5q dzēšanu rezultāti tiek parādīti atsevišķi (apstiprināto indikāciju skatīt 4.1. sadaļā).
Pētījumā MDS-004, kurā 205 pacienti tika vienlīdz nejauši izvēlēti ārstēšanai ar 10 mg, 5 mg vai 5 mg lenalidomīda vai placebo, primārā efektivitātes analīze sastāvēja no transfūzijas neatkarības reakcijas rādītāju salīdzināšanas 10 mg lenalidomīda un 5 mg grupās, salīdzinot ar placebo. (dubultmaskētā fāze no 16 līdz 52 nedēļām un atklāta fāze līdz 156 nedēļām). Pacientiem, kuriem pēc 16 nedēļām neuzrādījās vismaz viegla eritroidā reakcija, ārstēšana tika pārtraukta. vismaz viegla eritroīdā atbildes reakcija varētu turpināt terapiju līdz eritroidu recidīvam, slimības progresēšanai vai nepieņemamai toksicitātei. pēc 16 ārstēšanas nedēļām viņiem tika atļauts pāriet no placebo uz 5 mg lenalidomīda vai turpināt ārstēšana ar lielāku lenalidomīda devu (no 5 mg līdz 10 mg).
Pētījumā MDS-003, kurā 148 pacienti tika ārstēti ar lenalidomīdu 10 mg devā, primārā efektivitātes analīze ietvēra lenalidomīda terapijas efektivitātes novērtējumu, lai panāktu asinsrades uzlabošanos pacientiem ar mielodisplastiskiem sindromiem. Zems vai vidējs risks 1.
8. tabula. Efektivitātes rezultātu kopsavilkums-MDS-004 (dubultmaskētā fāze) un MDS-003, pacienti ar mērķi ārstēties
† Pacienti, kuri 28 dienu cikla 21. dienā tika ārstēti ar 10 mg lenalidomīda
†† Pacienti, kas 28 dienu ciklā tika ārstēti ar 5 mg lenalidomīda
* Lielākā daļa pacientu placebo grupā pārtrauca dubultmaskēto terapiju efektivitātes trūkuma dēļ pēc 16 ārstēšanas nedēļām, pirms sākās atklātā fāze
#Saistīts ar Hgb palielināšanos par ≥ 1 g / dL
∞ Nav sasniegts (mediāna netika sasniegta)
Pētījumā MDS-004 ievērojami lielāka daļa pacientu ar mielodisplastiskiem sindromiem sasniedza primāro transfūzijas neatkarību (> 182 dienas), lietojot 10 mg lenalidomīda, salīdzinot ar placebo (55,1% pret 6,0%). .
Del (5q) izolēts un ārstēts ar 10 mg lenalidomīda, 27 pacienti (57,4%) sasniedza neatkarību no eritrocītu pārliešanas.
Vidējais laiks līdz transfūzijas neatkarībai 10 mg lenalidomīda grupā bija 4,6 nedēļas. Vidējais transfūzijas neatkarības ilgums netika sasniegts nevienā no ārstēšanas grupām, bet paredzams, ka ārstētiem pacientiem tas pārsniegs 2 gadus. Ar lenalidomīdu. Hemoglobīns (Hgb) no sākotnējā stāvokļa 10 mg grupā bija 6,4 g / dl.
Papildu pētījuma parametri ietvēra citoģenētisko reakciju (lielas un nelielas citoģenētiskas atbildes reakcijas tika novērotas attiecīgi 30,0% un 24,0% pacientu 10 mg grupā), ar veselību saistītās dzīves kvalitātes (HRQoL) novērtējumu un progresēšanu līdz akūtai mieloleikozei. Citoģenētiskās atbildes un HRQoL rezultāti saskanēja ar primārā parametra rezultātiem un par labu ārstēšanai ar lenalidomīdu salīdzinājumā ar placebo.
Pētījumā MDS-003 liela daļa pacientu ar mielodisplastiskiem sindromiem sasniedza transfūzijas neatkarību (> 182 dienas), lietojot 10 mg lenalidomīda (58,1%). Vidējais laiks līdz transfūzijas neatkarībai bija 4,1 nedēļa. Transfūzijas neatkarības vidējais ilgums bija 114,4 nedēļas. Hemoglobīna (Hgb) pieauguma vidējais rādītājs bija 5,6 g / dl.
Lielas un nelielas citoģenētiskās reakcijas tika novērotas attiecīgi 40,9% un 30,7% pacientu.
Liela daļa pacientu, kas iesaistīti MDS-003 (72,9%) un MDS-004 (52,7%), iepriekš bija ārstēti ar eritropoēzi stimulējošiem līdzekļiem.
Mantijas šūnu limfoma
Lenalidomīda efektivitāte un drošība pacientiem ar apvalka šūnu limfomu tika novērtēta II fāzes, daudzcentru, randomizētā, atklātā pētījumā, salīdzinot ar pētnieka izvēlēto monoterapiju pacientiem, kuri nebija izturīgi pret pēdējo shēmu vai kuriem bija viens līdz trīs recidīvi ( Pētījums MCL-002).
Tika iekļauti vismaz 18 gadus veci pacienti ar histoloģiski apstiprinātu mantijas šūnu limfomu un izmērāmu slimību CT. Pacientiem bija jāsaņem atbilstoša iepriekšēja ārstēšana ar vismaz vienu iepriekšēju kombinētās ķīmijterapijas shēmu. Turklāt pētījuma iekļaušanas laikā pacientiem bija jābūt nepiemērotiem intensīvai ķīmijterapijai un / vai transplantācijai. Pacienti tika randomizēti 2: 1 pret lenalidomīdu vai kontroles grupu. Pētnieka izvēle par ārstēšanu tika nolemta agrāk. Randomizācija un sastāvēja no monoterapijas ar hlorambucilu, citarabīnu, rituksimabu, fludarabīnu vai gemcitabīnu.
Lenalidomīdu lietoja iekšķīgi 25 mg devā vienu reizi dienā pirmajās 21 dienās (no G1 līdz G21) atkārtotos 28 dienu ciklos līdz progresēšanai vai nepieņemamai toksicitātei. Pacientiem ar vidēji smagiem nieru darbības traucējumiem bija jāsaņem mazāka lenalidomīda sākuma deva (10 mg dienā) ar tādu pašu shēmu.
Sākotnējie demogrāfiskie rādītāji bija salīdzināmi starp lenalidomīdu un kontroles grupām. Abām pacientu grupām bija vidējais vecums 68,5 gadi, ar salīdzināmu vīriešu un sieviešu attiecību. Gan ECOG veiktspējas statuss, gan iepriekšējo terapiju skaits bija salīdzināms abās grupās.
MCL-002 primārais efektivitātes parametrs bija dzīvildze bez slimības progresēšanas (PFS).
Efektivitātes rezultātus paredzētās ārstēšanas (ITT) populācijai novērtēja Neatkarīgā pārskata komisija (Neatkarīga pārskatīšanas komiteja, IRC) un ir parādīti tabulā zemāk.
9. tabula. Efektivitātes rezultātu kopsavilkums-pētījums MCL-002, populācija, kas paredzēta ārstēšanai
CI = ticamības intervāls; CRR = pilnīgas atbildes līmenis; CR = pilnīga reakcija; CRu = pilnīga atbilde nav apstiprināta; DMC = datu uzraudzības komiteja; ITT = nodoms ārstēt; HR = bīstamības koeficients; KM = Kaplans-Meiers; MIPI = mantijas šūnu limfomas starptautiskais prognozes indekss; NP = nav būtisks; ORR = kopējais reakcijas līmenis; PD = progresējoša slimība; PFS = dzīvildze bez progresēšanas; PR = daļēja reakcija; SCT = cilmes šūnu transplantācija; SD = stabila slimība; SE = standarta kļūda.
a Mediāna ir balstīta uz KM novērtējumu.
b Diapazons tika aprēķināts kā 95% TI attiecībā uz vidējo izdzīvošanas laiku.
e Vidējais un mediāna ir vienfaktoru statistika bez saīsinājuma korekcijas.
d Stratifikācijas mainīgie lielumi ietvēra laiku no diagnozes noteikšanas līdz pirmajai devai (
e Secīgā testēšana tika balstīta uz vidējo svērto žurnāla ranga testa statistikas rādītāju, izmantojot neapstrādātas žurnāla ranga testu izlases lieluma palielināšanai un neapstrādātas žurnāla ranga testu no primārās analīzes. Svari ir balstīti uz notikumiem, kas novēroti RCD trešās sanāksmes datumā, un ir balstīti uz atšķirību starp novērotajiem notikumiem un notikumiem, kas gaidāmi primārās analīzes laikā.
Tiek parādīts saistītais secīgais HR un atbilstošais 95% TI.
Pētījumā MCL-002 ITT populācijā kopumā bija acīmredzams nāves gadījumu skaita pieaugums 20 nedēļu laikā lenalidomīda grupā, 22/170 (13%), salīdzinot ar 6/84 (7%) kontroles grupā. Pacientiem ar augstu audzēja slodzi attiecīgie skaitļi bija 16/81 (20%) un 2/28 (7%) (skatīt apakšpunktu 4.4).
Pediatriskā populācija
Eiropas Zāļu aģentūra ir atbrīvojusi no pienākuma iesniegt pētījumu rezultātus ar Revlimid visās bērnu populācijas apakšgrupās multiplās mielomas, mielodisplastisko sindromu un mantijas šūnu limfomas gadījumā (informāciju par lietošanu bērniem skatīt 4.2. Apakšpunktā).
05.2 "Farmakokinētiskās īpašības -
Lenalidomīdam ir asimetrisks oglekļa atoms; tāpēc tā molekula pastāv optiski aktīvās formās S (-) un R (+). Lenalidomīdu ražo kā racēmisku maisījumu. Lenalidomīds parasti labāk šķīst organiskos šķīdinātājos, bet maksimāli šķīst 0,1 N HCl šķīdumā.
Uzsūkšanās
Veseliem brīvprātīgajiem tukšā dūšā pēc perorālas lietošanas lenalidomīds ātri uzsūcas, sasniedzot maksimālo koncentrāciju plazmā no 0,5 līdz 2 stundām pēc devas. Gan pacientiem, gan veseliem brīvprātīgajiem maksimālā koncentrācija (Cmax) un l "laukums zem koncentrācijas un laika līknes ( AUC) proporcionāli palielinās, palielinot devu. Atkārtotas devas neizraisa būtisku zāļu uzkrāšanos. Plazmā lenalidomīda S- un R-enantiomēru relatīvā koncentrācija ir attiecīgi aptuveni 56% un 44%.
Vienlaicīga augstas kaloriju un tauku satura maltītes lietošana veseliem brīvprātīgajiem samazina uzsūkšanās apjomu, kā rezultātā laukums zem AUC samazinās par aptuveni 20% un plazmas Cmax samazinās par 50%. Tomēr galvenajos multiplās mielomas un mielodisplastisko sindromu reģistrācijas pētījumos, kuros tika noskaidrota lenalidomīda drošība un efektivitāte, zāles tika ievadītas, neņemot vērā uzturu. Tādēļ lenalidomīdu var lietot kopā ar ēdienu vai bez tā.
Populācijas farmakokinētikas analīzes liecina, ka perorālā lenalidomīda uzsūkšanās ātrums pacientiem ar multiplo mielomu, pacientiem ar mielodisplastiskiem sindromiem un mantijas šūnu limfomu ir līdzīgs.
Izplatīšana
In vitro, 14C iezīmētais lenalidomīds vāji saistās ar plazmas olbaltumvielām, vidējā vērtība attiecīgi 23% un 29% pacientiem ar multiplo mielomu un veseliem brīvprātīgajiem.
Lenalidomīds atrodas spermā (
Biotransformācija un eliminācija
Veikto cilvēku metabolisma pētījumu rezultāti in vitro norāda, ka lenalidomīdu nemetabolizē citohroma P450 enzīmi, kas liecina, ka lenalidomīda lietošana kopā ar zālēm, kas inhibē citohroma P450 enzīmus, maz ticams, ka izraisīs metabolisku zāļu mijiedarbību cilvēkiem. in vitro norāda, ka lenalidomīdam nav inhibējošas ietekmes uz CYP1A2, CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A vai UGT1A1. Tādēļ maz ticams, ka lenalidomīds izraisīs klīniski nozīmīgu zāļu mijiedarbību, ja to lieto vienlaikus ar šo enzīmu substrātiem.
Izglītība in vitro norāda, ka lenalidomīds nav cilvēka krūts vēža rezistences proteīna (BCRP), vairāku zāļu rezistences olbaltumvielu (MRP) transportētāju MRP1, MRP2 vai MRP3 substrāts, organisko anjonu transportētāji (OAT) OAT1 un OAT3, polipeptīdu organisko anjonu transportētājs (OATP) OATP1B1, organisks katjonu transportētāji (AZT) OCT1 un OCT2, zāļu un toksīnu ekstrūzijas proteīns (MATE) MATE1 un jauni organisko katjonu transportētāji (OCTN) OCTN1 un OCTN2.
Izglītība in vitro norāda, ka lenalidomīdam nav inhibējošas ietekmes uz cilvēka žults sāls eksporta sūkni (BSEP), BCRP, MRP2, OAT1, OAT3, OATP1B1, OATP1B3 un OCT2.
Lielākā daļa lenalidomīda tiek izvadīta ar urīnu. Nieru izdalīšanās ietekme uz kopējo klīrensu indivīdiem ar normālu nieru darbību bija 90%, bet 4% lenalidomīda tika izvadīti ar izkārnījumiem.
Lenalidomīds tiek vāji metabolizēts, tāpēc 82% devas neizmainītā veidā izdalās ar urīnu.Hidroksillenalidomīds un N-acetil-lenalidomīds veido attiecīgi 4,59% un 1,83% no izdalītās devas. Lenalidomīda nieru klīrenss pārsniedz glomerulārās filtrācijas ātrumu, tāpēc vismaz zināmā mērā tas tiek aktīvi izdalīts.
Lietojot devas no 5 līdz 25 mg dienā, pusperiods plazmā veseliem brīvprātīgajiem ir aptuveni 3 stundas, bet pacientiem ar multiplo mielomu, mielodisplastiskiem sindromiem vai mantijas šūnu limfomu-no 3 līdz 5 stundām.
Gados vecāki pacienti
Nav veikti īpaši klīniskie pētījumi, lai novērtētu lenalidomīda farmakokinētiku gados vecākiem pacientiem. Populācijas farmakokinētikas analīzē tika iekļauti pacienti vecumā no 39 līdz 85 gadiem un norādīts, ka vecums neietekmē lenalidomīda klīrensu (koncentrāciju plazmā). Tā kā gados vecākiem pacientiem, visticamāk, ir pavājināta nieru darbība, ieteicams ievērot piesardzību, izvēloties devu. piesardzības nolūkos ieteicams kontrolēt nieru darbību.
Nieru mazspēja
Lenalidomīda farmakokinētika tika pētīta pacientiem ar nieru mazspēju, ko izraisījušas ļaundabīgas slimības. Šajā pētījumā nieru funkcijas klasificēšanai tika izmantotas divas metodes: kreatinīna klīrenss urīnā, kas izmērīts 24 stundu laikā, un kreatinīna klīrenss, kas aprēķināts pēc Coccoft-Gault formulas. Rezultāti liecina, ka, samazinoties nieru funkcijai (lenalidomīda eliminācijas pusperiods palielinājās no aptuveni 3,5 stundas pacientiem ar kreatinīna klīrensu> 50 ml / min līdz vairāk nekā 9 stundām pacientiem ar nieru darbības traucējumiem
Aknu mazspēja
Populācijas farmakokinētikas analīzē tika iekļauti pacienti ar vieglu aknu mazspēju (N = 16, kopējais bilirubīns> 1 līdz ≤ 1,5 x ULN (augšējā normas robeža) vai ASAT> ULN) un norādīts, ka "viegla aknu mazspēja neietekmē klīrensu (koncentrācija plazmā)" par lenalidomīdu Nav pieejami dati par pacientiem ar vidēji smagiem vai smagiem aknu darbības traucējumiem.
Citi raksturīgie faktori
Populācijas farmakokinētikas analīzes liecina, ka ķermeņa svaram (33-135 kg), dzimumam, rasei un ļaundabīga hematoloģiska audzēja veidam (MM, MDS vai MCL) nav klīniski nozīmīgas ietekmes uz lenalidomīda klīrensu pieaugušiem pacientiem.
05.3 Preklīniskie drošības dati -
Tika veikts embrija un augļa attīstības pētījums pērtiķiem, kuri tika ārstēti ar lenalidomīdu devās no 0,5 līdz 4 mg / kg dienā. Šī pētījuma rezultāti liecināja, ka lenalidomīds izraisa ārējas anomālijas, tai skaitā neatklātas anālās atveres un augšējo un apakšējo ekstremitāšu (izliektas, saīsinātas, nepareizi veidotas, malrotētas un / vai neesošas ekstremitāšu daļas, oligo un / vai polidaktīlijas) malformācijas pērtiķu pēctečiem, kuri šo narkotiku saņēma grūtniecības laikā.
Atsevišķiem augļiem novērota arī atšķirīga viscerālā iedarbība (krāsas izmaiņas, sarkani perēkļi dažādos orgānos, maza bezkrāsaina masa virs atrioventrikulārā vārsta, mazs žultspūslis, nepareizi veidota diafragma).
Lenalidomīdam ir potenciāls akūtas toksicitātes risks; grauzējiem minimālās letālās devas pēc iekšķīgas lietošanas bija> 2000 mg / kg dienā. Atkārtota 75, 150 un 300 mg / kg / dienā perorāla lietošana līdz 26 nedēļām izraisīja atgriezenisku, ar ārstēšanu saistītu nieru iegurņa mineralizācijas palielināšanos žurkām, galvenokārt mātītēm, visos devu līmeņos. Novērojamas nelabvēlīgas ietekmes līmenis (NOAEL, nav novērots nelabvēlīgas ietekmes līmenis) tika uzskatīts par mazāku par 75 mg / kg / dienā un ir aptuveni 25 reizes lielāks nekā ikdienas iedarbība uz cilvēkiem, pamatojoties uz AUC vērtībām. Pērtiķiem atkārtota 4 un 6 mg / kg / dienā perorāla lietošana līdz 20 nedēļām izraisīja ievērojamu mirstību un toksicitāti (izteikts svara zudums, samazināts balto asins šūnu skaits, sarkano asins šūnu un trombocītu skaits, asiņošana vairākos orgānos, iekaisums). kuņģa -zarnu trakts, limfātisko audu un kaulu smadzeņu atrofija). Arī pērtiķiem atkārtota perorāla 1 un 2 mg / kg / dienā lietošana laikposmā līdz 1 gadam izraisīja atgriezeniskas izmaiņas kaulu smadzeņu šūnā, nelielu mielo-eritroīdo šūnu attiecības samazināšanos un aizkrūts dziedzera atrofiju. Tika novērots neliels leikocītu skaita samazinājums līdz 1 mg / kg dienā, kas atbilst aptuveni vienādai devai cilvēkiem, pamatojoties uz AUC salīdzinājumu.
Veikti mutagenitātes pētījumi in vitro (baktēriju mutācija, cilvēka limfocīti, peles limfoma, pārvēršanās Sīrijas kāmja embrija šūnās) un in vivo (žurku mikrokodolu tests) neatklāja nekādu ar narkotikām saistītu iedarbību ne gēnu, ne hromosomu līmenī. Kancerogenitātes pētījumi ar lenalidomīdu nav veikti.
Attīstības toksicitāte iepriekš tika pētīta trušiem. Šajos pētījumos trušiem iekšķīgi lietoja 3, 10 un 20 mg / kg lenalidomīda. Plaušu starpposma neesamība tika novērota, lietojot devu 10 un 20 mg / kg dienā, korelējot ar devu, un ārpusdzemdes nieres, lietojot devu 20 mg / kg dienā. Lai gan šie apstākļi tika novēroti, lietojot devu 20 mg / kg / dienā. devas, kas toksiskas mātei, var būt saistītas ar tiešu iedarbību Lietojot 10 un 20 mg / kg / dienā devas, augļos ir novērotas arī mīksto audu un skeleta izmaiņas.
06.0 FARMACEITISKĀ INFORMĀCIJA -
06.1 Palīgvielas
Kapsulas saturs
Bezūdens laktoze
Mikrokristāliskā celuloze
Nātrija kroskarmeloze
Magnija stearāts
Kapsulas apvalks
Želeja
Titāna dioksīds (E171)
Indigokarmīns (E132)
Dzeltenais dzelzs oksīds (E172)
Formulējuma tinte
Šellaks
Propilēnglikols
Melnais dzelzs oksīds (E172)
Kālija hidroksīds
06.2 Nesaderība "-
Nav būtisks.
06.3 Derīguma termiņš "-
3 gadi.
06.4 Īpaši uzglabāšanas nosacījumi -
Šīm zālēm nav nepieciešami īpaši uzglabāšanas apstākļi.
06.5 Tiešā iepakojuma veids un iepakojuma saturs -
Polivinilhlorīda (PVC) / polihlortrifluoretilēna (PCTFE) / alumīnija folijas blisteris ar 7 cietām kapsulām.
Iepakojumā 21 kapsula.
06.6 Lietošanas un lietošanas instrukcijas -
Neizlietotās zāles un šo zāļu atkritumi jāiznīcina saskaņā ar vietējiem noteikumiem.
07.0 "REĢISTRĀCIJAS APLIECĪBAS" ĪPAŠNIEKS
Celgene Europe Limited
1 Longwalk Road
Stoklija parks
Uksbridža
UB11 1DB
Lielbritānija
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS -
EU/1/07/391/002
038016022
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS -
Reģistrācijas datums: 2007. gada 14. jūnijs
Pēdējās atjaunošanas datums: 2012. gada 14. jūnijs
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS -
D.CCE 2016. gada septembris
11.0 RADIOPreparātiem - PILNĪGI DATI PAR IEKŠĒJO RADIĀCIJAS DOSIMETRIJU -
12.0 RADIOZĀLĒM, SĪKĀKAS SĪKĀKAS NORĀDĪJUMI PAR PAGAIDU SAGATAVOŠANU UN KVALITĀTES KONTROLI -















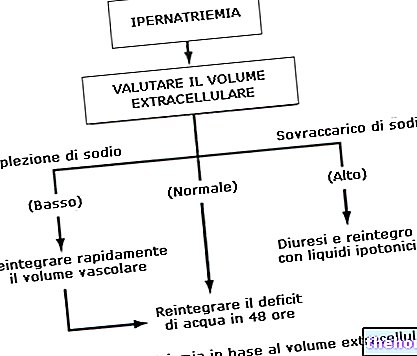


.jpg)







