Aktīvās sastāvdaļas: Prasugrel
Efient 10 mg apvalkotās tabletes
Efient 5 mg apvalkotās tabletes
Kāpēc lieto Efient? Kam tas paredzēts?
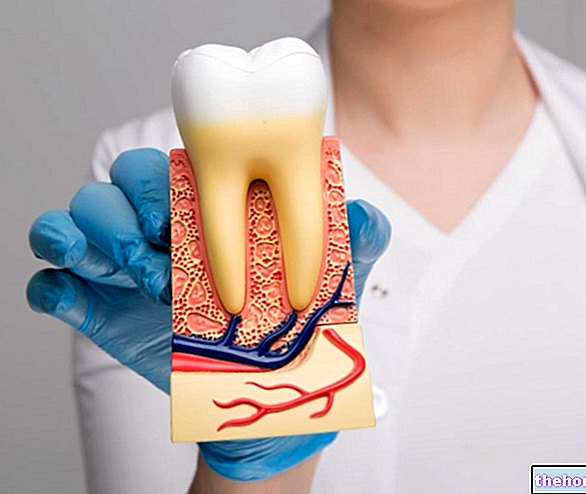
Efient, kas satur aktīvo vielu prasugrelu, pieder zāļu grupai, ko sauc par antitrombocītu līdzekļiem. Trombocīti ir ļoti mazas šūnas, kas cirkulē asinīs. Ja asinsvads ir bojāts, piemēram, ja tas ir sagriezts, trombocīti salīmējas kopā, lai veicinātu asins recekļa veidošanos (trombu). Tādēļ trombocīti ir būtiski, lai palīdzētu apturēt asiņošanu. Ja sacietējušā asinsvadā, piemēram, artērijā, veidojas recekļi, tie var būt ļoti bīstami, jo tie var bloķēt asinsriti, izraisot sirdslēkmi (miokarda infarktu), insultu vai nāvi Trombi artērijās, kas nes asinis uz sirdi, var arī samazināt asins plūsmu uz sirdi, izraisot nestabilu stenokardiju (stipras sāpes krūtīs).
Efient kavē trombocītu agregāciju un līdz ar to samazina trombu veidošanās iespēju.
Efient Jums tika parakstīts, jo Jums iepriekš ir bijis sirdslēkme vai nestabila stenokardija un esat ārstēts ar bloķētu sirds artēriju atvēršanas procedūru. Jums var būt bijis arī viens vai vairāki stenti, kas ievietoti aizsprostotajā vai sašaurinātajā artērijā, lai atjaunotu asins plūsmu. Efient samazina iespēju, ka Jums būs vēl viens sirdslēkme vai insults vai mirsit no kāda no šiem aterotrombotiskajiem notikumiem. Ārsts izrakstīs arī acetilsalicilskābi ( aspirīns), kas ir vēl viena antitrombocītu zāle.
Kontrindikācijas Kad Efient nedrīkst lietot
Nelietojiet Efient
- Ja Jums ir alerģija (paaugstināta jutība) pret prasugrelu vai kādu citu Efient sastāvdaļu. Alerģisku reakciju var atpazīt, jo tā izraisa izsitumus, niezi, sejas pietūkumu, lūpu pietūkumu vai sēkšanu.Ja rodas kāda no šīm parādībām, nekavējoties informējiet par to ārstu.
- Ja Jums ir veselības stāvoklis, kas izraisa asiņošanu, piemēram, asiņošana kuņģī vai zarnās.
- Ja Jums iepriekš ir bijis insults vai pārejošs išēmisks lēkme (TIA).
- Ja Jums ir smaga aknu slimība.
Piesardzība lietošanā Kas jāzina pirms Efient lietošanas
Ja rodas kāda no tālāk minētajām situācijām, pirms Efient lietošanas pastāstiet ārstam:
- Ja Jums ir paaugstināts asiņošanas risks, piemēram:
- 75 gadus veci vai vecāki. Ārsts izrakstīs dienas devu 5 mg, jo pacientiem, kas vecāki par 75 gadiem, ir paaugstināts asiņošanas risks.
- nesen smaga trauma
- nesen veikta operācija (ieskaitot dažas zobārstniecības procedūras)
- nesenā vai atkārtota asiņošana kuņģī vai zarnās (piemēram, kuņģa čūla vai resnās zarnas polips)
- ķermeņa svars ir mazāks par 60 kg. Ārsts izrakstīs Efient dienas devu 5 mg, ja Jūsu svars ir mazāks par 60 kg - mērena aknu vai nieru slimība
- ja lietojat noteiktas zāles (skatīt "Efient lietošana kopā ar citām zālēm")
- ja nākamo septiņu dienu laikā Jums paredzēta plānota operācija (ieskaitot dažas zobārstniecības procedūras). Ārsts var ieteikt uz laiku pārtraukt Efient lietošanu paaugstināta asiņošanas riska dēļ
- Ja Jums kādreiz ir bijušas alerģiskas (paaugstinātas jutības) reakcijas pret klopidogrelu vai kādu citu antitrombocītu līdzekli, lūdzu, pastāstiet savam ārstam pirms ārstēšanas uzsākšanas ar Efient. Ja pēc tam lietojat Efient un rodas alerģiskas reakcijas, kuras var atpazīt kā "izsitumus, niezi, sejas pietūkumu, lūpu pietūkumu vai elpas trūkumu, nekavējoties pastāstiet par to savam ārstam.
Lietojot Efient:
Nekavējoties pastāstiet savam ārstam, ja Jums rodas veselības stāvoklis, ko sauc par trombotisko trombocitopēnisko purpuru (PTT), kas ietver drudzi un zilumus zem ādas, kas var parādīties kā mazi sarkani punktiņi ar vai bez neizskaidrojama dziļa noguruma, apjukuma, krāsas maiņas vai bez tās. Dzeltena āda vai acis (dzelte) (skatīt 4. sadaļu "Iespējamās blakusparādības").
Bērni un pusaudži
Efient nav paredzēts lietošanai bērniem un pusaudžiem līdz 18 gadu vecumam.
Mijiedarbība Kādas zāles vai pārtikas produkti var mainīt Efient iedarbību
Pastāstiet ārstam par visām zālēm, kuras lietojat, pēdējā laikā esat lietojis vai varētu lietot, ieskaitot zāles, ko var iegādāties bez receptes, uztura bagātinātājus un augu izcelsmes līdzekļus. Ir īpaši svarīgi pastāstīt ārstam, ja Jūs ārstējat ar klopidogrelu (prettrombocītu zāles), varfarīnu (antikoagulantu) vai ar "nesteroīdiem pretiekaisuma līdzekļiem", lai mazinātu sāpes un samazinātu drudzi (piemēram, ibuprofēnu, naproksēns, etorikoksibs). Ja šīs zāles lieto kopā ar Efient, tās var palielināt asiņošanas risku.
Lietojiet citas zāles Efient lietošanas laikā tikai tad, ja ārsts to atļauj.
Brīdinājumi Ir svarīgi zināt, ka:
Grūtniecība un zīdīšanas periods
Pastāstiet ārstam, ja esat grūtniece vai plānojat grūtniecību Efient lietošanas laikā. Efient drīkst lietot tikai pēc tam, kad ar ārstu esat apspriedis iespējamos ieguvumus un iespējamo risku Jūsu nedzimušajam bērnam.
Ja barojat bērnu ar krūti, pirms jebkuru zāļu lietošanas konsultējieties ar ārstu vai farmaceitu
Transportlīdzekļu vadīšana un mehānismu apkalpošana
Maz ticams, ka Efient ietekmēs spēju vadīt transportlīdzekļus vai apkalpot mehānismus.
Efient satur laktozi.
Ja ārsts ir teicis, ka Jums ir “dažu cukuru nepanesamība, pirms šo zāļu lietošanas konsultējieties ar ārstu.
Deva, lietošanas veids un laiks Kā lietot Efient: Devas
Vienmēr lietojiet Efient tieši tā, kā ārsts Jums stāstījis. Ja rodas šaubas, konsultējieties ar ārstu vai farmaceitu.
Parastā Efient deva ir 10 mg dienā. Ārstēšana sākas ar vienu 60 mg devu. Ja jūsu ķermeņa svars ir mazāks par 60 kg vai ja esat vecāks par 75 gadiem, deva ir 5 mg Efient dienā.
Ārsts arī ieteiks lietot acetilsalicilskābi - viņš pateiks precīzu devu (parasti no 75 mg līdz 325 mg dienā).
Jūs varat lietot Efient kopā ar ēdienu vai bez tā. Lietojiet Efient katru dienu aptuveni vienā un tajā pašā laikā. Nesasmalciniet vai nesadaliet tableti.
Ir svarīgi pastāstīt ārstam, farmaceitam un zobārstam, ka lietojat Efient.
Pārdozēšana Ko darīt, ja esat lietojis pārāk daudz Efient
Ja esat lietojis Efient vairāk nekā noteikts
Nekavējoties sazinieties ar savu ārstu vai tuvāko slimnīcu, jo pastāv pārmērīga asiņošana. Parādiet ārstam savu Efient iepakojumu.
Ja esat aizmirsis lietot Efient
Ja esat aizmirsis lietot devu, ieņemiet vienu tableti, tiklīdz to pamanāt. Ja esat aizmirsis lietot devu visu dienu, nākamajā dienā vienkārši ieņemiet parasto Efient devu. Nelietojiet divas devas tajā pašā dienā. Iepakojumā pa 14, 28, 56, 84 un 98 tabletēm varat pārbaudīt pēdējās Efient tabletes lietošanas dienu, pārbaudot uz blistera uzdrukāto kalendāru.
Ja pārtraucat lietot Efient
Nepārtrauciet lietot Efient, neapspriežoties ar savu ārstu. Ja pārtraucat lietot Efient pārāk ātri, miokarda infarkta risks var būt lielāks.
Ja jums ir kādi jautājumi par šo zāļu lietošanu, jautājiet savam ārstam vai farmaceitam.
Blakusparādības Kādas ir Efient blakusparādības
Tāpat kā citas zāles, Efient var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas.
Jums nekavējoties jāsazinās ar ārstu, ja pamanāt kādu no šīm blakusparādībām:
- Pēkšņa miegainība vai vājums rokā, kājā vai sejā, īpaši, ja tā ir ierobežota vienā ķermeņa pusē
- Pēkšņa apjukums, grūtības runāt vai saprast citu teikto
- Pēkšņas grūtības staigāt vai līdzsvara vai koordinācijas zudums
- Pēkšņs reibonis vai pēkšņas stipras galvassāpes bez zināma iemesla.
Viss iepriekš minētais var būt insulta pazīmes. Insults ir reta Efient blakusparādība pacientiem, kuriem nekad nav bijis insults vai pārejošs išēmisks lēkme (TIA).
Nekavējoties sazinieties arī ar savu ārstu, ja pamanāt kādu no šīm blakusparādībām:
- drudzis un zilumi zem ādas, kas var parādīties kā sīki sarkani punktiņi, ar vai bez neizskaidrojama dziļa noguruma, apjukuma, ādas vai acu dzeltenuma (dzelte) (skatīt 2. punktu "PIRMS EFIENT LIETOŠANAS")
- "izsitumi uz ādas, nieze vai sejas pietūkums, lūpu / mēles pietūkums vai sēkšana. Tas viss var liecināt par nopietnu alerģisku reakciju (skatīt 2. punktu" Kas jāzina pirms Efient lietošanas ")
Jums nekavējoties jāsazinās ar ārstu, ja pamanāt kādu no šīm blakusparādībām:
- Asinis urīnā
- Asiņošana no taisnās zarnas, asinis izkārnījumos vai izkārnījumi melnā krāsā
- Nekontrolējama asiņošana, piemēram, no griezuma
Viss iepriekš minētais var būt asiņošanas pazīmes, kas ir visizplatītākā Efient blakusparādība. Lai gan retāk, smaga asiņošana var būt dzīvībai bīstama.
Biežas blakusparādības (var skart līdz 1 no 10 cilvēkiem)
- Asiņošana kuņģī vai zarnās
- Asiņošana no adatas dūriena vietas
- Deguna asiņošana
- Ādas izsitumi
- Nelieli sarkani zilumi uz ādas (zilumi)
- Asinis urīnā
- Hematoma (asiņošana zem ādas injekcijas vietā vai muskulī, izraisot pietūkumu)
- Zems hemoglobīna līmenis vai zems sarkano asins šūnu skaits (anēmija)
- Brūces
Retākas blakusparādības (var skart līdz 1 no 100 cilvēkiem)
- Alerģiska reakcija (izsitumi, nieze, lūpu / mēles pietūkums vai sēkšana)
- Spontāna asiņošana no acs, taisnās zarnas, smaganām vai vēdera ap iekšējiem orgāniem
- Asiņošana pēc operācijas
- Klepojot asinis
- Asinis izkārnījumos
Retas blakusparādības (var skart līdz 1 no 1000 cilvēkiem)
- Zems trombocītu skaits asinīs
- Zemādas hematoma (asiņošana zem ādas, kas izraisa pietūkumu)
Ziņošana par blakusparādībām
Ja novērojat jebkādas blakusparādības, kas šajā instrukcijā nav minētas, vai kāda no minētajām blakusparādībām Jums izpaužas smagi, lūdzu, izstāstiet to savam ārstam vai farmaceitam. Jūs varat ziņot par blakusparādībām arī tieši, izmantojot V pielikumā minēto valsts ziņošanas sistēmu. Ziņojot par blakusparādībām, jūs varat palīdzēt iegūt vairāk informācijas par šo zāļu drošumu.
Derīguma termiņš un saglabāšana
Uzglabāt Efient bērniem neredzamā un nepieejamā vietā.
Nelietot Efient pēc derīguma termiņa beigām, kas norādīts uz blistera un kastītes pēc “Derīgs līdz”. Derīguma termiņš attiecas uz mēneša pēdējo dienu.
Uzglabāt oriģinālajā iepakojumā, lai pasargātu no gaisa un mitruma.
Zāles nedrīkst izmest kanalizācijā vai sadzīves atkritumos. Jautājiet farmaceitam, kā izmest zāles, kuras vairs nelietojat. Tas palīdzēs aizsargāt vidi.
Ko Efient satur
- Aktīvā viela ir prasugrels.
Efient 10 mg: katra tablete satur 10 mg prasugrela (hidrohlorīda veidā).
Efient 5 mg: katra tablete satur 5 mg prasugrela (hidrohlorīda veidā).
- Citas sastāvdaļas ir mikrokristāliskā celuloze, mannīts (E421), nātrija kroskarmeloze, hipromeloze (E464), magnija stearāts, laktozes monohidrāts, titāna dioksīds (E171), triacetīns (E1518), sarkanais dzelzs oksīds (tikai 10 mg tabletēm) (E172) , dzeltenais dzelzs oksīds (E172) un talks.
Efient ārējais izskats un iepakojums
Efient 10 mg: tabletes ir smilškrāsas un dubultās bultiņas formas, ar iespiedumu "10 MG" vienā pusē un "4759" otrā pusē.
Efient 5 mg: tabletes ir dzeltenas un dubultas bultiņas formas, ar iespiedumu "5 MG" vienā pusē un "4760" otrā pusē.
Efient ir pieejams iepakojumos pa 14, 28, 30, 56, 84, 90 un 98 tabletēm.
Visi iepakojuma lielumi tirgū var nebūt pieejami.
Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī. Pašlaik pieejamā informācija var nebūt atjaunināta.
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija.
01.0 ZĀĻU NOSAUKUMS
EFIENT 10 MG TABLETES, KAS PĀRKLĀTAS AR FILMU
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS
Katra tablete satur 10 mg prasugrela (hidrohlorīda veidā).
Palīgvielas ar zināmu iedarbību: katra tablete satur 2,1 mg laktozes.
Pilnu palīgvielu sarakstu skatīt apakšpunktā 6.1.
03.0 ZĀĻU FORMA
Apvalkotā tablete (tablete).
Bēšas krāsas, dubultās bultiņas formas tabletes ar iespiedumu "10 MG" vienā pusē un "4759" otrā.
04.0 KLĪNISKĀ INFORMĀCIJA
04.1 Terapeitiskās indikācijas
Efient, lietojot kombinācijā ar acetilsalicilskābi (ASS), ir indicēts aterotrombotisku notikumu profilaksei pieaugušiem pacientiem ar akūtu koronāro sindromu (AKS) (t.i., nestabilu stenokardiju, miokarda infarktu bez ST segmenta pacēluma [UA / NSTEMI] vai ST segmenta). paaugstināts miokarda infarkts [STEMI]), kam tiek veikta primāra vai aizkavēta perkutāna koronārā iejaukšanās (PCI).
Sīkāku informāciju skatīt 5.1.
04.2 Devas un lietošanas veids
Devas
Pieaugušie
Efient jāsāk ar vienu 60 mg piesātinošu devu un pēc tam jāturpina ar 10 mg vienu reizi dienā. Pacientiem, kuri lieto Efient, jālieto arī 75 - 325 mg acetilsalicilskābes (ASS) dienā.
Pacientiem ar akūtu koronāro sindromu (AKS), kam tiek veikta perkutāna koronārā iejaukšanās, agrīna jebkādu antitrombocītu zāļu, tostarp Efient, pārtraukšana var palielināt trombozes, miokarda infarkta vai nāves risku pacienta veselības stāvokļa dēļ. Ieteicams lietot mēnešu ilgumu, ja vien Efient lietošanas pārtraukšana nav klīniski indicēta (skatīt 4.4. un 5.1. apakšpunktu).
Vecuma pacienti ≥ 75 gadus vecs
Efient lietošana pacientiem, kas vecāki par 75 gadiem, parasti nav ieteicama. Ja pēc ārstējošā ārsta rūpīgas individuālās ieguvuma un riska attiecības izvērtēšanas (skatīt apakšpunktu 4.4) ārstēšana ar Efient tiek uzskatīta par nepieciešamu pacientiem vecuma grupā ≥ 75 gadi, pēc 60 mg piesātinošās devas jānosaka samazināta uzturošā deva 5 mg. Pacientiem vecumā no 75 gadiem ir paaugstināta jutība pret asiņošanu un paaugstināta prasugrela aktīvās sastāvdaļas metabolīta iedarbība (skatīt 4.4., 4.8., 5.1. 5.2).
Pacienti ar ķermeņa svaru
Efient jāievada kā viena 60 mg piesātinošā deva, kam seko 5 mg deva vienu reizi dienā. Uzturošā deva 10 mg nav ieteicama. Tas ir saistīts ar prasugrela aktīvā metabolīta iedarbības palielināšanos un palielinātu asiņošanas risku pacientiem ar svaru.
Nieru darbības traucējumi
Pacientiem ar nieru mazspēju, ieskaitot pacientus ar beigu stadijas nieru slimību, devas pielāgošana nav nepieciešama (skatīt 5.2. Apakšpunktu). Ir ierobežota terapeitiskā pieredze pacientiem ar nieru mazspēju (skatīt apakšpunktu 4.4).
Aknu darbības traucējumi
Pacientiem ar viegliem vai vidēji smagiem aknu darbības traucējumiem (A un B klase pēc Child-Pugh) deva nav jāpielāgo (skatīt 5.2. Apakšpunktu). Ir ierobežota terapeitiskā pieredze pacientiem ar viegliem un vidēji smagiem aknu darbības traucējumiem (skatīt apakšpunktu 4.4). Efient ir kontrindicēts pacientiem ar smagiem aknu darbības traucējumiem (C klase pēc Child Pugh).
Pediatriskā populācija
Efient drošība un efektivitāte, lietojot bērniem līdz 18 gadu vecumam, vēl nav pierādīta.
Lietošanas veids
Iekšķīgai lietošanai. Efient var lietot neatkarīgi no ēdienreizēm. 60 mg prasugrela piesātinošās devas lietošana tukšā dūšā var izraisīt ātrāku zāļu iedarbības sākumu (skatīt 5.2. Apakšpunktu). Nesasmalciniet vai nesadaliet tableti.
04.3 Kontrindikācijas
Paaugstināta jutība pret aktīvo vielu vai jebkuru no 6.1. Apakšpunktā uzskaitītajām palīgvielām.
Notiek patoloģiska asiņošana.
Insults vai pārejoša išēmiska lēkme (TIA) anamnēzē.
Smagi aknu darbības traucējumi (C klase pēc Child-Pugh).
04.4 Īpaši brīdinājumi un piesardzība lietošanā
Asiņošanas risks
3. fāzes klīniskajā pētījumā galvenie izslēgšanas kritēriji bija paaugstināts asiņošanas risks; anēmija; trombocitopēnija; atklājumu vēsture, kas liecina par intrakraniālu patoloģiju.
Pacientiem ar akūtu koronāro sindromu, kuriem tika veikta perkutāna koronārā iejaukšanās un kuri tika ārstēti ar Efient un ASA, saskaņā ar TIMI klasifikācijas sistēmu palielinājās smagas un nelielas asiņošanas risks.
Tādēļ Efient lietošana pacientiem ar paaugstinātu asiņošanas risku jāapsver tikai tad, ja tiek uzskatīts, ka ieguvumi no išēmisku notikumu profilakses atsver nopietnas asiņošanas risku. Šis piesardzības pasākums īpaši attiecas uz pacientiem:
• vecums ≥75 gadi (skatīt zemāk).
• ar noslieci uz asiņošanu (piemēram, nesenas traumas, nesenas operācijas, nesenas vai atkārtotas kuņģa -zarnu trakta asiņošanas vai notiekošas peptiskas čūlas dēļ)
• ar ķermeņa svaru
• vienlaikus ārstējot ar zālēm, kas var palielināt asiņošanas risku, ieskaitot perorālos antikoagulantus, klopidogrelu, nesteroīdos pretiekaisuma līdzekļus (NPL) un fibrinolītiskos līdzekļus.
Pacientiem ar pastāvīgu asiņošanu, kuriem jāmaina Efient farmakoloģiskā iedarbība, var būt piemērota trombocītu pārliešana.
Efient lietošana pacientiem, kas vecāki par 75 gadiem, parasti nav ieteicama, un tā jādara tikai piesardzīgi pēc tam, kad "ārsts, kurš izrakstījis zāles, rūpīgi izvērtē ieguvumu un risku, liecina, ka išēmisku notikumu profilakses ieguvums ir lielāks par nopietnas asiņošanas risku". . 3. fāzes klīniskajā pētījumā šiem pacientiem bija paaugstināts asiņošanas risks, ieskaitot letālu asiņošanu, salīdzinot ar vecuma pacientiem
Terapeitiskā pieredze ar prasugrelu pacientiem ar nieru darbības traucējumiem (ieskaitot pacientus ar nieru slimību beigu stadijā (ESRD)) un pacientiem ar vidēji smagiem aknu darbības traucējumiem ir ierobežota. Šiem pacientiem var būt paaugstināts asiņošanas risks.
Tādēļ šiem pacientiem prasugrels jālieto piesardzīgi.
Pacienti jābrīdina, ka, lietojot prasugrelu (kombinācijā ar ASS), asiņošanas apturēšana var aizņemt ilgāku laiku nekā parasti, un jāinformē ārsts par jebkuru neparastu asiņošanu (pēc atrašanās vietas vai ilguma).
Ķirurģiska iejaukšanās
Pirms jebkādas operācijas un pirms jaunu zāļu lietošanas pacientiem jāpasaka ārstiem un zobārstiem, ka viņi lieto prasugrelu. Ja pacientam plānota operācija un antitrombocītu iedarbība netiek uzskatīta par atbilstošu, Efient lietošana jāpārtrauc vismaz 7 dienas pirms operācijas. Pacientiem, kuriem tiek veikta CABG operācija, asiņošanas biežums un smagums var palielināties (3 reizes). 7 dienas pēc prasugrela lietošanas pārtraukšanas (skatīt 4.8. Apakšpunktu). Prasugrela ieguvumi un riski rūpīgi jāapsver tiem pacientiem, kuriem nav noteikta koronārā anatomija, un ir iespējama steidzama CABG operācija.
Paaugstināta jutība, ieskaitot angioneirotisko tūsku
Pacientiem, kas lieto prasugrelu, tostarp pacientiem ar paaugstinātas jutības reakcijām pret klopidogrelu, ziņots par paaugstinātas jutības reakcijām, tai skaitā angioneirotisko tūsku. Pacientiem ar zināmu alerģiju pret tienopiridīniem ir ieteicams kontrolēt paaugstinātas jutības pazīmes (skatīt apakšpunktu 4.8).
Trombotiskā trombocitopēniskā purpura (PTT)
Ir ziņots par PTT, lietojot prasugrelu. PTT ir nopietns stāvoklis, kas prasa tūlītēju ārstēšanu.
Laktoze
Pacientiem ar retu iedzimtu galaktozes nepanesību, Lapp laktāzes deficītu vai glikozes-galaktozes malabsorbciju nevajadzētu lietot Efient..
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi
Varfarīns: Efient un citu kumarīna atvasinājumu, izņemot varfarīnu, vienlaicīga lietošana nav pētīta. Tā kā ir palielināts asiņošanas risks, jāievēro piesardzība, vienlaikus lietojot varfarīnu (vai citus kumarīna atvasinājumus) un prasugrelu (skatīt apakšpunktu 4.4).
Nesteroīdie pretiekaisuma līdzekļi (NPL):
Hronisku NSPL vienlaicīga lietošana nav pētīta. Tā kā ir palielināts asiņošanas risks, hronisku NPL (ieskaitot COX-2 inhibitorus) un Efient lietošana vienlaikus jāveic piesardzīgi (skatīt apakšpunktu 4.4).
Efient var ievadīt kombinācijā ar zālēm, kuras metabolizē citohroma P450 enzīmi (ieskaitot statīnus), vai zālēm, kas ir citohroma P450 enzīmu induktori vai inhibitori. Efient var lietot arī kombinācijā ar ASS, heparīnu, digoksīnu un zālēm, kas paaugstina kuņģa pH, ieskaitot protonu sūkņa inhibitorus un H2 blokatorus.
Lai gan tas nebija specifisku mijiedarbības pētījumu priekšmets, Efient tika ievadīts 3. fāzes klīniskajā pētījumā kombinācijā ar zemas molekulmasas heparīnu, bivalirudīnu un GP IIb / IIIa inhibitoriem (nav pieejama informācija par GP IIb / IIIa inhibitoru veidu). bez pierādījumiem par klīniski nozīmīgu nelabvēlīgu mijiedarbību.
Citu zāļu ietekme uz Efient:
Acetilsalicilskābe: Efient jāievada kombinācijā ar ASS. Lai gan ir iespējama farmakodinamiskā mijiedarbība ar ASS, līdz ar to palielināts asiņošanas risks, pierādījumi par prasugrela efektivitāti un drošību ir iegūti no pacientiem, kuri tiek ārstēti kombinācijā ar ASS.
Heparīns: Viena nefrakcionēta heparīna intravenoza bolus deva (100 V / kg) būtiski nemainīja prasugrela izraisīto trombocītu agregācijas inhibīciju. Tāpat prasugrels būtiski nemainīja heparīna ietekmi uz koagulācijas parametriem.
Tādēļ abas zāles var lietot kombinācijā. Lietojot Efient kombinācijā ar heparīnu, ir iespējams paaugstināts asiņošanas risks.
Statīni: Atorvastatīns (80 mg dienā) nemainīja prasugrela farmakodinamisko aktivitāti vai kavēja trombocītu agregāciju. Tādēļ nav sagaidāms, ka CYP3A substrāta statīni ietekmēs prasugrela farmakokinētiku vai prasugrela inhibīciju..
Zāles, kas paaugstina kuņģa pHVienlaicīga ranitidīna (H2 blokators) vai lansoprazola (protonu sūkņa inhibitors) lietošana katru dienu nemainīja prasugrela aktīvā metabolīta AUC un Tmax, bet samazināja Cmax attiecīgi par 14% un 29%.3. fāzes klīniskajā pētījumā Efient tika ievadīts neatkarīgi no vienlaicīgas protonu sūkņa inhibitora vai H2 blokatora lietošanas. Lietojot 60 mg prasugrela piesātinošo devu, vienlaikus neizmantojot protonu sūkņa inhibitorus, zāļu iedarbība var sākties ātrāk.
CYP3A inhibitoriKetokonazols (400 mg dienā), spēcīgs un selektīvs CYP3A4 un CYP3A5 inhibitors, nemainīja prasugrela izraisīto trombocītu agregācijas inhibīciju vai prasugrela aktīvā metabolīta AUC un T, bet samazināja Cmax par 34% līdz 46% Tāpēc nav sagaidāms, ka CYP3A inhibitori, piemēram, azola pretsēnīšu līdzekļi, HIV proteāzes inhibitori, klaritromicīns, telitromicīns, verapamils, diltiazems, indinavīrs, ciprofloksacīns un greipfrūtu sula, būtiski neietekmēs aktīvā metabolīta farmakokinētiku.
Citohroma P450 induktori: Rifampicīns (600 mg dienā), spēcīgs CYP3A un CYP2B6 induktors, kā arī CYP2C9, CYP2C19 un CYP2C8 induktors, būtiski nemainīja prasugrela farmakokinētiku. Tāpēc nav sagaidāms, ka zināmi CYP3A induktori, piemēram, rifampicīns, karbamazepīns un citi citohromu P450 induktori, būtiski ietekmēs aktīvā metabolīta farmakokinētiku.
Efient ietekme uz citām zālēm:
DigoksīnsPrasugrelam nav klīniski nozīmīgas ietekmes uz digoksīna farmakokinētiku.
Zāles, ko metabolizē CYP2C9Prasugrels neinhibēja CYP2C9, jo neietekmēja varfarīna-S farmakokinētiku. Iespējama paaugstināta asiņošanas riska dēļ, lietojot varfarīnu un Efient kombinācijā, jāievēro piesardzība (skatīt apakšpunktu 4.4).
Zāles, ko metabolizē CYP2B6Prasugrels ir vājš CYP2B6 inhibitors. Veseliem cilvēkiem prasugrels par 23%samazināja hidroksibupropiona-CYP2B6 mediētā bupropiona metabolīta-iedarbību. Šis efekts varētu būt klīniski nozīmīgs tikai tad, ja prasugrelu lieto kombinācijā ar zālēm, kurām vienīgais metabolisma ceļš ir CYP2B6 un kurām ir ierobežots terapeitiskais periods (piemēram, ciklofosfamīds, efavirenzs).
04.6 Grūtniecība un zīdīšana
Nav veikti klīniskie pētījumi grūtniecēm un sievietēm, kas baro bērnu ar krūti.
Grūtniecība
Pētījumi ar dzīvniekiem neliecina par tiešu kaitīgu ietekmi uz grūtniecību, embrija / augļa attīstību, dzemdībām vai pēcdzemdību attīstību (skatīt 5.3. Apakšpunktu). Tā kā reproduktīvās aktivitātes pētījumi ar dzīvniekiem ne vienmēr paredz ietekmi uz cilvēkiem, Efient grūtniecības laikā drīkst lietot tikai tad, ja iespējamais ieguvums attaisno iespējamo risku auglim.
Barošanas laiks
Nav zināms, vai prasugrels izdalās mātes pienā. Pētījumi ar dzīvniekiem ir parādījuši prasugrela izdalīšanos mātes pienā.Prasugrela lietošana zīdīšanas laikā nav ieteicama.
Auglība
Prasugrels neietekmēja žurku tēviņu un mātīšu auglību, lietojot perorālās devas, kas līdz 240 reizēm pārsniedza ieteicamo uzturošo dienas devu cilvēkam (novērtēts mg / m2).
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus
Nav sagaidāms, ka Prasugrel ietekmēs vai nenozīmīgi ietekmēs spēju vadīt transportlīdzekļus vai apkalpot mehānismus.
04.8 Nevēlamās blakusparādības
Drošības profila kopsavilkums
Drošums pacientiem ar akūtu koronāro sindromu, kuriem tiek veikta perkutāna koronārā iejaukšanās, tika novērtēts klopidogrela (TRITON) kontrolētā klīniskajā pētījumā, kurā 6741 pacientu ārstēja ar prasugrelu (ar piesātinošo devu 60 mg un uzturošo devu 10 mg dienā). vidēji 14,5 mēneši (5 802 pacienti tika ārstēti ilgāk par 6 mēnešiem, 4 136 pacienti tika ārstēti ilgāk par 1 gadu). Pētāmo zāļu pārtraukšanas biežums blakusparādību dēļ bija 7,2% prasugrela un 6,3% klopidogrela. No tiem asiņošana bija visizplatītākā blakusparādība, kuras dēļ abas zāles tika pārtrauktas (2,5% prasugrela un 1,4% klopidogrela).
Asiņošana
Asiņošana, kas nav saistīta ar koronāro artēriju šuntēšanu (CABG)
TRITON pētījumā to pacientu biežums, kuriem bija asiņošanas epizode, kas nav saistīta ar koronāro artēriju šuntēšanu (CABG), ir parādīta 1. tabulā. Lielas asiņošanas biežums (pēc TIMI definīcijām), kas nav saistīts ar koronāro artēriju šuntēšanu (CABG), ieskaitot tos, kuriem draud nāve un letāls iznākums, kā arī neliela asiņošana (saskaņā ar TIMI definīcijām) bija statistiski ticami augstāka pacientiem, kas ārstēti ar prasugrelu, salīdzinot ar pacientiem, kuri ārstēti ar klopidogrelu, gan UA / NSTEMI, gan visā AKS populācijā . STEMI populācijā netika novērotas būtiskas atšķirības. Visbiežāk spontānā asiņošana bija kuņģa -zarnu trakts (1,7%, lietojot prasugrelu un 1,3%, lietojot klopidogrelu); visbiežāk sastopamā asiņošanas vieta bija artēriju piekļuves vieta (1,3% ar prasugrelu un 1,2% ar klopidogrelu).
1. tabula. Asiņošanas biežums, kas nav saistīts ar koronāro artēriju šuntēšanas operāciju (CABG) a (% pacientu)
a Notikumi, kas definēti pēc kritērijiem, ko veic pētījuma grupas trombolīze miokarda infarkta gadījumā (TIMI) centralizēta.
b Pēc vajadzības tika ievadītas citas standarta terapijas.
c Jebkura intrakraniāla asiņošana vai klīniski acīmredzama asiņošana, kas saistīta ar samazināšanos hemoglobīna līmenis ≥5 g / dl.
d Asiņošana ar nāves risku ir lielas asiņošanas apakšgrupa (saskaņā ar TIMI definīcijām) e ietver tālāk uzskaitītos veidus. Pacientus var saskaitīt vairākās rindās.
un ICH = intrakraniāla asiņošana.
f Klīniski acīmredzama asiņošana, kas saistīta ar hemoglobīna līmeņa pazemināšanos ≥3 g / dl, bet
Vecuma pacienti ≥ 75 gadus vecs
Lielas vai nelielas asiņošanas biežums (TIMI), kas nav saistīts ar koronāro artēriju šuntēšanu (CABG):
* TRITON pētījums pacientiem ar AKS, kuriem tiek veikta PCI
** TRILOGY-ACS pētījums pacientiem, kuriem netiek veikta PCI (skatīt 5.1. Apakšpunktu):
uz prasugrels 10 mg; prasugrel 5 mg, ja
Pacienti ar ķermeņa svaru
Lielas vai nelielas asiņošanas biežums (TIMI), kas nav saistīts ar koronāro artēriju šuntēšanu (CABG):
* TRITON pētījums pacientiem ar AKS, kuriem tiek veikta PCI
** TRILOGY-ACS pētījums pacientiem, kuriem netiek veikta PCI (skatīt 5.1. Apakšpunktu):
uz prasugrels 10 mg; 5 mg prasugrela, ja vecums ir ≥75 gadi
Pacienti, kuru ķermeņa masa ir ≥60 kg un vecums
Pacientiem, kuru ķermeņa masa ir ≥60 kg un vecums
Asiņošana saistībā ar koronāro artēriju šuntēšanu (CABG)
3. fāzes klīniskajā pētījumā 437 pacientiem tika veikta koronāro artēriju šuntēšana (CABG). No šiem pacientiem lielas vai nelielas asiņošanas (TIMI) biežums saistībā ar koronāro artēriju šuntēšanu (CABG) bija 14,1% prasugrela grupā un 4,5% klopidogrela grupā. Vislielākais asiņošanas epizožu risks pacientiem, kuri tika ārstēti ar prasugrelu, saglabājās līdz 7 dienām pēc pēdējās pētāmās zāles devas. Pacientiem, kuri saņēma tienopiridīnu 3 dienu laikā pirms koronāro artēriju šuntēšanas (CABG), smagas vai nelielas asiņošanas (TIMI) biežums prasugrela grupā bija 26,7% (12 no 45 pacientiem), salīdzinot ar 5,0% (3 no 60 pacientiem) klopidogrela grupā. Pacientiem, kuri saņēma pēdējo tienopiridīna devu 4 līdz 7 dienu laikā pirms koronāro artēriju šuntēšanas (CABG), biežums prasugrela grupā samazinājās līdz 11,3% (9 no 80 pacientiem) un 3,4 % (3 no 89 pacientiem) klopidogrela grupā. Vairāk nekā 7 dienas pēc zāļu lietošanas pārtraukšanas novērotais asiņošanas biežums, kas saistīts ar koronāro artēriju šuntēšanu (CABG), bija līdzīgs 2 ārstēšanas grupās (skatīt apakšpunktu 4.4).
Nevēlamo blakusparādību kopsavilkuma tabula
2. tabulā apkopotas hemorāģiskās un nehemorāģiskās blakusparādības TRITON pētījumā vai spontānos ziņojumos, kas klasificēti pēc biežuma un orgānu sistēmas. To biežums ir noteikts, ievērojot šādus nosacījumus: Ļoti bieži (≥ 1/10); bieži (≥ 1/100,
2. tabula. Hemorāģiskas un nehemorāģiskas blakusparādības
Pacientiem ar vai bez anamnēzē pārejošas išēmiskas lēkmes (TIA) vai insulta insulta biežums 3. fāzes pētījumā bija šāds (skatīt apakšpunktu 4.4):
* ICH = intrakraniāla asiņošana.
Ziņošana par iespējamām blakusparādībām
Ir svarīgi ziņot par iespējamām blakusparādībām, kas radušās pēc zāļu reģistrācijas, jo tas ļauj nepārtraukti uzraudzīt zāļu ieguvuma un riska attiecību. Veselības aprūpes speciālistus lūdz ziņot par visām iespējamām blakusparādībām, izmantojot valsts ziņošanas sistēmu. .
04.9 Pārdozēšana
Efient pārdozēšana var pagarināt asiņošanas laiku un izraisīt asiņošanas komplikācijas. Nav informācijas par prasugrela farmakoloģiskās aktivitātes "atcelšanu"; tomēr, ja nepieciešama ātra pagarināta asiņošanas laika korekcija, var apsvērt trombocītu vai citu asins produktu pārliešanu.
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS
05.1 Farmakodinamiskās īpašības
Farmakoterapeitiskā grupa: antitrombocītu līdzekļi, izņemot heparīnu.
ATĶ kods: B01AC22.
Farmakodinamiskā iedarbība
Prasugrels ir trombocītu aktivācijas un agregācijas inhibitors, kas darbojas, neatgriezeniski saistoties tā aktīvajam metabolītam ar P2Y12 klases ADP trombocītu receptoriem. Trombocītu funkcija var samazināt kardiovaskulāro notikumu, piemēram, nāves, miokarda infarkta vai insulta, biežumu.
Pēc 60 mg prasugrela piesātinošās devas ADP izraisīta trombocītu agregācijas inhibīcija notiek 15 minūtēs ar 5 mcM ADP un 30 minūtēs ar 20 mcM ADP. Maksimālā trombocītu agregācijas inhibīcija, ko izraisa ADP, kas iegūta ar prasugrelu, ir 83% ar 5 mcM ADP un 79% ar 20 mcM ADP, abos gadījumos ar 89% veseliem cilvēkiem un pacientiem ar stabilu aterosklerozi 1 stundas laikā sasniedzot vismaz 50% trombocītu agregācijas inhibīcijas. Trombocītu agregācijas inhibīcija, kas panākta, lietojot Prasugrel, liecina par mazāku (9%) un indivīda (12%) mainīgumu gan ar 5 mcM, gan 20 mcM ADP. Vidējā trombocītu agregācijas inhibīcija līdzsvara stāvoklī bija 74% un 69%, attiecīgi 5 mcM ADP un 20 mcM ADP, un tā tika sasniegta pēc 3 līdz 5 dienu ilgas vienas devas lietošanas. mg prasugrela pirms 60 mg piesātinošās devas uzturēšanas devas laikā vairāk nekā 98% pacientu trombocītu agregācijas inhibīcija bija ≥ 20%.
Pēc ārstēšanas trombocītu agregācija pakāpeniski atgriezās sākotnējā stāvoklī 7 līdz 9 dienu laikā pēc vienas 60 mg prasugrela piesātinošās devas ievadīšanas un 5 dienas pēc līdzsvara uzturēšanas devas pārtraukšanas.
Dati par pāreju no klopidogrela uz prasugrelu: Pēc 75 mg klopidogrela lietošanas vienreiz dienā 10 dienas 40 veseliem indivīdiem pārgāja uz 10 mg prasugrela vienu reizi dienā, ar vai bez 60 mg piesātinošās devas. Lietojot prasugrelu, tika novērota līdzīga vai lielāka trombocītu agregācijas inhibīcija. Pārejot tieši uz 60 mg prasugrela piesātinošo devu, trombocītu inhibīcijas palielināšanās sākās ātrāk.Pēc 900 mg klopidogrela piesātinošās devas (kombinācijā ar ASS) ievadīšanas 56 pacienti ar AKS 14 dienas tika ārstēti ar 10 mg prasugrela vienu reizi dienā vai 150 mg klopidogrela vienu reizi dienā, un viņi tika mainīti uz ārstēšanu ar 150 mg klopidogrela vai prasugrela 10 mg attiecīgi vēl 14 dienas ("slēdzis"). Vislielākā trombocītu agregācijas inhibīcija tika novērota pacientiem, kuri pārgāja uz 10 mg prasugrela, salīdzinot ar tiem, kuri tika ārstēti ar 150 mg klopidogrela. pēc hospitalizācijas pirms koronāro angiogrāfijas, lietojot piesātinošo devu 60 mg prasugrela, kas tika ievadīts perkutānas koronārās iejaukšanās laikā, izraisīja līdzīgu agregācijas inhibīcijas trombocītu skaita pieaugumu 72 stundu pētījuma laikā.
Efektivitāte un drošība akūta koronārā sindroma gadījumā
Trešās fāzes TRITON pētījumā Efient (prasugrelu) salīdzināja ar klopidogrelu, abi kopā ar ASS un citām standarta terapijām. TRITON ir starptautisks, randomizēts, dubultmaskēts, paralēlas grupas daudzcentru pētījums, kurā piedalījās 13 608 pacienti. Pacientiem bija ACS ar mērenu vai augstu riska UA un NSTEMI vai STEMI, un viņi tika ārstēti ar PCI.
Pacienti ar UA / NSTEMI 72 stundu laikā pēc simptomu parādīšanās vai ar STEMI no 12 stundām līdz 14 dienām pēc simptomu parādīšanās tika randomizēti pēc zināšanām par koronārās asinsrites anatomiju. Pacienti ar STEMI 12 stundu laikā pēc simptomu parādīšanās un plānoti primārajai PCI Visiem pacientiem piesātinošo devu varēja ievadīt jebkurā laikā no randomizācijas līdz 1 stundai pēc tam, kad pacients bija izgājis no laboratorijas, kurā tika veikta sirds katetrizācija.
Pacienti, kuri tika nejauši izvēlēti pēc prasugrela (60 mg piesātinošās devas, kam seko 10 mg vienu reizi dienā) vai klopidogrela (300 mg piesātinošās devas, kam seko 75 mg vienu reizi dienā), tika ārstēti vidēji 14,5 mēnešus (ne ilgāk kā 15 mēnešus, bet vismaz (6 mēnešu novērošana). Pacienti saņēma arī ASS (no 75 mg līdz 325 mg vienu reizi dienā).
Jebkura tienopiridīna lietošana 5 dienas pirms uzņemšanas bija izslēgšanas kritērijs. Citas terapijas, piemēram, heparīns un GPIIb / IIIa inhibitori, tika ievadītas pēc ārsta ieskatiem. Apmēram 40% pacientu (katrā ārstēšanas grupā) bija saņēmuši GPIIb / IIIa inhibitorus, lai atbalstītu PCI (informācija par GP IIb tipu nav pieejama) / IIIa inhibitoru.) Aptuveni 98% pacientu (katrā ārstēšanas grupā) bija tieši saņēmuši antitrombīnus (heparīnu, zemas molekulmasas heparīnu, bivalirudīnu vai citas zāles) kā atbalstu PCI.
Pētījuma iznākuma primārais rādītājs bija laiks līdz pirmajam kardiovaskulārās (CV) nāves gadījumam, nāvējošam miokarda infarktam (MI) vai nāvējošam insultam. Apvienotā mērķa analīze visā ACS populācijā (ieskaitot UA / NSTEMI un STEMI grupas) bija atkarīga no prasugrela statistiskā pārākuma pierādīšanas salīdzinājumā ar klopidogrelu UA / NSTEMI grupā (p
ACS kopējā populācija: Efient demonstrēja izcilu efektivitāti salīdzinājumā ar klopidogrelu, samazinot primāro salikto parametru, kā arī iepriekš noteiktos sekundāros parametrus, ieskaitot stenta trombozi (skatīt 3. tabulu). Prasugrela ieguvums bija redzams pirmajās 3 dienās un turpinājās līdz pētījuma beigām. Augstāko efektivitāti papildināja smagas asiņošanas palielināšanās (skatīt 4.4. Un 4.8. Apakšpunktu). Pacientu populācija bija 92% kaukāziešu, 26% sieviešu un 39% vecāki par 65 gadiem. Ieguvumi, kas saistīti ar prasugrelu, nebija atkarīgi no citu akūtu un ilgstošu kardiovaskulāru terapiju lietošanas, ieskaitot zemas molekulmasas heparīnu / heparīnu, bivalirudīnu, intravenozus GPIIb / IIIa inhibitorus, lipīdu līmeni pazeminošas zāles, beta blokatorus un angiotenzīnu konvertējošā enzīma inhibitorus. Prasugrela efektivitāte nebija atkarīga no ASS devas (75-325 mg vienu reizi dienā). TRITON pētījumā nebija atļauts lietot perorālos antikoagulantus, antitrombocītu zāles, kas nav pētāmās, un hroniskus NPL. Visā ACS populācijā prasugrels bija saistīts ar zemāku CV nāves gadījumu skaitu. ar nāvējošu insultu, salīdzinot ar klopidogrelu, neatkarīgi no sākotnējām īpašībām, piemēram, vecuma, dzimuma, ķermeņa svara, ģeogrāfiskā reģiona, GPIIb / IIIa inhibitoru lietošanas un stenta veida. Ieguvums galvenokārt bija saistīts ar ievērojamu nāves gadījumu skaita samazināšanos. AMI gadījumi (sk. 3. tabulu) Diabēta slimniekiem ievērojami samazinājās primārie un visi sekundārie kombinētie parametri.
Prasugrela ieguvums, kas novērots ≥ 75 gadus veciem pacientiem, bija mazāks nekā pacientiem ar cukura diabētu, STEMI, palielinātu stenta trombozes vai atkārtotu notikumu risku.
Pacientiem ar TIA anamnēzē vai ar išēmisku lēkmi vairāk nekā 3 mēnešus pirms prasugrela terapijas primārais saliktais mērķis nebija samazinājies.
3. tabula. Pacienti ar klīniskiem rezultātiem TRITON pētījuma primārajā analīzē
Visā ACS populācijā katra sekundārā parametra analīze parādīja būtisku labumu (lpp
Prasugrel bija saistīts ar stenta trombozes samazināšanos par 50% 15 mēnešu novērošanas periodā. Stenta trombozes samazināšanās ar Efient tika novērota gan agri, gan pēc 30 dienām gan metāla, gan ārstnieciskiem stentiem.
Analizējot pacientus, kuri izdzīvoja išēmisku notikumu, prasugrels bija saistīts ar turpmāko primāro mērķa notikumu biežuma samazināšanos (7,8%, lietojot prasugrelu un 11,9%, lietojot klopidogrelu).
Lai gan asiņošana tika palielināta, lietojot prasugrelu, salikta "mērķa analīze", kurā ietilpa nāve no visiem cēloņiem, nāvējošs miokarda infarkts, nāvējošs insults un ar TIMI nesaistīta smaga asiņošana, Efient bija labvēlīga salīdzinājumā ar klopidogrelu (HR 0,87 ; 95% TI, 0,79 līdz 0,95; p = 0,004). TRITON pētījumā uz katriem 1000 pacientiem, kuri tika ārstēti ar Efient, bija par 22 pacientiem ar miokarda infarktu mazāk un vēl 5 pacientiem ar lielu TIMI asiņošanu, kas nebija saistīta ar CABG, salīdzinot ar pacientiem, kuri tika ārstēti ar klopidogrelu.
Farmakodinamikas / farmakogenomikas pētījuma rezultāti, kuros piedalījās 720 Āzijas AKS pacienti, kuriem tika veikta PCI, parādīja, ka ar prasugrelu tiek sasniegts augstāks trombocītu inhibīcijas līmenis nekā ar klopidogrelu un ka 60 mg prasugrela iekraušanas / 10 mg uzturošā deva ir piemērota dozēšanas shēma Āzijas indivīdiem, kuri sver vismaz 60 kg un ir jaunāki par 75 gadiem (skatīt 4.2. apakšpunktu).
30 mēnešus ilgā pētījumā (TRILOGY-ACS), kas tika veikts 9326 medicīniski ārstētiem pacientiem ar ACS UA / NSTEMI, bez revaskularizācijas (nereģistrēta indikācija), prasugrels būtiski nesamazināja MI vai insulta kombinētā CV nāves mērķa biežumu Smagas asiņošanas (TIMI) biežums (ieskaitot nāves risku, letālu iznākumu un intrakraniālu asiņošanu) ar prasugrelu un klopidogrelu ārstētiem pacientiem bija līdzīgs. ≥ 75 gadus veci vai sver mazāk nekā 60 kg (N = 3022) randomizēti 5 mg prasugrela, tāpat kā pacientiem vecumā
05.2 Farmakokinētiskās īpašības
Prasugrels ir priekšzāles un ātri metabolizējas in vivo uz aktīvu metabolītu un neaktīviem metabolītiem. Aktīvo metabolītu iedarbībai (AUC) ir mērena vai zema atšķirība starp pacientiem (27%) un indivīdiem (19%). Prasugrela farmakokinētika ir līdzīga veseliem cilvēkiem, pacientiem ar stabilu aterosklerozi un pacientiem, kuriem tiek veikta perkutāna koronārā iejaukšanās.
Uzsūkšanās
Prasugrela uzsūkšanās un metabolisms ir ātrs, un aktīvā metabolīta maksimālā koncentrācija plazmā (Cmax) tiek sasniegta aptuveni 30 minūtēs. Aktīvā metabolīta (AUC) iedarbība palielinās proporcionāli terapeitiskajai devai. maltīte ar augstu tauku un kaloriju daudzumu nemainīja aktīvo metabolītu, bet Cmax samazinājās par 49% un laiks Cmax (Tmax) sasniegšanai palielinājās no 0, 5 līdz 1,5 stundām. TRITON pētījumā Efient tika lietots neatkarīgi no pārtikas, tāpēc Efient var ievadīt neatkarīgi no pārtikas; tomēr, ievadot prasugrela piesātinošo devu tukšā dūšā, iedarbība var sākties ātrāk (skatīt 4.2. apakšpunktu).
Izplatīšana
Aktīvā metabolīta saistīšanās ar cilvēka seruma albumīnu (4% buferšķīdums) bija 98%.
Vielmaiņa
Pēc perorālas lietošanas plazmrels neparādās plazmā. Zarnās tas ātri hidrolizējas līdz tiolaktonam, ko pēc tam vienā metabolisma posmā citohroms P450, galvenokārt CYP3A4 un CYP2B6, un mazākā mērā - CYP2C9 un CYP2C19 pārvērš par aktīvo metabolītu. Pēc tam aktīvais metabolīts tiek metabolizēts divos savienojumos neaktīvs ar S-metilēšanu vai konjugāciju ar cisteīnu.
Veseliem cilvēkiem, pacientiem ar stabilu aterosklerozi un pacientiem ar AKS, kuri saņēma Efient, nebija būtiskas CYP3A5, CYP2B6, CYP2C9 vai CYP2C19 ģenētiskās variācijas ietekmes uz prasugrela farmakokinētiku vai tās agregācijas inhibīciju.
Eliminācija
Aptuveni 68% prasugrela devas tiek izvadīti ar urīnu un 27% ar izkārnījumiem kā neaktīvi metabolīti. Aktīvā metabolīta eliminācijas pusperiods ir aptuveni 7,4 stundas (2 līdz 15 stundas).
Īpašas populācijas:
Pensionāriem: Pētījumā ar veseliem cilvēkiem vecumā no 20 līdz 80 gadiem vecums būtiski neietekmēja prasugrela farmakokinētiku vai tā radīto trombocītu agregācijas inhibīciju. "Lielajā 3. fāzes klīniskajā pētījumā" ļoti veciem pacientiem (vecums ≥ 75 gadi) aktīvā metabolīta (AUC) iedarbība bija par 19% lielāka nekā pacientiem vecumā
Prasugrel jālieto piesardzīgi ≥ 75 gadus veciem pacientiem, jo šajā populācijā var rasties asiņošanas risks (skatīt 4.2. Un 4.4. Apakšpunktu). Pētījumā, kurā piedalījās pacienti ar stabilu aterosklerozi, vidējā aktīvā metabolīta iedarbība (AUC) pacientiem, kas vecāki par 75 gadiem un lietoja 5 mg prasugrela, bija aptuveni puse no pacientiem, kas vecāki par 75 gadiem.
Aknu mazspēja: Pacientiem ar viegliem vai vidēji smagiem aknu darbības traucējumiem (A vai B klase pēc Child-Pugh) deva nav jāpielāgo. Prasugrela farmakokinētika un tā trombocītu agregācijas inhibīcija bija līdzīga cilvēkiem ar viegliem vai vidēji smagiem aknu darbības traucējumiem, salīdzinot ar veseliem cilvēkiem. Prasugrela farmakokinētika un farmakodinamika pacientiem ar smagiem aknu darbības traucējumiem nav pētīta. To nedrīkst lietot pacientiem ar smagi aknu darbības traucējumi (skatīt apakšpunktu 4. 3).
Nieru mazspēja: Pacientiem ar nieru mazspēju, ieskaitot pacientus ar beigu stadijas nieru slimību (ESRD), devas pielāgošana nav nepieciešama. Prasugrela farmakokinētika un tā trombocītu agregācijas kavēšana ir līdzīga pacientiem ar vidēji smagiem nieru darbības traucējumiem (glomerulārās filtrācijas ātrums (GFR) 30-2) un veseliem cilvēkiem. Prasugrela izraisītas trombocītu agregācijas inhibīcija bija līdzīga. Arī pacientiem ar ESRD, kuriem nepieciešama hemodialīze salīdzinot ar veseliem cilvēkiem, lai gan ESRD pacientiem aktīvā metabolīta Cmax un AUC samazinājās attiecīgi par 51% un 42%.
Ķermeņa masa: Prasugrela aktīvā metabolīta iedarbība (AUC) ir aptuveni par 30 līdz 40% lielāka veseliem cilvēkiem un pacientiem ar ķermeņa masu
Etniskā piederība: Klīniskajos farmakoloģijas pētījumos pēc ķermeņa masas pielāgošanas aktīvā metabolīta AUC ķīniešu, japāņu un korejiešu indivīdiem bija aptuveni par 19% augstāks nekā baltās rases pārstāvjiem, galvenokārt saistībā ar lielāku iedarbību Āzijas indivīdiem ar ķermeņa svaru
Sekss: Veseliem cilvēkiem un pacientiem prasugrela farmakokinētika sievietēm un vīriešiem ir līdzīga.
Pediatriskā populācija: Prasugrela farmakokinētika un farmakodinamika pediatriskā populācijā nav novērtēta (skatīt 4.2. Apakšpunktu).
05.3 Preklīniskie drošības dati
Ne-klīniskajos standartpētījumos iegūtie dati par farmakoloģisko drošību, atkārtotu devu toksicitāti, genotoksicitāti, kancerogēnu potenciālu vai reproduktīvo toksicitāti neliecina par īpašu risku cilvēkam. Ietekme neklīniskos pētījumos tika novērota tikai tad, ja iedarbība tika uzskatīta par pietiekami lielu. maksimālā iedarbība uz cilvēkiem, kas norāda uz zemu atbilstību klīniskai lietošanai.
Toksikoloģiskie pētījumi par žurku un trušu embrija-augļa attīstību neliecināja par prasugrela izraisītām malformācijām. Lietojot ļoti lielu devu (> 240 reizes lielāka par ieteicamo uzturošo dienas devu cilvēkam mg / m2), kas ietekmēja mātes ķermeņa svaru un / vai pārtikas patēriņu, pēcnācēju ķermeņa masa nedaudz samazinājās (salīdzinājumā ar kontrolgrupām) pirms un pēcdzemdību pētījumos ar žurkām, ārstēšana ar mātēm neietekmēja pēcnācēju uzvedības vai reproduktīvo attīstību, lietojot devas, kas līdz 240 reizēm pārsniedza ieteicamo uzturošo dienas devu (izteikta mg / m2).
2 gadus ilgā pētījumā ar žurkām netika novēroti audzēji, kas saistīti ar savienojumiem, un prasugrela ekspozīcija bija vairāk nekā 75 reizes lielāka par ieteicamo terapeitisko ekspozīciju cilvēkiem (pamatojoties uz aktīvā metabolīta un cilvēka metabolītu iedarbību uz cilvēka plazmu). Galvenās apritē). Pelēm, kuras 2 gadus bija pakļautas lielām devām (> 75 reizes lielākas par cilvēka iedarbību), bija "palielināts audzēju (hepatocelulāru adenomu) sastopamības biežums, bet tas tika uzskatīts par sekundāru prasugrela izraisītas enzīmu indukcijas dēļ. L" Grauzējiem raksturīga aknu saistība audzēji un zāļu izraisīta enzīmu indukcija ir labi dokumentēta literatūrā. Aknu audzēju palielināšanās, ievadot pelēm prasugrelu, netiek uzskatīts par būtisku risku cilvēkiem.
06.0 FARMACEITISKĀ INFORMĀCIJA
06.1 Palīgvielas
Planšetdatora kodols:
Mikrokristāliskā celuloze
Mannīts (E421)
Nātrija kroskarmeloze
Hipromeloze (E464)
Magnija stearāts
Pārklājums:
Laktozes monohidrāts
Hipromeloze (E464)
Titāna dioksīds (E171)
Triacetīns (E1518)
Sarkanais dzelzs oksīds (E172)
Dzeltenais dzelzs oksīds (E172)
Talks
6.2 Nesaderība
Nav piemērojams.
06.2 Nesaderība
2 gadi.
06.3 Derīguma termiņš
2 gadi.
06.4 Īpaši uzglabāšanas nosacījumi
Šīm zālēm nav nepieciešama īpaša uzglabāšanas temperatūra. Uzglabāt oriģinālajā iepakojumā, lai pasargātu no gaisa un mitruma.
06.5 Tiešā iepakojuma veids un iepakojuma saturs
Alumīnija blisteri kastītēs pa 14, 28, 30, 30 (x1), 56, 84, 90 (x1) un 98 tabletēm.
Visi iepakojuma lielumi tirgū var nebūt pieejami.
06.6 Norādījumi lietošanai un lietošanai
Nav īpašu norādījumu.
07.0 REĢISTRĀCIJAS APLIECĪBAS ĪPAŠNIEKS
Eli Lilly Nederland BV, Grootslag 1-5, NL-3991 RA Houten, Nīderlande.
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS
EU/1/08/503/008
039055088
EU/1/08/503/009
039055090
EU/1/08/503/010
039055102
EU/1/08/503/011
039055114
EU/1/08/503/012
039055126
EU/1/08/503/013
039055138
EU/1/08/503/014
039055140
EU/1/08/503/016
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS
Reģistrācijas datums: 2009. gada 25. februāris
Pēdējais atjaunošanas datums:
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS
11.0 RADIOZĀLĒM, PILNĪGI DATI PAR IEKŠĒJO RADIĀCIJAS DOSIMETRIJU
12.0 RADIOZĀLĒM, PAPILDU SĪKĀKI NORĀDĪJUMI PAR ĪSTENAJU SAGATAVOŠANU UN KVALITĀTES KONTROLI
VIENOJĀS ar EIROPAS ZĀĻU AĢENTŪRU (EMA) UN ITĀLIJAS Narkotiku aģentūru (AIFA)
2013. gada decembris
Paaugstināts smagas asiņošanas risks pacientiem ar nestabilu stenokardiju / miokarda infarktu (UA) / bez ST segmenta pacēlumu / NSTEMI, ja pirms diagnostikas koronāro angiogrāfijas tiek ievadīts EFIENT (prasugrels).
Cienījamais ārsts, cienījamais ārsts,
"Eiropas Zāļu aģentūra un Itālijas Zāļu aģentūra - AIFA, vienojoties ar Daiichi -Sankyo un Eli Lilly Italia, vēlas jūs informēt par šādu ieteikumu par EFIENT (prasugrela) - antitrombocītu zāles, kas paredzētas akūtu slimību ārstēšanai - lietošanu koronāro sindromu (AKS) pacientiem, kuriem tiek veikta perkutāna koronārā iejaukšanās (PCI):
Pacientiem ar nestabilu stenokardiju / miokarda infarktu (UA) / bez ST segmenta pacēlumu / NSTEMI, ja koronāro angiogrāfiju veic 48 stundu laikā pēc hospitalizācijas, EFIENT piesātinošā deva jāievada tikai PCI laikā, lai mazinātu risku no asiņošanas.
Šis ieteikums ir balstīts uz nesen pabeigta klīniskā pētījuma rezultātiem ar NSTEMI pacientiem, kuriem plānota koronārā angiogrāfija 2 līdz 48 stundas pēc randomizācijas. Pētījumā tika salīdzināta sākotnējās 30 mg prasugrela piesātinošās devas ievadīšanas ietekme pirms koronāro angiogrāfijas (vidēji 4 stundas), kam sekoja "papildu 30 mg deva PCI laikā, un efekts, ko radīja pilnīga ievadīšana". piesātinošā deva 60 mg PCI laikā. Rezultāti parādīja lielāku asiņošanas risku, kas saistīts ar sākotnējās piesātinošās devas lietošanu pirms koronāro angiogrāfijas, kam sekoja papildu deva PCI laikā, salīdzinot ar vienu prasugrela piesātinošo devu PCI laikā. starp abām dozēšanas shēmām.
"ACCOAST" pētījums ar nosaukumu: Prasugrel salīdzinājums perkutānas koronārās iejaukšanās laikā vai kā iepriekšēja ārstēšana diagnozes laikā pacientiem ar miokarda infarktu, kam nav ST līmeņa paaugstināšanās.
Uzziniet vairāk par drošības aspektiem
ACCOAST bija 30 dienu pētījums, kurā piedalījās 4033 pacienti ar NSTEMI un paaugstinātu troponīna līmeni, kuriem bija plānota koronārā angiogrāfija, kam sekoja PCI 2 līdz 48 stundas pēc randomizācijas. Pacientiem, kuri saņēma prasugrela piesātinošo devu 30 mg vidēji 4 stundas pirms koronārās angiogrāfijas, kam sekoja piesātinošā deva 30 mg PCI laikā (n = 2037), bija paaugstināts perioperatīvās asiņošanas risks. (nav saistīts ar koronāro artēriju šuntēšanas operāciju) un nav papildu ieguvuma salīdzinājumā ar pacientiem, kuri PCI laikā saņēma piesātinošo devu 60 mg (n = 1996). Konkrēti, indivīdiem netika ievērojami samazināts kardiovaskulāro nāves gadījumu, miokarda infarkta, insulta, steidzamas revaskularizācijas vai glikoproteīna (GP) IIb / IIIa inhibitora lietošanas "glābšanas terapijā" biežums 7 dienu laikā pēc randomizācijas. kas saņēma prasugrelu pirms koronāro angiogrāfijas, salīdzinot ar pacientiem, kuri PCI laikā saņēma pilnu prasugrela piesātinošo devu. Turklāt galvenā drošības mērķa biežums, ko attēloja visas galvenās asiņošanas saskaņā ar TIMI (CABG un ne-CABG notikumi) 7 dienu laikā pēc randomizācijas visiem ārstētajiem, bija ievērojami lielāks pacientiem, kuri saņēma prasugrelu divās dalītās devās (4 stundas pirms koronāro angiogrāfijas un PCI laikā), salīdzinot ar pacientiem, kuri PCI laikā saņēma pilnu prasugrela piesātinošo devu vienreizējai lietošanai.
Ziņošana par iespējamām nevēlamām reakcijām
Ārstiem un citiem veselības aprūpes speciālistiem ir jāziņo par visām iespējamām blakusparādībām, kas saistītas ar prasugrelu saturošām zālēm.
Ārstiem un citiem veselības aprūpes speciālistiem saskaņā ar likumu ir jānosūta ziņojumi par iespējamām blakusparādībām, izmantojot speciālu papīra veidlapu (pieejama vietnē http://www.agenziafarmaco.gov.it/sites/default/files/tipo_filecb84.pdf) vai nekavējoties tiešsaistē aizpildot elektronisko veidlapu (http://www.agenziafarmaco.gov.it/sites/default/files/scheda_aifa_oper_sanitario16.07.2 012.doc), tās veselības aprūpes iestādes, kurai tie pieder, farmakovigilances vadītājam vai , ja darbojas privātajās veselības iestādēs, ar Veselības departamenta starpniecību - šajā jomā kompetentajam ASL farmakovigilances vadītājam.
Papildu informācija
Jautājumu un / vai papildu informācijas gadījumā, lūdzu, sazinieties ar Eli Lilly "Medicīniskās informācijas" biroju, zvanot uz šādu bezmaksas numuru: 800117678 vai rakstot uz šādu adresi: [email protected]
Ziņojumi par iespējamām zāļu nelabvēlīgām reakcijām jānosūta tās struktūras farmakovigilances vadītājam, kurai pieder operators.
Šī informatīvā piezīme ir publicēta arī AIFA tīmekļa vietnē (www.agenziafarmaco.it), kuras regulāra apspriešanās ir ieteicama, lai iedzīvotājiem sniegtu vislabāko profesionālo un pakalpojumu informāciju.





















.jpg)