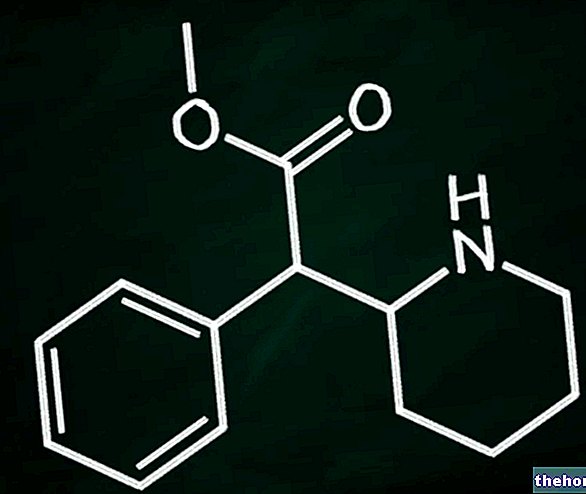
Kas ir Aubagio - teriflunomide un kādam nolūkam to lieto?
Aubagio ir zāles, kas satur aktīvo vielu teriflunomīdu. Tas ir indicēts pieaugušo ārstēšanai ar multiplo sklerozi (MS), slimību, kurā "iekaisums iznīcina nervu apvalku pārklājušo aizsargpārklājumu. Aubagio ir indicēts multiplās sklerozes veidā, kas pazīstams kā" recidivējoši remitējošs "(ti. kad pacients cieš no simptomu paasinājumiem (recidīviem), kam seko atveseļošanās periodi (remisijas)).
Kā lieto Aubagio?
Aubagio var iegādāties tikai pret recepti, un ārstēšana jāsāk un jāuzrauga ārstam, kam ir pieredze multiplās sklerozes ārstēšanā. Aubagio ir pieejams tablešu veidā (14 mg). Ieteicamā deva ir 14 mg vienu reizi dienā.
Kā Aubagio - teriflunomīds darbojas?
Multiplās sklerozes gadījumā ķermeņa imūnsistēma nedarbojas pareizi un uzbrūk dažām centrālās nervu sistēmas daļām (veidojas smadzenēs un muguras smadzenēs), izraisot iekaisumu, kas bojā nervu apvalkus. Aubagio aktīvā viela teriflunomīds bloķē enzīmu, ko sauc par “dihidroorotāta dehidrogenāzi”, kas nepieciešams šūnu proliferācijai. Precīzs teriflunomīda darbības mehānisms multiplās sklerozes gadījumā nav zināms, taču tiek uzskatīts, ka tas samazina limfocītu skaitu, kas veido imūnsistēmas daļu un ir iesaistīti iekaisuma procesā. Samazinot limfocītus, samazinās iekaisums un ir vieglāk kontrolēt multiplās sklerozes simptomus.
Kāds ir Aubagio - teriflunomide iedarbīgums šajos pētījumos?
Aubagio tika pētīts četros pamatpētījumos, iesaistot vairāk nekā 2700 pieaugušos ar recidivējoši remitējošu multiplo sklerozi. Pētījumā, kurā piedalījās 179 pacienti, Aubagio iedarbība tika salīdzināta ar placebo (viela, kas neietekmē ķermeni) iedarbību, pārbaudot aktīvo bojājumu (bojāto zonu) skaitu, izmantojot smadzeņu magnētiskās rezonanses attēlveidošanu. Efektīvāka nekā placebo. : pēc aptuveni 9 mēnešiem (36 nedēļām) katra skenēšana atklāja aptuveni 1 aktīvu bojājumu pacientiem, kuri tika ārstēti ar Aubagio, salīdzinot ar aptuveni 2,7 aktīviem bojājumiem pacientiem, kuri tika ārstēti ar placebo. gada recidīvu rādītājs), salīdzinot ar placebo. Ārstēšana ilga ne vairāk kā trīs gadus (152 nedēļas). Aubagio bija efektīvāks par placebo: pacientiem, kuri tika ārstēti ar Aubagio, recidīvu samazināšanās bija aptuveni par 30% lielāka nekā pacientiem, kuri tika ārstēti ar placebo (Aubagio gadījumā gada recidīvu biežums bija 0,35, bet placebo gadījumā - 0,53). Pētījumos tika pārbaudīta arī Aubagio ietekme uz izmaiņām pacientu invaliditātes pakāpē, parādot, ka invaliditātes pasliktināšanās risks bija par 30% mazāks nekā tas, kas tika iegūts ar placebo pēc aptuveni divarpus gadu (132 nedēļas) ārstēšanas. , kurā piedalījās 324 pacienti, salīdzināja Aubagio un beta-1a interferona (cita multiplās sklerozes ārstēšana) ietekmi uz ārstēšanas neveiksmes ātrumu, izmērot laiku līdz pirmajam recidīvam vai līdz pārtraukšanai. Pētījums ilga līdz diviem gadiem. Pētījuma rezultāti neļāva izdarīt galīgus secinājumus. Pacientiem, kuri tika ārstēti ar Aubagio, tika novērota pastāvīga pārtraukšana 13,5% gadījumu, salīdzinot ar 24% pacientu, kuri tika ārstēti ar beta-1a interferonu. Tomēr recidīvu biežums bija 23,4%, lietojot Aubagio, salīdzinot ar 15,4% ar beta-1a interferonu. Kopumā no šī pētījuma nevarēja izdarīt secinājumus par atšķirībām starp Aubagio un beta-1a interferonu multiplās sklerozes ārstēšanā.
Kāds pastāv risks, lietojot Aubagio - teriflunomide?
Visbiežāk novērotās Aubagio blakusparādības (kas var skart vairāk nekā 1 no 10 cilvēkiem) ir gripa, augšējo elpceļu infekcija (saaukstēšanās), urīnceļu infekcija (ti, urīna nesošās struktūras), parestēzija (neparastas sajūtas, piemēram, tirpšana un dūrieni), caureja, paaugstināts aknu enzīmu līmenis, slikta dūša un alopēcija (matu izkrišana) .Kopumā caureja, slikta dūša un alopēcija ir vieglas vai vidēji smagas, laika gaitā izzūd un parasti nav jāpārtrauc ārstēšana. Pilnu Aubagio izraisīto blakusparādību sarakstu skatīt lietošanas instrukcijā. Aubagio nedrīkst lietot pacientiem:
- cieš no smagas aknu slimības;
- smagos imūndeficīta stāvokļos, piemēram, iegūtā imūndeficīta sindromā (AIDS);
- ar traucētu kaulu smadzeņu darbību vai zemu asins šūnu (sarkano asins šūnu, balto asins šūnu vai trombocītu) skaitu;
- ar smagām infekcijām;
- ar smagiem nieru darbības traucējumiem, kuriem nepieciešama dialīze; ar smagu hipoproteinēmiju (asins olbaltumvielu samazināšanās).
Aubagio nedrīkst lietot arī grūtnieces vai sievietes, kas baro bērnu ar krūti. Sievietes reproduktīvā vecumā nedrīkst lietot Aubagio, neizmantojot uzticamus kontracepcijas līdzekļus. Pilnu ierobežojumu sarakstu skatīt lietošanas instrukcijā.
Kāpēc Aubagio - teriflunomide tika apstiprinātas?
Aģentūras Cilvēkiem paredzēto zāļu komiteja (CHMP) nolēma, ka ieguvums, lietojot Aubagio, pārsniedz šo zāļu radīto risku, un ieteica to apstiprināt lietošanai ES. Lai aizkavētu invaliditātes progresēšanu pacientiem ar recidivējoši-remitējošu multiplo sklerozi. Lai gan zāles bija pieticīgas, tās tika uzskatītas par nozīmīgām un līdzīgām citām multiplās sklerozes terapijām, lai gan nebija iespējams izdarīt stingrus secinājumus, salīdzinot tieši ar beta-1a interferonu. Aubagio lieto iekšķīgi, kas tika uzskatīts par priekšrocību salīdzinājumā ar citām zālēm, piemēram, beta-1a interferonu. Kas attiecas uz drošību, blakusparādības bija līdzīgas tām, kas novērotas, lietojot imūnsupresantu. leflunomīds, jo leflunomīds organismā tiek pārveidots par teriflunomīdu. Nopietnu blakusparādību risks organismā. aknas un muguras smadzenes tiek uzskatītas par pārvaldāmām un atbilstoši ierobežotas ar riska samazināšanas pasākumiem.
Kas tiek darīts, lai nodrošinātu nekaitīgu un efektīvu Aubagio -teriflunomide lietošanu?
Lai nodrošinātu pēc iespējas drošāku Aubagio lietošanu, ir izstrādāts riska pārvaldības plāns. Pamatojoties uz šo plānu, Aubagio zāļu aprakstam un lietošanas instrukcijai ir pievienota drošības informācija, ieskaitot atbilstošus piesardzības pasākumus, kas jāievēro veselības aprūpes speciālistiem un pacientiem. Turklāt uzņēmumam, kas ražo Aubagio, ir jānodrošina, lai visi veselības aprūpes speciālisti, kas varētu lietot Aubagio, saņemtu informācijas paketi, kas satur svarīgu drošības informāciju, tostarp testus un pārbaudes, kas pacientiem jāiziet pirms un pēc terapijas uzsākšanas. Iepakojumā būs arī informācija par reģistru, ko uzņēmums izveidos, lai apkopotu datus par bērniem, kas dzimuši sievietēm, kuras ārstētas ar Aubagio, kā arī atgādinājumu pacientiem ar būtisku drošības informāciju.
Cita informācija par Aubagio - teriflunomīdu
Eiropas Komisija 2013. gada 26. augustā izsniedza Aubagio reģistrācijas apliecību, kas derīga visā Eiropas Savienībā. Pilnu Aubagio EPAR versiju skatiet aģentūras tīmekļa vietnē: ema.Europa.eu / Find medicine / Human medicines / European publiski novērtējuma ziņojumi Lai iegūtu vairāk informācijas par Aubagio terapiju, izlasiet lietošanas instrukciju (pievienota EPAR) vai sazinieties ar savu ārstu vai farmaceitu. Pēdējais šī kopsavilkuma atjauninājums: 08-2013.
Šajā lapā publicētā informācija par Aubagio -teriflunomīdu var būt novecojusi vai nepilnīga. Lai pareizi izmantotu šo informāciju, skatiet atrunu un noderīgas informācijas lapu.











-non-sentire-gli-odori.jpg)