Aktīvās sastāvdaļas: Podofilotoksīns
Condyline 0,5% ādas šķīdums
Indikācijas Kāpēc lieto Condyline? Kam tas paredzēts?
Condyline satur aktīvo vielu podofilotoksīnu, ekstraktu, kas nāk no auga un pieder zāļu grupai, ko sauc par "pretvīrusu līdzekļiem".
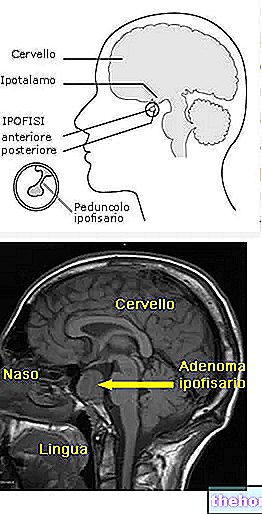
Condyline ir aktuāls medikaments, kas paredzēts dažu veidu kārpu ārstēšanai, kas veidojas uz ārējās ādas dzimumorgānu apvidū (ārējās asās kārpas).
Konsultējieties ar ārstu, ja pēc plānotā ārstēšanas perioda nejūtaties labāk vai jūtaties sliktāk.
Kontrindikācijas, kad Condyline nedrīkst lietot
Nelietojiet Condyline
- ja Jums ir alerģija pret podofilotoksīnu vai kādu citu (6. punktā minēto) šo zāļu sastāvdaļu;
- bērniem
- ja esat grūtniece (skatīt sadaļu "Grūtniecība un zīdīšanas periods")
- ja barojat bērnu ar krūti (skatīt sadaļu "Grūtniecība un zīdīšanas periods")
- ja lietojat citas zāles, kas satur podofilīnu.
Piesardzība lietošanā Kas jāzina pirms Condyline lietošanas
Pirms Condyline lietošanas konsultējieties ar ārstu vai farmaceitu.
- Izvairieties no Condyline šķīduma saskares ar gļotādu vai veselu ādu kārpu tuvumā vai pamatnē, jo tas var izraisīt lokālu kairinājumu un / vai gļotādas vai veselas ādas bojājumus. Lai izvairītos no nejaušas veselīgas zonas saskares ar Condyline šķīdumu pirms ārstēšanas uzsākšanas, jūs varat aizsargāt veselīgo zonu, uzklājot neitrālu ziedi vai krēmu, kura pamatā ir vazelīns vai cinka oksīds.
- Izvairieties no šo zāļu saskares ar acīm, jo tas var izraisīt nopietnu kairinājumu. Ja tas notiek nejauši, nekavējoties ilgstoši izskalojiet acis ar ūdeni un konsultējieties ar ārstu.
- Izvairieties lietot šīs zāles lielās platībās, jo tas var izraisīt blakusparādības, kas ietekmē dažādus ķermeņa orgānus.
- Ja esat sieviete un šo zāļu lietošana ir sarežģīta, jo brūce nav pieejama pašārstēšanai, sazinieties ar savu ārstu, lai lietotu Condyline.
- Ja pēc noteiktā ārstēšanas perioda šo zāļu iedarbība nav acīmredzama, ārsts apsvērs alternatīvas terapijas metodes.
Bērni
Condyline nav paredzēts lietošanai bērniem.
Mijiedarbība Kādas zāles vai pārtikas produkti var mainīt Condyline iedarbību
Citas zāles un Condyline
Pastāstiet ārstam vai farmaceitam par visām zālēm, kuras lietojat, pēdējā laikā esat lietojis vai varētu lietot. Īpaši pastāstiet ārstam, ja lietojat kādas citas zāles, kas satur podofilīnu, jo šajā gadījumā šīs zāles nevar lietot (skatīt sadaļu "Nelietojiet Condyline šādos gadījumos").
Brīdinājumi Ir svarīgi zināt, ka:
Grūtniecība un zīdīšanas periods
Nelietojiet Condyline, ja esat grūtniece, domājat, ka Jums varētu būt iestājusies grūtniecība vai barojat bērnu ar krūti.
Transportlīdzekļu vadīšana un mehānismu apkalpošana
Šīs zāles neietekmē spēju vadīt transportlīdzekļus un apkalpot mehānismus.
Deva, lietošanas veids un laiks Kā lietot Condyline: Devas
Vienmēr lietojiet šīs zāles tieši tā, kā ārsts vai farmaceits Jums teicis. Ja rodas šaubas, konsultējieties ar ārstu vai farmaceitu.
Pieaugušie
Ieteicamā deva ir viena lietošana divas reizes dienā, no rīta un vakarā.
Ārstēšanas ilgums
Lietojiet šīs zāles no rīta un vakarā 3 dienas pēc kārtas. Ārstēšanas shēmu var atkārtot katru nedēļu ne ilgāk kā 5 nedēļas pēc kārtas, atstājot 4 dienu intervālu starp vienu un otru nedēļu bez ārstēšanas.Zāles jālieto īsu laiku un ārsta uzraudzībā.
Norādījumi pareizai lietošanai
- Pudelei ir "bērniem droša" drošības aizdare. Lai atvērtu pudeli, nospiediet vāciņu un vienlaikus atskrūvējiet bultiņas norādītajā virzienā (kā parādīts attēlā).
- Uzklājiet šķīdumu uz apstrādājamās ādas vietas, izmantojot vienu no iepakojumā esošajiem aplikatoriem, izvairoties no saskares ar veselīgu ādu (skatīt punktu "Brīdinājumi un piesardzība lietošanā").
- Pēc uzklāšanas ļaujiet šķīdumam nožūt gaisā, lai šķīdums nesaskartos ar veselām vietām, īpaši, ja kārpas atrodas uz priekšādiņas (ādas kroka, kas sedz dzimumlocekļa galu vīriešiem).
- Pēc uzklāšanas izmetiet izmantoto aplikatoru un rūpīgi nomazgājiet rokas.
- Pēc lietošanas aizveriet vāciņu. Pudele ir aizvērta pret bērniem neatveramu, ja, atskrūvējot vāciņu, nespiežot, dzirdat klikšķi.
Pārdozēšana Ko darīt, ja esat lietojis pārāk daudz Condyline
Ja esat lietojis Condyline vairāk nekā noteikts
Lietojot pārāk daudz Condyline, nav ziņots par blakusparādībām. Tomēr, ja nejauši esat lietojis Condyline vairāk nekā noteikts un rodas jebkādas blakusparādības, nekavējoties sazinieties ar savu ārstu vai tuvāko slimnīcu. Jūsu ārsts to veiks. Atbilstoša atbalstoša aprūpe.
Ja esat aizmirsis lietot Condyline
Nelietojiet dubultu devu, lai aizvietotu aizmirsto devu.
Ja pārtraucat lietot Condyline
Ja jums ir kādi jautājumi par šo zāļu lietošanu, jautājiet savam ārstam vai farmaceitam.
Blakusparādības Kādas ir Condyline blakusparādības?
Tāpat kā citas zāles, šīs zāles var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas.
Vietējās blakusparādības galvenokārt rodas otrajā vai trešajā ārstēšanas dienā, kad sākas kārpu nāve. Parasti blakusparādības ir vieglas un labi panesamas.
Turpmāko blakusparādību biežums nav zināms.
Nevēlamās blakusparādības, kas ietekmē ādu un gļotādas
- eritēma (ādas kairinājums) ar vieglām sāpēm un / vai virspusējiem ādas bojājumiem apstrādātajā zonā. Šajā gadījumā Condyline lietošana var būt sāpīga
- tūska (pietūkums) un balanopostīts (dzimumlocekļa ekstremitāšu infekcija). Šis efekts rodas lielu kārpu gadījumā priekšādiņas dobumā
Nepareiza produkta uzklāšanas gadījumā var rasties arī:
- kuņģa un zarnu darbības traucējumi
- leikopēnija (samazināts balto asins šūnu skaits asinīs)
- trombocitopēnija (trombocītu skaita samazināšanās asinīs)
- izmaiņas aknu darbībā
- izmaiņas nieru darbībā
- perifērās neiropātijas (perifērās nervu sistēmas slimības)
- parasti mēreni maņu traucējumi (viegls garīgs apjukums), šie efekti var progresēt un kļūt sarežģīti ar nopietnākiem attēliem, kas ietekmē centrālo nervu sistēmu.
Ziņošana par blakusparādībām
Ja Jums rodas jebkādas blakusparādības, konsultējieties ar ārstu, ieskaitot visas iespējamās blakusparādības, kas nav minētas šajā instrukcijā. Jūs varat ziņot par blakusparādībām arī tieši, izmantojot valsts ziņošanas sistēmu vietnē www.agenziafarmaco.gov.it/it/responsabili. Ziņojot par blakusparādībām, jūs varat palīdzēt iegūt vairāk informācijas par šo zāļu drošumu.
Derīguma termiņš un saglabāšana
Uzglabāt šīs zāles bērniem neredzamā un nepieejamā vietā.
Uzglabāt temperatūrā līdz 25 ° C.
Nelietot šīs zāles pēc derīguma termiņa beigām, kas norādīts uz kastītes pēc “Derīgs līdz”. Derīguma termiņš attiecas uz norādītā mēneša pēdējo dienu.
Neizmetiet zāles kanalizācijā vai sadzīves atkritumos. Jautājiet farmaceitam, kā izmest zāles, kuras vairs nelietojat. Tas palīdzēs aizsargāt vidi.
Sastāvs un zāļu forma
Iepakojuma saturs un cita informācija
- aktīvā sastāvdaļa ir: podofilotoksīns (1 ml šķīduma satur 5 mg podofilotoksīna)
- citas sastāvdaļas ir: pienskābe, nātrija laktāts, bezūdens etanols, ūdens.
Condyline ārējā izskata apraksts un iepakojums
Condyline tiek ražots šķīdumā vietējai lietošanai, iepakots pudelē ar 3,5 ml šķīduma.
Kastītē ir divi iepakojumi ar 15 aplikatoriem, kas nepieciešami terapijai.
Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī. Pašlaik pieejamā informācija var nebūt atjaunināta.
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija.
01.0 ZĀĻU NOSAUKUMS
CONDYLINE® 0,5% ĀDAS RISINĀJUMS
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS
1 ml satur: 5 mg podofilotoksīna.
03.0 ZĀĻU FORMA
Ādas šķīdums.
04.0 KLĪNISKĀ INFORMĀCIJA
04.1 Terapeitiskās indikācijas
Ārējo akuminēto kārpu lokāla ārstēšana.
04.2 Devas un lietošanas veids
Uzklājiet šķīdumu uz kārpas, izmantojot vienu no iepakojumā esošajiem aplikatoriem, izvairoties no saskares ar veselīgu ādu.
Lietošana jāveic divas reizes dienā, no rīta un vakarā, 3 dienas pēc kārtas.Šo ārstēšanas shēmu var atkārtot katru nedēļu līdz maksimāli 5 nedēļām pēc kārtas, atstājot 4 dienu intervālu bez ārstēšanas starp vienu un otru nedēļu.
Pēc šķīduma uzklāšanas ļauj tam labi nožūt gaisā, lai tas neizplatītos uz vietām, kuras slimība nav skārusi; it īpaši, ja kārpas ir lokalizētas priekšādiņā.
Pēc uzklāšanas izmetiet izmantoto aplikatoru un rūpīgi nomazgājiet rokas.
04.3 Kontrindikācijas
Zināma paaugstināta jutība pret sastāvdaļām.
Condyline lietošana bērniem un sievietēm grūtniecības un zīdīšanas laikā ir kontrindicēta. Tās lietošana ir kontrindicēta arī kopā ar podofilīna saturošiem līdzekļiem.
04.4 Īpaši brīdinājumi un piesardzība lietošanā
Produkts jālieto īsu laiku un ārsta uzraudzībā.
Preparāta uzklāšana uz samērā lielām gļotām virsmām var izraisīt sistēmiskas reakcijas, tāpēc no tā jāizvairās.
Kondilīns nedrīkst nonākt acīs, jo tas var izraisīt smagas kairinošas izpausmes. Ja tas notiek nejauši, nekavējoties ilgstoši izskalojiet acis ar ūdeni un konsultējieties ar ārstu.
Uzglabāt bērniem nepieejamā un neredzamā vietā.
Sievietēm, kurām bojājums nav pieejams pašārstēšanai, ārstēšana jāveic tiešā ārsta uzraudzībā.
Vietējās kairinošās izpausmes un / vai čūlas uz gļotādas vai veselas ādas tuvumā vai kārpu pamatnē, ko nejauši izraisa saskare ar Condyline šķīdumu, var izvairīties, aizsargājot veselo zonu ar neitrālu ziedi vai krēmu. , pamatojoties uz vazelīnu vai cinka oksīdu, jāpielieto pirms apstrādes ar Condyline.
Ja pēc plānotā ārstēšanas perioda preparāta efektivitāte nav acīmredzama, jāapsver alternatīvas terapijas metodes.
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi
Nelietojiet Condyline terapijas laikā ar produktiem, kas satur podofilīnu.
04.6 Grūtniecība un zīdīšana
Nelietojiet Condyline grūtniecības un zīdīšanas laikā.
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus
Zāles neietekmē spēju vadīt transportlīdzekļus un apkalpot mehānismus.
04.8 Nevēlamās blakusparādības
Vietējās sekundārās reakcijas rodas galvenokārt kopā ar optimālo terapeitisko efektu, galvenokārt otrajā vai trešajā ārstēšanas dienā, kad sākas kārpu nekroze. Šīs sekundārās reakcijas parasti rodas viegli, un pacienti tās labi panes, ja pirms terapijas uzsākšanas tās ir brīdinājis ārsts. Paredzams, ka apstrādātajā zonā var parādīties eritēma ar nelielu jutīgumu un / vai virspusēju čūlu veidošanos epitēlijā, un tāpēc Condyline lietošana var būt sāpīga.
Tūska un balanopostīts novērots dažiem pacientiem ar lielām kārpām priekšādiņas dobumā.
Nepareiza produkta lietošana var izraisīt sistēmiskas uzsūkšanās izpausmes, piemēram, kuņģa -zarnu trakta darbības traucējumus, leikopēniju, trombocitopēniju, aknu vai nieru darbības izmaiņas, perifērās neiropātijas, parasti nelielus maņu traucējumus (vieglu garīgu apjukumu), bet var progresēt un sarežģīt nopietnākus gadījumus kas ietekmē CNS.
04.9 Pārdozēšana
Nav ziņots par podofilotoksīna pārdozēšanas izraisītajām blakusparādībām. Šādu ietekmi nevajadzētu sagaidīt, pareizi lietojot Condyline, ņemot vērā preparāta lielo drošības rezervi.
Tomēr, ja rodas sistēmiskas pārdozēšanas sekas, īstenojiet terapeitiskus pasākumus, kas līdzīgi tiem, kas paredzēti podofilīna pārdozēšanas gadījumā, lai kontrolētu simptomus (vemšanu un krampjus); spiediens un diurēze ir rūpīgi jāuzrauga, paturot prātā, ka akūtas saindēšanās ar podofilīnu gadījumā var būt norādīta šķidruma atjaunošana un hemoperfūzija.
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS
05.1 Farmakodinamiskās īpašības
Podofilotoksīns, Condyline aktīvā sastāvdaļa, ķīmiski pieder lignānu grupai.
ATĶ kods: D06BB04.
Tā ir podofilīna galvenā terapeitiskā sastāvdaļa, no kuras to iegūst, izmantojot īpašu ekstrakcijas procesu, kas nodrošina augstu produkta tīrības pakāpi un standartizāciju. Podofilotoksīnam piemīt izteikta antimitotiska un citolītiska aktivitāte, kas ātri izraisa asu kārpu nekrozi. Podofilotoksīna aktivitāte tiek veikta ātrāk un efektīvāk nekā podofilīna, pateicoties tā augstajai tīrības pakāpei un standartizācijai. Tas ļauj ievadīt atbilstošas devas ar zemāku blakusparādību risku un ļauj ārstēt pacientu mājās ar augstu izārstēšanas ātrumu.
05.2 "Farmakokinētiskās īpašības
Akūta toksicitāte
Akūtās toksicitātes pētījumi parādīja, ka perorāla vienas podofilotoksīna devas, kas ir mazāka par 25 mg / kg, lietošana žurkām un pelēm nav toksiska.
Podofilotoksīna akūtā toksicitāte ir pētīta daudzām dzīvnieku sugām un dažādos ievadīšanas veidos.
LD50 pelēm ir 40 mg / kg (perorāli), no 19 līdz 33 mg / kg intravenozi, 31 mg / kg subkutāni un 4,6 mg / kg intravenozi; žurkām tas ir 14 mg / kg subkutāni, 3 mg / kg intramuskulāri un 15 mg / kg intramuskulāri; trušiem 5 mg / kg intravenozi; sunim subkutāni no 10 līdz 30 mg atkarībā no ķermeņa svara.
Akūtas toksicitātes pētījumi ilgstošai epikutānai uzklāšanai 24 stundas (robežpārbaudes) Condyline devā 2 ml / kg ķermeņa svara (kas atbilst podofilotoksīnam 10 mg / kg) pelēm un žurkām uz muguras (pēdējās zemāk) oklūzija), ir pierādījuši, ka produktam nav sistēmiskas toksicitātes.
Subakūtas vai hroniskas toksicitātes pētījumi
Pēc epikutānas lietošanas pelēm divas reizes nedēļā 74 nedēļas 2,5% podofilotoksīna šķīduma polietilēnglikolā uz 2,5 cm2 lielas muguras zonas tika konstatēts, ka pēc 29 ārstēšanas nedēļām mirušo skaits bija 0/ 25, pēc 50 nedēļām tas bija 5/25 un pēc 74 nedēļām pieauga līdz 12/25 (48%).
Izmantotā deva bija 50 mcl, kas atbilst aptuveni 1,25 mg uz vienu peli.
Ņemot vērā ķermeņa masu 20 g, lietotā lokālā deva ir ekvivalenta 62,5 mg / kg.
Cilvēkiem Condyline 0,5% tika lietots apmēram 10-100 mcl devās, kas atbilst 0,0007-0,007 mg / kg.
Tā kā Condyline ir aktuāls produkts, Magnusona-Klingmana "maksimizācijas tests" tika veikts jūrascūciņām, izmantojot 0,5% podofilotoksīna propilēnglikolā un 0,01% līdz 0,5% šķīdumus indukcijas fāzē.
Provokācijas tests ar 0,1% un 0,5% koncentrāciju izraisīja nealerģisku kairinošu reakciju.
Nevienā no eksperimentiem nebija alerģisku reakciju.
Vietējais kairinošais efekts pēc atkārtotas lietošanas (2 reizes dienā 10 dienas) ar 0,01%, 0,05%, 0,1% un 0,5% podofilotoksīna šķīdumiem 70% etanolā tika pētīts trušiem (salīdzinājumā ar kontroles grupu, kas tika ārstēta tikai ar 70% etanolu). ), gan izmērot ādas krokas biezumu, gan vizuāli novērtējot tādus parametrus kā eritēma, eksudācija un garozas klātbūtne.
Rezultāti parādīja lineāru korelāciju starp podofilotoksīna koncentrācijas palielināšanos un krokas biezuma palielināšanos, kā arī eksponenciālu saistību starp zāļu koncentrācijas palielināšanos un ādas reakciju.
Podofilotoksīns ir embriotoksisks, bet tam nav kancerogēnas vai mutagēnas aktivitātes.
05.3 Preklīniskie drošības dati
Farmakokinētikas pētījumi ar marķētu podofilotoksīnu tika veikti veselām pelēm, kurām bija audzējs. Pēc 4 stundu subkutānas ievadīšanas lielākā daļa radioaktivitātes bija vienādi sadalīta zarnās un urīnā, bet tikai pēdas bija aknās, žultspūslī un nierēs, kā arī smadzenēs, virsnieru garozā un sēkliniekos. Pelēm ar sarkomu 180 lielākā daļa radioaktivitātes tika konstatēta urīnā.
Pēdējiem dzīvniekiem podofilotoksīna eliminācija bija daudz ātrāka. Audzējs nesatur ievērojamu daudzumu radioaktivitātes. Ar urīnu atgūtās radioaktivitātes līmenis bija daudz zemāks pelēm, kurām bija Ērliha ascīta karcinoma. Visiem dzīvniekiem ārstēja salīdzinoši augstu radioaktivitāte tika konstatēta žulti, kas kopā ar nieru emunktoriju šķiet vissvarīgākais podofilotoksīna un tā metabolītu izvadīšanas ceļš.
Perkutānas uzsūkšanās pētījumos pacientiem, kuri tika ārstēti ar 0,5% podofilotoksīnu, lietojot 0,01-0,05 ml devā 3 dienas, nebija iespējams noteikt zāļu daudzumu serumā ½-1 stundu pēc dienas.
Izmantojot 0,1 ml devas (kārpām, kuru kopējā platība> 4 cm2), tika konstatēts podofilotoksīna līmenis serumā.
Ar 0,15 ml devu seruma līmenis bija aptuveni vienāds, savukārt 5 pacientiem 12 stundas pēc lietošanas tas bija ≤ 1 ng / ml.
Pacientiem, kas ārstēti ar 0,1-1,5 ml ļoti plašu bojājumu gadījumā, maksimālais līmenis pēc 1-12 stundām bija 1-17 ng / ml. Tomēr ir pierādīts, ka klīniskajā praksē reti nepieciešams šķīduma daudzums, kas lielāks par 0,1 ml. Salīdzinoši ilgs 0,1 ml 0,5% šķīduma klīrenss pēc uzklāšanas divas reizes dienā var norādīt, ka sadalījums notiek saskaņā ar 2 nodalījumu modeli. No veiktajiem pētījumiem var ekstrapolēt seruma pusperiodu no 1 līdz 1 4½ stundas Podofilotoksīna uzkrāšanās netika novērota.
06.0 FARMACEITISKĀ INFORMĀCIJA
06.1 Palīgvielas
Pienskābe, nātrija laktāts, bezūdens etanols, ūdens.
06.2 Nesaderība
Tie nav zināmi.
06.3 Derīguma termiņš
3 gadi.
06.4 Īpaši uzglabāšanas nosacījumi
Uzglabāt temperatūrā līdz 25 ° C
06.5 Tiešā iepakojuma veids un iepakojuma saturs
Kastīte ar 3,5 ml pudeli ar drošības slēdzeni.
06.6 Norādījumi lietošanai un lietošanai
Nav būtisks.
07.0 REĢISTRĀCIJAS APLIECĪBAS ĪPAŠNIEKS
Astellas Pharma S.p.A. - Via delle Industrie 1 - 20061 Carugate (Milāna)
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS
027136011
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS
Reģistrācija 1990. gada 2. maijs - Atļaujas atjaunošana 2010. gada 1. jūnijs
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS
2011. gada septembris