Aktīvās sastāvdaļas: bupropions (bupropiona hidrohlorīds)
ELONTRIL 150 mg modificētas darbības tabletes
ELONTRIL 300 mg modificētas darbības tabletes
Indikācijas Kāpēc lieto Elontril? Kam tas paredzēts?
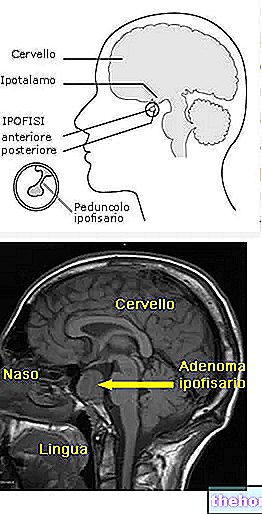
Elontril ir zāles, ko ārsts izrakstījis depresijas ārstēšanai. Tiek uzskatīts, ka tas mijiedarbojas ar ķīmiskām vielām smadzenēs, ko sauc par norepinefrīnu un dopamīnu, kas ir saistītas ar depresiju.
Kontrindikācijas Kad Elontril nedrīkst lietot
Nelietojiet Elontril
- Ja Jums ir alerģija pret bupropionu vai kādu citu (6. punktā minēto) šo zāļu sastāvdaļu
- Ja lietojat citas zāles, kas satur bupropionu
- Ja Jums ir diagnosticēta epilepsija vai agrāk bijuši krampji
- Ja Jums ir vai kādreiz ir bijuši ēšanas traucējumi (piemēram, bulīmija vai nervu anoreksija)
- Ja Jums ir smadzeņu audzējs
- Ja esat dzērājs, kurš tikko atmetis vai gatavojas pārtraukt dzeršanu
- Ja Jums ir smagi aknu darbības traucējumi
- Ja esat nesen pārtraucis lietot nomierinošus līdzekļus vai gatavojaties pārtraukt to lietošanu Elontril lietošanas laikā
- Ja pēdējo 14 dienu laikā lietojat vai esat lietojis citas zāles depresijas ārstēšanai, ko sauc par monoamīnoksidāzes inhibitoriem (MAOI)
Ja kaut kas no iepriekš minētā attiecas uz Jums, nekavējoties konsultējieties ar ārstu, nelietojot Elontril.
Piesardzība lietošanā Kas jāzina pirms Elontril lietošanas
Pirms Elontril lietošanas konsultējieties ar ārstu vai farmaceitu
Bērni un pusaudži
Elontril nav ieteicams lietot pacientiem līdz 18 gadu vecumam.
Ja pacienti, kas jaunāki par 18 gadiem, tiek ārstēti ar antidepresantiem, palielinās ar pašnāvību saistītu domu un uzvedības risks.
Pieaugušie
Pirms Elontril lietošanas ārstam jāzina:
- Ja jūs regulāri lietojat lielu daudzumu alkohola
- Ja Jums ir diabēts, kuram lietojat insulīnu vai tabletes
- Ja Jums iepriekš ir bijusi smaga galvas trauma vai galvas trauma, ir pierādīts, ka Elontril izraisa krampjus aptuveni 1 no 1000 cilvēkiem. Šī blakusparādība, visticamāk, rodas iepriekš aprakstītajām personām. Ja ārstēšanas laikā Jums ir lēkme, Jums jāpārtrauc Elontril lietošana, nekavējoties pārtrauciet to lietot un sazinieties ar savu ārstu.
- Ja Jums ir bipolāri traucējumi (ārkārtējas garastāvokļa izmaiņas), jo Elontril var izraisīt šīs slimības epizodi
- Ja Jums ir aknu vai nieru darbības traucējumi, Jums biežāk rodas blakusparādības.
Ja kaut kas no iepriekš minētā attiecas uz Jums, pirms Elontril lietošanas konsultējieties ar ārstu. Jūsu ārsts var vēlēties pievērst īpašu uzmanību jūsu terapijai vai ieteikt citu ārstēšanu.
Mijiedarbība Kādas zāles vai pārtikas produkti var mainīt Elontril iedarbību
Ja pēdējo 14 dienu laikā lietojat vai esat lietojis citus antidepresantus, ko sauc par monoamīnoksidāzes inhibitoriem (MAOI), lūdzu, pastāstiet ārstam, nelietojot Elontril (skatīt arī 2. punktu "Nelietojiet Elontril šādos gadījumos").
Pastāstiet ārstam vai farmaceitam par visām zālēm, augu izcelsmes produktiem vai vitamīniem, pat ja tos esat lietojis, pēdējā laikā esat lietojis vai varētu lietot. Ārsts var mainīt Elontril devu vai ieteikt mainīt citas zāles.
Dažas zāles nedrīkst lietot kopā ar Elontril. Daži var palielināt krampju vai krampju risku. Citas zāles var palielināt citu blakusparādību risku. Daži piemēri ir uzskaitīti zemāk, taču saraksts nav pilnīgs.
Krampju iespējamība var būt lielāka nekā parasti ...
- Ja lietojat citas zāles depresijas vai citu garīgu slimību ārstēšanai
- Ja lietojat teofilīnu astmas vai plaušu slimības ārstēšanai
- Ja lietojat tramadolu, spēcīgu pretsāpju līdzekli
- Ja esat lietojis nomierinošus līdzekļus vai ja gatavojaties tos pārtraukt Elontril lietošanas laikā (skatīt arī 2. punktu "Nelietojiet Elontril šādos gadījumos")
- Ja lietojat zāles pret malāriju (piemēram, meflokvīnu vai hlorokvīnu)
- Ja lietojat stimulantus vai citas zāles svara vai apetītes kontrolei
- Ja lietojat steroīdus (iekšķīgi vai injekciju veidā)
- Ja lietojat antibiotikas, ko sauc par hinoloniem
- Ja lietojat noteikta veida antihistamīna līdzekļus, kas var izraisīt miegainību
- Ja lietojat zāles diabēta ārstēšanai Ja kaut kas no iepriekš minētā attiecas uz Jums, pirms Elontril lietošanas nekavējoties konsultējieties ar ārstu. Ārsts novērtēs Elontril lietošanas ieguvumus un riskus.
Citu blakusparādību iespējamība var būt lielāka nekā parasti ...
- Ja Jūs lietojat citas zāles depresijas ārstēšanai (piemēram, amitriptilīnu, fluoksetīnu, paroksetīnu, dosulepīnu, desipramīnu vai imipramīnu) vai citu garīgu slimību ārstēšanai (piemēram, klozapīnu, risperidonu, tioridazīnu vai olanzapīnu)
- Ja Jūs lietojat zāles Parkinsona slimības ārstēšanai (levodopa, amantadīns vai orfenadrīns)
- Ja lietojat zāles, kas ietekmē organisma spēju izvadīt Elontril (karbamazepīns, fenitoīns, valproāts)
- Ja lietojat noteiktas zāles vēža ārstēšanai (piemēram, ciklofosfamīdu, ifosfamīdu)
- Ja lietojat tiklopidīnu vai klopidogrelu, ko lieto galvenokārt insulta profilaksei
- Ja lietojat noteiktus beta blokatorus (piemēram, metoprololu)
- Ja lietojat noteiktas zāles neregulāram sirds ritmam (propafenonu vai flekainīdu)
- Ja lietojat nikotīna plāksterus, lai palīdzētu atmest smēķēšanu.
Ja kaut kas no iepriekš minētā attiecas uz Jums, pirms Elontril lietošanas nekavējoties konsultējieties ar ārstu.
Elontril var būt mazāk efektīvs
- Ja lietojat ritonavīru vai efavirenzu, zāles HIV infekcijas ārstēšanai.
Ja tas attiecas uz jums, konsultējieties ar ārstu. Ārsts pārbaudīs, kā Elontril darbojas uz jums. Deva var būt jāpalielina vai jāmaina uz citu depresijas ārstēšanu. Nepalieliniet Elontril devu bez ārsta ieteikuma, jo tas var palielināt blakusparādību, tai skaitā krampju, risku.
Elontril var samazināt citu zāļu efektivitāti
- Ja lietojat tamoksifēnu, ko lieto krūts vēža ārstēšanai
Ja tas attiecas uz jums, pastāstiet to ārstam. Var būt nepieciešams izmantot citu depresijas ārstēšanu.
- Ja lietojat digoksīnu sirdij
Ja tas attiecas uz jums, pastāstiet to ārstam. Jūsu ārsts var apsvērt iespēju mainīt digoksīna devu.
Elontril un alkohols
Alkohols var mainīt Elontril darbību un, lietojot kopā, reti var izmainīt jūsu nervus un garīgo stāvokli. Daži cilvēki uzskata, ka, lietojot Elontril, ir jutīgāki pret alkoholu. Ārsts var ieteikt nelietot alkoholu (alu, vīnu vai stipros alkoholiskos dzērienus) Elontril lietošanas laikā vai mēģināt dzert nelielu daudzumu. Bet, ja jūs pašlaik daudz dzerat, neapstājieties pēkšņi: tas var radīt krampju risku.
Pirms Elontril lietošanas konsultējieties ar ārstu par alkohola lietošanu.
Brīdinājumi Ir svarīgi zināt, ka:
Domas, kas saistītas ar pašnāvību un depresijas pasliktināšanos
Ja esat nomākts, dažkārt var rasties domas par savainošanos vai pašnāvību. Šīs domas var būt biežākas pirmo reizi, kad sākat lietot antidepresantus, jo visu šo zāļu iedarbība prasa zināmu laiku, parasti apmēram divas nedēļas, bet dažreiz ilgāk.
Jums, visticamāk, radīsies šādas domas:
- ja Jums iepriekš ir bijušas domas par pašnāvību vai kaitējumu sev
- ja esat jauns pieaugušais. Dati, kas iegūti klīniskajos pētījumos, liecina par paaugstinātu pašnāvnieciskas uzvedības risku pieaugušajiem, kas jaunāki par 25 gadiem ar psihiskiem traucējumiem un kuri ir ārstēti ar antidepresantu.
Ja jums rodas domas par savainošanos vai pašnāvību jebkurā laikā, nekavējoties sazinieties ar savu ārstu vai dodieties uz slimnīcu. Jums var būt noderīgi pateikt radiniekam vai draugam, ka Jums ir depresija, un lūgt viņu izlasīt šo instrukciju. Jūs varat viņiem pajautāt, vai, viņuprāt, jūsu depresija pasliktinās, vai arī viņi ir noraizējušies par izmaiņām jūsu uzvedībā.
Ietekme uz urīna analīzi
Elontril var traucēt dažus urīna testus, ko izmanto citu zāļu noteikšanai. Ja Jums nepieciešama urīna analīze, lūdzu, pastāstiet ārstam vai slimnīcai, ka lietojat Elontril.
Grūtniecība un zīdīšanas periods
Nelietojiet Elontril, ja esat grūtniece, ja Jums ir aizdomas vai plānojat grūtniecību, ja vien ārsts to neiesaka. Pirms šo zāļu lietošanas konsultējieties ar ārstu vai farmaceitu. Dažos, bet ne visos pētījumos ziņots par paaugstinātu iedzimtu defektu, īpaši sirds defektu, risku zīdaiņiem, kuru mātes lietoja Elontril. Nav zināms, vai tas ir saistīts ar Elontril lietošanu.
Elontril sastāvdaļas nonāk mātes pienā. Pirms Elontril lietošanas konsultējieties ar ārstu vai farmaceitu.
Transportlīdzekļu vadīšana un mehānismu apkalpošana
Ja Elontril izraisa reiboni vai apjukumu, nevadiet transportlīdzekli un neapkalpojiet mehānismus.
Deva, lietošanas veids un laiks Kā lietot Elontril: Devas
Vienmēr lietojiet šīs zāles tieši tā, kā ārsts vai farmaceits Jums teicis. Šīs ir parastās devas, taču ārsta norādījumi ir paredzēti jums personīgi. Ja rodas šaubas, konsultējieties ar ārstu vai farmaceitu.
Var paiet zināms laiks, lai jūs justos labāk. Zāļu pilnīgai iedarbībai nepieciešams zināms laiks, dažreiz nedēļas vai mēneši. Kad sākat justies labāk, ārsts var ieteikt turpināt lietot Elontril, lai novērstu depresijas atkārtošanos.
Cik daudz vajadzētu lietot
Parastā ieteicamā deva ir viena 150 mg tablete dienā tikai pieaugušajiem.
Ārsts var palielināt devu līdz 300 mg dienā, ja depresija pēc dažām nedēļām neuzlabojas.
Lietojiet Elontril tablešu devu no rīta. Nelietojiet Elontril vairāk kā vienu reizi dienā.
Tablete ir pārklāta ar apvalku, kas lēnām atbrīvo zāles organismā. Jūs varat pamanīt kaut ko izkārnījumos, kas izskatās kā tablete. Šī ir doba odere, kas izgājusi cauri ķermenim.
- Norijiet tabletes veselas. Jūs nedrīkstat tos sakošļāt, sasmalcināt vai sadalīt - ja to darāt, pastāv pārdozēšanas risks, jo zāles organismā nonāktu pārāk ātri. Tas palielinās iespējamību, ka Jums radīsies blakusparādības, tostarp krampji.
Daži cilvēki turpina lietot vienu 150 mg tableti dienā visas ārstēšanas laikā.
Jūsu ārsts, iespējams, ir izrakstījis šo devu, ja Jums ir aknu vai nieru darbības traucējumi.
Cik ilgi tas jālieto
Tikai jūs un ārsts varat izlemt, cik ilgi lietot Elontril. Ārstēšana var ilgt nedēļas vai mēnešus, lai redzētu uzlabojumus. Regulāri konsultējieties ar savu ārstu par simptomiem, lai izlemtu, cik ilgi jums tas jālieto. Kad sākat justies labāk, ārsts var ieteikt turpināt lietot Elontril, lai novērstu depresijas atkārtošanos.
Ja esat aizmirsis lietot Elontril
Ja esat izlaidis devu, pagaidiet un lietojiet nākamo tableti parastajā laikā. Nelietojiet dubultu devu, lai aizvietotu aizmirsto tableti.
Ja pārtraucat lietot Elontril
Nepārtrauciet Elontril lietošanu un nesamaziniet devu, iepriekš nekonsultējoties ar ārstu. Ja jums ir kādi jautājumi par šo zāļu lietošanu, jautājiet savam ārstam vai farmaceitam.
Pārdozēšana Ko darīt, ja esat lietojis pārāk daudz Elontril
Ja esat lietojis pārāk daudz tablešu, tas var palielināt lēkmju vai krampju risku. Netērējiet laiku. Jautājiet savam ārstam, ko darīt, vai nekavējoties dodieties uz tuvākās slimnīcas neatliekamās palīdzības numuru.
Blakusparādības Kādas ir Elontril blakusparādības?
Tāpat kā citas zāles, šīs zāles var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas.
Krampji vai krampji
Apmēram 1 no 1000 cilvēkiem, kuri lieto Elontril, ir krampju (lēkmju) risks. Tā iespējamība ir lielāka, ja esat lietojis pārāk daudz no tā, ja lietojat noteiktas zāles vai ja Jums ir lielāks nekā parasti krampju risks. Ja jūs uztraucaties, konsultējieties ar ārstu.
Ja Jums ir lēkme, pastāstiet ārstam, tiklīdz jūtaties labāk. Nelietojiet citas tabletes.
Alerģiskas reakcijas
Dažiem cilvēkiem var būt alerģiskas reakcijas pret Elontril. Tie ietver
- Sarkana āda vai izsitumi (līdzīgi nātrenei), niezoši pūslīši vai pūslīši (nātrene) uz ādas Dažiem izsitumiem var būt nepieciešama ārstēšana slimnīcā, īpaši, ja Jums ir sāpes mutē vai acīs.
- Neparasta sēkšana un apgrūtināta elpošana
- Plakstiņu, lūpu vai mēles pietūkums
- Sāpes muskuļos vai locītavās
- Sabrukums vai samaņas zudums
Ja Jums ir kādas alerģiskas reakcijas pazīmes, nekavējoties sazinieties ar ārstu. Nelietojiet citas tabletes.
Alerģiskas reakcijas var ilgt ilgu laiku. Ja ārsts izraksta zāles, kas mazina alerģijas simptomus, noteikti pabeidziet ārstēšanu.
Citas blakusparādības
Ļoti bieži sastopamas blakusparādības: var skart vairāk nekā vienu no 10 cilvēkiem
- Grūtības aizmigt. Noteikti lietojiet Elontril no rīta
- Galvassāpes
- Sausa mute
- Slikta dūša, vemšana
Biežas blakusparādības: var skart līdz vienam no 10 cilvēkiem
- Drudzis, reibonis, nieze, svīšana un izsitumi (dažreiz alerģiskas reakcijas dēļ)
- Drebuļi, trīce, vājums, nogurums, sāpes krūtīs
- Trauksmes vai satraukuma sajūta
- Sāpes vēderā vai citas sūdzības (aizcietējums), pārtikas garšas izmaiņas, apetītes zudums (anoreksija)
- Dažreiz smags asinsspiediena paaugstināšanās, pietvīkums (pēkšņs apsārtums)
- Zvana ausī, redzes traucējumi
Retākas blakusparādības var rasties līdz vienam no 100 cilvēkiem
- Depresijas sajūta (skatīt arī 2. sadaļu "Īpaša piesardzība, lietojot Elontril, nepieciešama šādos gadījumos" sadaļā "Domas par pašnāvību un depresijas pasliktināšanos")
- Apjukuma sajūta
- Grūtības koncentrēties
- Paātrināta sirdsdarbība
- Svara zudums.
Retas blakusparādības var rasties līdz vienam no 1000 cilvēkiem
- Krampji.
Ļoti retas blakusparādības var rasties līdz vienam no 10 000 cilvēkiem
- Sirdsklauves, ģībonis
- Muskuļu raustīšanās, muskuļu stīvums, nekontrolētas kustības, problēmas ar staigāšanu vai koordināciju
- Satraukta, aizkaitināta, naidīga, agresīva, dīvaini sapņi, tirpšana vai nejutīgums, atmiņas zudums
- Dzeltena ādas vai acu baltuma krāsas maiņa (dzelte), ko var izraisīt paaugstināts aknu enzīmu līmenis, hepatīts
- Smagas alerģiskas reakcijas; izsitumi, kas saistīti ar sāpēm locītavās un muskuļos
- Cukura līmeņa izmaiņas asinīs
- Urinēšana vairāk vai mazāk nekā parasti
- Smagi izsitumi uz ādas, kas var ietekmēt muti vai citas ķermeņa daļas un var būt dzīvībai bīstami
- Psoriāzes pasliktināšanās (sarkani ādas plankumi)
- Nerealitātes vai atsvešinātības sajūta (depersonalizācija); redzēt vai dzirdēt lietas, kas tur nav (halucinācijas); sajūta vai ticība lietām, kuras tur nav (maldi); smagas aizdomas (paranoja).
Citas blakusparādības
Citas blakusparādības ir radušās nelielam skaitam cilvēku, bet to precīzs biežums nav zināms:
- domas par paškaitējumu vai pašnāvību Elontril lietošanas laikā vai tūlīt pēc ārstēšanas pārtraukšanas (skatīt 2. punktu "Kas jāzina pirms Elontril lietošanas"). Ja Jums rodas šīs domas, nekavējoties sazinieties ar savu ārstu vai dodieties uz slimnīcu.
- kontakta ar realitāti zudums un nespēja skaidri domāt vai spriest (psihoze); citi simptomi var būt halucinācijas un / vai delīrijs.
- Sarkano asins šūnu skaita samazināšanās (anēmija), balto asins šūnu skaita samazināšanās (leikopēnija) un trombocītu skaita samazināšanās (trombocitopēnija).
Ziņošana par blakusparādībām
Ja Jums rodas jebkādas blakusparādības, konsultējieties ar ārstu vai farmaceitu. Tas attiecas arī uz iespējamām blakusparādībām, kas nav minētas šajā instrukcijā. Jūs varat ziņot par blakusparādībām arī tieši, izmantojot valsts ziņošanas sistēmu vietnē www.agenziafarmaco.gov.it/it/responsabili. Ziņojot par blakusparādībām, jūs varat palīdzēt nodrošināt vairāk informācijas par šo zāļu drošumu.
Derīguma termiņš un saglabāšana
Uzglabāt šīs zāles bērniem neredzamā un nepieejamā vietā.
Nelietot šīs zāles pēc derīguma termiņa beigām, kas norādīts uz kastītes. Derīguma termiņš attiecas uz norādītā mēneša pēdējo dienu.
Uzglabāt oriģinālajā iepakojumā, lai pasargātu no mitruma un gaismas. Pudelē ir neliels noslēgts trauks ar kokogli un silikagelu, lai tabletes būtu sausas. Atstājiet trauku pudelē. Nenorīt.
Neizmetiet zāles kanalizācijā vai sadzīves atkritumos. Jautājiet farmaceitam, kā izmest zāles, kuras vairs nelietojat. Tas palīdzēs aizsargāt vidi.
Termiņš "> Cita informācija
Ko Elontril satur
Aktīvā viela ir bupropiona hidrohlorīds. Katra tablete satur 150 mg vai 300 mg bupropiona hidrohlorīda.
Citas sastāvdaļas ir: tabletes kodols: polivinilspirts, gliceril dibeenāts, tabletes apvalks: etilceluloze, povidons K-90, makrogols 1450, metakrilskābes kopolimēra dispersijas etilakrilāts, silīcija dioksīds, trietilcitrāts.
Tinte: šellaka fiksators, melnais dzelzs oksīds (E172) un amonija hidroksīds.
Elontril ārējais izskats un iepakojums
Elontril 150 mg tabletes ir krēmīgi baltas vai gaiši dzeltenas, apaļas, ar melnu tinti uzdrukātu "GS5FV" un otrā pusē bez uzdrukas. Tās ir pieejamas baltās polietilēna pudelēs pa 7, 30 vai 90 (3x30) tabletēm.
Elontril 300 mg tabletes ir krēmīgi baltas vai gaiši dzeltenas, apaļas, ar melnu tinti uzdrukātu "GS5YZ" un otrā pusē bez uzdrukas. Tās ir pieejamas baltās polietilēna pudelēs pa 7, 30 vai 90 (3x30) tabletēm.
Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī. Pašlaik pieejamā informācija var nebūt atjaunināta.
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija.
01.0 ZĀĻU NOSAUKUMS -
ELONTRIL MODIFICĒTĀS TABLETES
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS -
Katra tablete satur 150 mg vai 300 mg bupropiona hidrohlorīda.
Pilnu palīgvielu sarakstu skatīt apakšpunktā 6.1.
03.0 ZĀĻU FORMA -
Modificētas darbības tabletes.
150 mg tabletes: krēmīgi baltas vai gaiši dzeltenas, apaļas tabletes ar melnu tinti vienā pusē ar uzrakstu "GS5FV" un bez uzdrukas otrā pusē.
300 mg tabletes: krēmīgi baltas līdz gaiši dzeltenas, apaļas tabletes ar melnu tinti vienā pusē ar uzrakstu "GS5YZ" un bez uzdrukas otrā pusē.
04.0 KLĪNISKĀ INFORMĀCIJA -
04.1 Terapeitiskās indikācijas -
ELONTRIL ir indicēts smagu depresijas epizožu ārstēšanai.
04.2 Devas un lietošanas veids -
Lietošana pieaugušajiem
Ieteicamā sākumdeva ir 150 mg vienu reizi dienā. Optimālā deva nav noteikta klīniskajos pētījumos. Ja pēc 4 nedēļu ilgas ārstēšanas ar 150 mg uzlabojumi nav redzami, devu var palielināt līdz 300 mg, lietojot vienu reizi dienā. Starp nākamajām devām ir nepieciešams vismaz 24 stundu intervāls.
Attiecībā uz bupropionu terapeitiskā iedarbība tika novērota 14 dienas pēc ārstēšanas uzsākšanas.Līdzīgi kā visiem citiem antidepresantiem, pilnīga ELONTRIL antidepresanta iedarbība var būt nepārprotama tikai pēc vairākām ārstēšanas nedēļām.
Pacienti ar depresiju jāārstē pietiekami vismaz 6 mēnešus, lai nodrošinātu, ka viņiem nav simptomu.
Bezmiegs ir ļoti bieži sastopama blakusparādība un bieži vien ir pārejoša. Bezmiegu var mazināt, izvairoties no devas lietošanas pirms gulētiešanas (ar nosacījumu, ka starp devām ir vismaz 24 stundas).
• Pacienti, kas iepriekš ārstēti ar WELLBUTRIN ilgstošās darbības tabletēm:
Kad pacienti pāriet no ilgstošas darbības bupropiona tablešu lietošanas divas reizes dienā
ārstējot ar ELONTRIL modificētās darbības tabletēm, kad vien iespējams, ievadiet to pašu kopējo dienas devu.
Pediatriskā populācija
ELONTRIL lietošana nav indicēta bērniem un pusaudžiem līdz 18 gadu vecumam (skatīt apakšpunktu 4.4). ELONTRIL drošība un efektivitāte pacientiem līdz 18 gadu vecumam nav noteikta.
Pensionāriem
Efektivitāte gados vecākiem cilvēkiem nav skaidri pierādīta. Klīniskajā pētījumā gados vecāki pacienti lietoja tādu pašu devu režīmu kā pieaugušajiem (skatīt “Lietošana pieaugušajiem”). Nevar izslēgt paaugstinātu jutību dažiem gados vecākiem cilvēkiem.
Pacienti ar aknu darbības traucējumiem
ELONTRIL jālieto piesardzīgi pacientiem ar aknu mazspēju (skatīt apakšpunktu 4.4). Tā kā pacientiem ar viegliem vai vidēji smagiem traucējumiem ir palielināta farmakokinētikas mainība, ieteicamā deva šādiem pacientiem ir 150 mg vienu reizi dienā.
Pacienti ar nieru darbības traucējumiem
Ieteicamā deva šiem pacientiem ir 150 mg vienu reizi dienā, jo šādiem pacientiem bupropions un tā aktīvie metabolīti var uzkrāties lielākā mērā nekā parasti (skatīt apakšpunktu 4.4).
Lietošanas veids
ELONTRIL tabletes jānorij veselas. Tabletes nedrīkst sagriezt, sasmalcināt vai košļāt, jo tas var palielināt blakusparādību, tai skaitā krampju, risku.
ELONTRIL tabletes var lietot kopā ar ēdienu vai bez tā.
Terapijas pārtraukšana
Lai gan ELONTRIL klīniskajos pētījumos netika novērotas abstinences reakcijas (mērītas kā spontāni ziņojumi, nevis vērtēšanas skalas), jāapsver saīsināšanas periods. Bupropions ir selektīvs kateholamīnu neironu atpakaļsaistes inhibitors, un nevar izslēgt iedarbību atsitiens vai abstinences reakcijas.
04.3 Kontrindikācijas -
ELONTRIL ir kontrindicēts pacientiem ar paaugstinātu jutību pret bupropionu vai kādu no 6.1. Apakšpunktā uzskaitītajām palīgvielām.
ELONTRIL ir kontrindicēts pacientiem, kuri lieto citas zāles, kas satur bupropionu, jo krampju biežums ir atkarīgs no devas un lai izvairītos no pārdozēšanas.
ELONTRIL ir kontrindicēts pacientiem ar krampju traucējumiem vai anamnēzē.
ELONTRIL ir kontrindicēts pacientiem ar centrālās nervu sistēmas audzēju.
ELONTRIL ir kontrindicēts pacientiem, kuri to pārtrauc jebkurā ārstēšanas laikā
pēkšņi dzerot alkoholu vai jebkādas zāles, par kurām zināms, ka tās ir saistītas ar krampju risku (īpaši benzodiazepīni un benzodiazepīniem līdzīgi līdzekļi).
ELONTRIL ir kontrindicēts pacientiem ar smagu aknu cirozi.
ELONTRIL ir kontrindicēts pacientiem ar pašreizēju vai iepriekš diagnosticētu bulīmiju vai nervu anoreksiju.
Vienlaicīga ELONTRIL un monoamīnoksidāzes inhibitoru (MAO inhibitoru) lietošana ir kontrindicēta. Starp neatgriezenisku MAO inhibitoru lietošanas pārtraukšanu un ārstēšanas uzsākšanu ar ELONTRIL jāpaiet vismaz 14 dienām. Atgriezeniskiem MAO inhibitoriem pietiek ar 24 stundu periodu.
04.4 Īpaši brīdinājumi un piesardzība lietošanā -
Krampji
Nedrīkst pārsniegt ieteicamās modificētās darbības bupropiona tablešu devu, jo bupropions ir saistīts ar devu saistītu krampju risku. Kopējais krampju biežums, lietojot modificētas darbības bupropiona tabletes klīniskajos pētījumos ar devām līdz 450 mg dienā, bija aptuveni 0,1%.
Lietojot ELONTRIL, ir paaugstināts krampju risks predisponējošu riska faktoru klātbūtnē, kas pazemina krampju slieksni. Tādēļ ELONTRIL jālieto piesardzīgi pacientiem ar vienu vai vairākiem apstākļiem, kas var izraisīt krampju sliekšņa pazemināšanos. .
Visi pacienti jānovērtē attiecībā uz predisponējošiem riska faktoriem, tostarp
§ Vienlaicīga citu zāļu lietošana, kas pazemina krampju slieksni (piemēram, antipsihotiskie līdzekļi, antidepresanti, pretmalārijas līdzekļi, tramadols, teofilīns, sistēmiskie steroīdi, hinoloni un nomierinoši antihistamīni)
§ Alkohola lietošana (sk. Arī 4.3. Sadaļu)
§ galvas traumas vēsture
§ Cukura diabēts, kas ārstēts ar hipoglikēmiskiem līdzekļiem vai insulīnu
§ Stimulējošu vai anorektisku produktu lietošana
ELONTRIL lietošana jāpārtrauc un nav ieteicama pacientiem, kuriem ārstēšanas laikā rodas krampji.
Mijiedarbība (skatīt 4.5. Apakšpunktu)
Farmakokinētiskās mijiedarbības dēļ var mainīties bupropiona vai tā metabolītu līmenis plazmā, tādējādi palielinot nevēlamo blakusparādību (piemēram, kserostomija, bezmiegs, krampji) rašanās risku. Tādēļ jāievēro piesardzība, ja bupropionu lieto vienlaikus ar zālēm, kas var izraisīt vai kavēt tā metabolismu.
Bupropions kavē citohroma P450 2D6 metabolismu. Jāievēro piesardzība, ja vienlaikus tiek lietotas zāles, kuras metabolizē šis enzīms.
Literatūrā ir pierādīts, ka zāles, kas inhibē CYP2D6, var samazināt endoksifēna, kas ir tamoksifēna aktīvais metabolīts, koncentrāciju. Tādēļ ārstēšanas laikā ar tamoksifēnu, ja vien iespējams, jāizvairās no bupropiona, kas ir CYP2D6 inhibitors, lietošanas (skatīt 4.5. Apakšpunktu).
Neiropsihiatrija
Pašnāvība / domas par pašnāvību vai klīniskā stāvokļa pasliktināšanās
Depresija ir saistīta ar paaugstinātu domu par pašnāvību, paškaitējuma un pašnāvības risku (ar pašnāvību saistīti notikumi).
Šis risks saglabājas, līdz notiek ievērojama remisija. Tā kā pirmajās vai tūlīt pēc ārstēšanas nedēļām uzlabošanās var nenotikt, pacienti rūpīgi jāuzrauga, līdz parādās uzlabojumi. Kopējā klīniskā pieredze liecina, ka pašnāvības risks uzlabošanās sākumposmā var palielināties.
Ir zināms, ka pacientiem, kuriem anamnēzē ir bijuši ar pašnāvību saistīti notikumi vai kuriem pirms ārstēšanas uzsākšanas ir ievērojamas domas par pašnāvību, ir paaugstināts domu par pašnāvību vai pašnāvības mēģinājumu risks, un viņi ārstēšanas laikā rūpīgi jāuzrauga.
Klīnisko pētījumu metaanalīze, kas veikta ar antidepresantiem, salīdzinot ar placebo pieaugušiem pacientiem ar psihiskiem traucējumiem, parādīja paaugstinātu pašnāvnieciskas uzvedības risku vecuma grupā līdz 25 gadiem pacientiem, kuri tika ārstēti ar antidepresantiem, salīdzinot ar placebo.
Narkotiku terapijai vienmēr jābūt saistītai ar rūpīgu pacientu, īpaši augsta riska pacientu, uzraudzību, īpaši ārstēšanas sākumposmā un pēc devas maiņas. Pacientus (un aprūpētājus) jābrīdina par nepieciešamību kontrolēt jebkādu klīnisku pasliktināšanos, pašnāvniecisku uzvedību vai domas un neparastas izmaiņas uzvedībā, un, ja rodas šādi simptomi, nekavējoties jākonsultējas ar ārstu. Jāatzīst, ka dažu neiropsihisku simptomu parādīšanās var būt saistīta ar pamata slimības stāvokli vai zāļu terapiju (skatīt zemāk Neiropsihiatriskie simptomi, tostarp mānija un bipolāri traucējumi; skatīt apakšpunktu 4.8).
Pacientiem, kuriem rodas domas par pašnāvību / uzvedību, jāapsver režīma maiņa, tostarp iespējama ārstēšanas pārtraukšana, īpaši, ja šādi simptomi ir smagi, pēkšņi vai nav iekļauti simptomātikā.
Neiropsihiski simptomi, tostarp mānija un bipolāri traucējumi
Ir ziņots par neiropsihiskiem simptomiem (skatīt apakšpunktu 4.8). Jo īpaši ir novēroti psihotiski un mānijas simptomi, galvenokārt pacientiem ar psihiskām slimībām. Turklāt lielas depresijas epizodes var būt bipolāru traucējumu priekšnoteikums. Parasti tiek uzskatīts (lai gan tas nav konstatēts kontrolētos klīniskos pētījumos), ka šīs epizodes ārstēšana tikai ar antidepresantu var palielināt jauktās / mānijas epizodes iespējamību pacientiem ar bipolāru traucējumu risku. Ierobežoti klīniskie dati par bupropiona lietošanu kombinācijā ar garastāvokļa stabilizatoriem pacientiem ar bipolāriem traucējumiem anamnēzē liecina par zemu pārejas ātrumu uz māniju. Pirms ārstēšanas uzsākšanas ar antidepresantiem pacienti ir pienācīgi jāpārbauda, lai noteiktu, vai viņiem ir bipolāru traucējumu risks; šai atlasei jāietver detalizēta psihiatriskā vēsture, tostarp pašnāvību, bipolāru traucējumu un depresijas ģimenes anamnēze.
Dati par dzīvniekiem liecina par ļaunprātīgas izmantošanas iespējamību, tomēr pētījumi par ļaunprātīgas izmantošanas iespējamību cilvēkiem un plaša klīniskā pieredze rāda, ka bupropionam ir zems ļaunprātīgas izmantošanas potenciāls.
Klīniskā pieredze ar bupropionu pacientiem, kuri saņem elektrokonvulsīvo terapiju (EKT), ir ierobežota.Piesardzība jāievēro pacientiem, kuri vienlaikus ar bupropiona terapiju saņem elektrokonvulsīvo terapiju (EKT).
Paaugstināta jutība
Ja ārstēšanas laikā pacientiem rodas paaugstinātas jutības reakcijas, ELONTRIL lietošana nekavējoties jāpārtrauc. Ārstiem jābrīdina, ka simptomi var progresēt vai atkārtoties pēc ELONTRIL lietošanas pārtraukšanas, un jānodrošina, lai simptomātiska ārstēšana tiktu veikta adekvātu laika periodu (vismaz vienu nedēļu). Simptomi parasti ir izsitumi uz ādas, nieze, nātrene vai sāpes krūtīs, bet smagākas reakcijas var būt angioneirotiskā tūska, aizdusa / bronhu spazmas, anafilaktiskais šoks, multiformā eritēma vai Stīvensa-Džonsona sindroms.Ir ziņots arī par artralģiju, mialģiju un drudzi saistībā ar izsitumiem vai citiem simptomiem, kas liecina par aizkavētu paaugstinātu jutību (skatīt apakšpunktu 4.8). Vairumam pacientu simptomi uzlabojās pēc bupropiona lietošanas pārtraukšanas un antihistamīna un kortikosteroīdu lietošanas uzsākšanas un laika gaitā izzuda.
Sirds un asinsvadu slimības
Klīniskā pieredze par bupropiona lietošanu depresijas ārstēšanai pacientiem ar sirds un asinsvadu slimībām ir ierobežota. Jāievēro piesardzība, ja šādiem pacientiem lieto bupropionu. Tomēr pētījumos par smēķēšanas atmešanu pacientiem ar išēmisku sirds un asinsvadu slimību bupropions parasti bija labi panesams (skatīt 5.1. Apakšpunktu).
Asinsspiediens
Ir pierādīts, ka bupropions neizraisa būtisku asinsspiediena paaugstināšanos pacientiem ar depresiju, kam nav I pakāpes hipertensijas, tomēr klīniskajā praksē pacientiem, kuri lietoja bupropionu, ziņots par hipertensiju, kas dažos gadījumos bija smaga (skatīt 4.8. un nepieciešama akūta ārstēšana. Tas novērots pacientiem ar hipertensiju un bez tās.
Sākotnējais asinsspiediens ir jāmēra ārstēšanas sākumā, veicot papildu pārbaudes, īpaši pacientiem ar hipertensiju. Ja tiek novērots klīniski nozīmīgs asinsspiediena paaugstināšanās, jāpārtrauc ārstēšana ar ELONTRIL.
Vienlaicīga bupropiona un transdermālo nikotīna ievadīšanas sistēmu lietošana var paaugstināt asinsspiedienu.
Īpašas pacientu grupas
Pediatriskā populācija - ārstēšana ar antidepresantiem ir saistīta ar paaugstinātu domu par pašnāvību un uzvedības risku bērniem un pusaudžiem ar smagiem depresijas traucējumiem un citiem psihiskiem traucējumiem.
Pacienti ar aknu darbības traucējumiem - Bupropions tiek plaši metabolizēts aknās līdz tā aktīvajiem metabolītiem; šie metabolīti tiek tālāk metabolizēti. Pacientiem ar vieglu vai vidēji smagu aknu cirozi, salīdzinot ar veseliem brīvprātīgajiem, netika novērotas statistiski nozīmīgas bupropiona farmakokinētikas atšķirības, bet bupropiona līmenis plazmā uzrādīja lielāku atšķirību starp atsevišķiem pacientiem. Tādēļ ELONTRIL jālieto piesardzīgi pacientiem ar viegliem vai vidēji smagiem aknu darbības traucējumiem (skatīt apakšpunktu 4.2).
Visi pacienti ar aknu darbības traucējumiem rūpīgi jānovēro, lai konstatētu iespējamās blakusparādības (piemēram, bezmiegs, kserostomija, krampji), kas varētu liecināt par paaugstinātu zāļu vai metabolītu līmeni.
Pacienti ar nieru darbības traucējumiem - Bupropions galvenokārt izdalās ar urīnu metabolītu veidā. Tādēļ pacientiem ar nieru darbības traucējumiem bupropions un tā aktīvie metabolīti var uzkrāties plašāk nekā parasti. Pacienti rūpīgi jānovēro, vai nav iespējamu nevēlamu blakusparādību (piemēram, bezmiegs, kserostomija, krampji), kas varētu liecināt par paaugstinātu zāļu vai metabolītu līmeni (skatīt 4.2. ).
Gados vecāki cilvēki. Efektivitāte nav viennozīmīgi pierādīta gados vecākiem cilvēkiem. Klīniskajā pētījumā gados vecāki cilvēki lietoja tādu pašu devu režīmu kā pieaugušie (skatīt 4.2. Apakšpunktu Lietošana pieaugušajiem un 5.2.). .
Iejaukšanās urīna analīzē
Bupropions, jo tam ir amfetamīnam līdzīga ķīmiskā struktūra, traucē testus, ko izmanto dažos ātros testos par narkotiku klātbūtni urīnā, kā rezultātā rodas kļūdaini pozitīvi rezultāti, īpaši attiecībā uz amfetamīniem. Pozitīvs rezultāts parasti jāapstiprina ar specifiskāku metodi.
Nepareizi ievadīšanas veidi
ELONTRIL paredzēts tikai iekšķīgai lietošanai. Ir ziņots par sasmalcinātu tablešu ieelpošanu vai bupropiona injekciju, kas var izraisīt ātru izdalīšanos, ātrāku uzsūkšanos un iespējamu pārdozēšanu. Ir ziņots par krampjiem un / vai nāves gadījumiem, ievadot degunu vai parenterāli ievadot bupropionu.
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi -
Tā kā monoamīnoksidāzes A un B inhibitori arī palielina kateholamīnerģisko ceļu, izmantojot citu mehānismu nekā bupropions, vienlaicīga ELONTRIL un monoamīnoksidāzes inhibitoru (MAO inhibitoru) lietošana ir kontrindicēta (skatīt 4.3. Apakšpunktu), jo palielinās nevēlamo blakusparādību iespējamība. Reakcijas pēc neatgriezenisku MAO inhibitoru lietošanas pārtraukšanas un ārstēšanas ar ELONTRIL uzsākšanas ir jāpaiet vismaz 14 dienām. Atgriezeniskiem MAO inhibitoriem pietiek ar 24 stundu periodu.
Bupropiona ietekme uz citām zālēm
Lai gan bupropions un tā galvenais metabolīts hidroksibupropions netiek metabolizēts ar CYP2D6 izoenzīmu, tas kavē CYP2D6 ceļu. Vienlaicīga bupropiona un desipramīna lietošana veseliem brīvprātīgajiem, par kuriem zināms, ka ir spēcīgi CYP2D6 metabolizētāji, izraisīja lielu Cmax pieaugumu (2–5 reizes) un desipramīna AUC. CYP2D6 inhibīcija saglabājās vismaz 7 dienas pēc pēdējās bupropiona devas.
Vienlaicīga terapija ar zālēm ar samazinātu terapeitisko indeksu, kuras galvenokārt metabolizē CYP2D6, jāsāk ar mazākajām devām vienlaikus lietoto zāļu devu diapazonā. Pie šādām zālēm pieder daži antidepresanti (piemēram, desipramīns, imipramīns), antipsihotiskie līdzekļi ( piemēram, risperidons, tioridazīns), beta blokatori (piemēram, metoprolols), selektīvie serotonīna atpakaļsaistes inhibitori (SSAI) un 1.C tipa antiaritmiskie līdzekļi (piemēram, propafenons, flekainīds), jāapsver nepieciešamība samazināt sākotnējo zāļu devu. šādos gadījumos paredzamais ELONTRIL terapijas ieguvums ir rūpīgi jāsalīdzina ar iespējamo risku.
Narkotikām, kurām nepieciešama metaboliska aktivācija ar CYP2D6 iedarbību, lai tās būtu efektīvas (piemēram, tamoksifēns), efektivitāte var samazināties, ja tās lieto vienlaikus ar CYP2D6 inhibitoriem, piemēram, bupropionu (skatīt apakšpunktu 4.4).
Lai gan citalopramu (SSAI) galvenokārt nemetabolizē CYP2D6, vienā pētījumā bupropions palielināja citaloprama C un AUC attiecīgi par 30% un 40%.
Citu zāļu ietekme uz bupropionu
Bupropionu galvenokārt metabolizē par galveno aktīvo metabolītu - hidroksibupropionu - citohroma P450 CYP2B6 (skatīt apakšpunktu 5.2).
Vienlaicīga zāļu lietošana, kas var ietekmēt CYP2B6 izoenzīma izraisīto bupropiona metabolismu (piemēram, CYP2B6 substrāti: ciklofosfamīds, ifosfamīds un CYP2B6 inhibitori: orfenadrīns, tiklopidīns, klopidogrels), var izraisīt bupropiona līmeņa paaugstināšanos plazmā un aktīvā metabolīta līmeņa pazemināšanos. Pašlaik nav zināmas klīniskās sekas, ko izraisa CYP2B6 enzīma izraisītās bupropiona metabolisma kavēšanas un no tā izrietošās izmaiņas bupropiona-hidroksibupropiona attiecībās.
Tā kā bupropions pārsvarā tiek metabolizēts, jāievēro piesardzība, ja bupropionu lieto kopā ar zālēm, par kurām zināms, ka tās izraisa metabolismu (piemēram, karbamazepīns, fenitoīns, ritonavīrs, efavirenzs) vai inhibē vielmaiņu (piemēram, valproāts), jo tās var ietekmēt klīnisko efektivitāti un panesamību .
Pētījumu sērijā ar veseliem brīvprātīgajiem ritonavīrs (100 mg divas reizes dienā vai 600 mg divas reizes dienā) vai ritonavīrs kopā ar 400 mg lopinavīra divas reizes dienā samazināja bupropiona un tā galveno metabolītu iedarbību pēc devas. Atkarībā no 20% līdz aptuveni 80% ( skatīt 5.2. apakšpunktu). Līdzīgi, 600 mg efavirenza vienu reizi dienā divas nedēļas veseliem brīvprātīgajiem samazināja bupropiona iedarbību par aptuveni 55%. Samazinātas iedarbības klīniskās sekas nav skaidras, bet var ietvert samazinātu efektivitāti smagas depresijas ārstēšanā Pacientiem, kuri saņem vienu no šīm zālēm kombinācijā ar bupropionam var būt nepieciešamas lielākas bupropiona devas, taču nedrīkst pārsniegt maksimālo ieteicamo bupropiona devu.
Uzziniet vairāk par mijiedarbību
ELONTRIL jāievada piesardzīgi pacientiem, kuri vienlaikus saņem levodopu vai amantadīnu. Ierobežoti klīniskie dati liecina par lielāku nevēlamo blakusparādību sastopamību (piemēram, sliktu dūšu, vemšanu un neiropsihiskiem traucējumiem - skatīt apakšpunktu 4.8) pacientiem, kuri vienlaikus tiek ārstēti ar bupropionu un levodopu vai amantadīnu.
Lai gan klīniskie dati neliecina par bupropiona un alkohola farmakokinētisko mijiedarbību, ir bijuši reti ziņojumi par neiropsihiatriskām blakusparādībām vai alkohola tolerances traucējumiem pacientiem, kuri bupropiona terapijas laikā dzēra alkoholu. ELONTRIL lietošanas laikā alkohola lietošana jāsamazina līdz minimumam vai jāizvairās.
Farmakokinētikas pētījumi ar bupropiona un benzodiazepīnu vienlaicīgu lietošanu nav veikti. Ņemot vērā vielmaiņas ceļus in vitro, nav pamata attaisnot šo mijiedarbību. Pēc bupropiona un diazepāma vienlaicīgas lietošanas veseliem brīvprātīgajiem sedācija bija mazāka nekā lietojot tikai diazepāmu.
Nav sistemātiski novērtēts bupropiona saistība ar antidepresantiem (izņemot desipramīnu un citalopramu), benzodiazepīniem (izņemot diazepāmu) vai neiroleptiskiem līdzekļiem. Arī klīniskā pieredze ar asinszāli ir ierobežota.
Vienlaicīga ELONTRIL un transdermālo nikotīna ievadīšanas sistēmu lietošana var paaugstināt asinsspiedienu.
04.6 Grūtniecība un zīdīšanas periods -
Grūtniecība
Dažos epidemioloģiskos pētījumos par grūtniecības iznākumu pēc mātes pakļautības bupropionam pirmajā trimestrī ir ziņots par "saistību ar paaugstinātu noteiktu iedzimtu kardiovaskulāru anomāliju risku, jo īpaši sirds kambaru starpsienas defektiem un sirds defektiem, kas saistīti ar kreisā kambara aizplūšanas traktu. Šie konstatējumi neatbilst Pētījumi ar dzīvniekiem neliecina par tiešu vai netiešu kaitīgu ietekmi uz reproduktīvo toksicitāti (skatīt 5.3. apakšpunktu). ELONTRIL nedrīkst lietot grūtniecības laikā. Grūtnieces jāmudina pārtraukt smēķēšanu, neizmantojot zāļu terapiju.
Barošanas laiks
Bupropions un tā metabolīti izdalās mātes pienā. Lēmums par to, vai atturēties no zīdīšanas vai atturēties no ELONTRIL terapijas, jāpieņem, ņemot vērā zīdīšanas ieguvumu zīdainim un ELONTRIL terapijas ieguvumu mātei.
Auglība
Nav datu par bupropiona ietekmi uz cilvēka auglību.Reprodukcijas pētījumā ar žurkām netika konstatētas auglības pasliktināšanās pazīmes (skatīt apakšpunktu 5.3).
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus -
Tāpat kā citas zāles, kas ietekmē centrālo nervu sistēmu, bupropions var ietekmēt spēju veikt uzdevumus, kuriem nepieciešama uzmanība vai motora un kognitīvās prasmes. Tādēļ pacientiem pirms transportlīdzekļu vadīšanas vai mehānismu apkalpošanas jāievēro piesardzība, līdz viņi ir pārliecināti, ka ELONTRIL neietekmē viņu darbību.
04.8 Nevēlamās blakusparādības -
Turpmākajā sarakstā ir sniegta informācija par klīniskajā pieredzē konstatētajām nevēlamajām blakusparādībām, kas iedalītas pēc sastopamības un orgānu sistēmas klasēm.
Blakusparādības ir sakārtotas pēc biežuma, izmantojot šādu konvenciju; ļoti bieži (≥1 / 10), bieži (≥1 / 100,
* Paaugstināta jutība var izpausties kā ādas reakcijas Skatīt sadaļu "Imūnās sistēmas traucējumi" un "Ādas un zemādas audu bojājumi".
** Krampju biežums ir aptuveni 0,1% (1/1 000). Visbiežāk sastopamie krampju veidi ir ģeneralizēti toniski-kloniski krampji-krampju veids, kas dažos gadījumos var izraisīt apjukumu vai atmiņas traucējumus (skatīt sadaļu). 4.4).
*** Bupropiona terapijas laikā vai drīz pēc ārstēšanas pārtraukšanas ziņots par domām par pašnāvību un pašnāvniecisku uzvedību (skatīt apakšpunktu 4.4).
Ziņošana par iespējamām blakusparādībām
Ziņojumi par iespējamām blakusparādībām, kas rodas pēc zāļu reģistrācijas, ir
tas ir svarīgi, jo tas ļauj nepārtraukti uzraudzīt zāļu ieguvuma / riska attiecību. Veselības aprūpes speciālistus lūdz ziņot par jebkādām iespējamām blakusparādībām, izmantojot valsts ziņošanas sistēmu vietnē www.agenziafarmaco.gov.it/it/responsabili.
04.9 Pārdozēšana -
Ir ziņots par akūtu devu uzņemšanu, kas pārsniedz 10 reizes lielāku par maksimālo terapeitisko devu. Papildus notikumiem, kas aprakstīti sadaļā Nevēlamās blakusparādības, pārdozēšana izraisīja tādus simptomus kā miegainība, samaņas zudums un / vai EKG izmaiņas, piemēram, vadīšanas traucējumi (ieskaitot QRS pagarināšanos) ), aritmijas un tahikardija. Ir ziņots arī par QTc intervāla pagarināšanos, taču tas parasti ir novērots saistībā ar QRS intervāla pagarināšanos un sirdsdarbības ātruma palielināšanos. Lai gan lielākā daļa pacientu atveseļojās bez sekām, nāves gadījumi tika ziņoti reti. zāles pārdozēšanas gadījumā.
Ārstēšana: Pārdozēšanas gadījumā ieteicama hospitalizācija. Ir jāuzrauga EKG un dzīvībai svarīgās pazīmes.
Jānodrošina atbilstošs elpceļu klīrenss, skābekļa piegāde un ventilācija.Ieteicams izmantot aktivēto ogli. Nav zināms specifisks bupropiona antidots. Turpmāka ārstēšana tiks veikta, pamatojoties uz klīnisko ainu.
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS -
05.1 "Farmakodinamiskās īpašības -
Farmakoterapeitiskā grupa: citi antidepresanti - ATĶ kods N06AX12
Darbības mehānisms
Bupropions ir selektīvs kateholamīnu (noradrenalīna un dopamīna) neironu atpakaļsaistes inhibitors, ar minimālu ietekmi uz indolamīnu (serotonīna) atpakaļsaistīšanu un neaizkavē monoamīnoksidāzi.
Bupropiona kā antidepresanta darbības mehānisms nav zināms, tomēr tiek pieņemts, ka tā darbību ietekmē noradrenerģiski un / vai dopamīnerģiski mehānismi.
Klīniskā efektivitāte
Bupropiona antidepresantu aktivitāte tika pētīta klīniskajā programmā, kas tika veikta pacientiem ar smagiem depresijas traucējumiem (MDD), kurā kopumā piedalījās 1155 pacienti, kuri tika ārstēti ar ELONTRIL, un 1868 pacienti, kuri tika ārstēti ar WELLBUTRIN ilgstošās darbības tabletēm. Septiņos pētījumos tika pārbaudīta ELONTRIL efektivitāte. : 3 tika veiktas Eiropas Savienībā ar devām līdz 300 mg dienā un 4 tika veiktas ASV kā daļa no diapazons elastīgas devas līdz 450 mg dienā. Turklāt 9 pētījumi ar WELLBUTRIN ilgstošās darbības tabletēm smagu depresijas traucējumu gadījumā tika uzskatīti par atbalstošiem, pamatojoties uz ELONTRIL (vienu reizi dienā) un WELLBUTRIN ilgstošās darbības (divas reizes dienā) tablešu bioekvivalenci.
Tika pierādīts, ka ELONTRIL ir statistiski labāks par placebo, pamatojoties uz kopvērtējuma uzlabojuma novērtējumu Montgomerija-Asbergas depresijas novērtējuma skala (MADRS) vienā no diviem identiskiem pētījumiem, izmantojot devas no diapazons 150-300 mg.Reakcijas un remisijas rādītāji bija statistiski nozīmīgi augstāki, lietojot ELONTRIL, nekā lietojot placebo. Trešajā pētījumā ar gados vecākiem pacientiem statistiskais pārākums salīdzinājumā ar placebo netika sasniegts primārajā parametrā, vidējā sākotnējo vērtību samazināšanā MADRS ("analīzes" ietvaros) Pēdējais novērojums tika pārnests uz priekšu), lai gan statistiski nozīmīga ietekme tika novērota "sekundārajā analīzē (novēroto gadījumu analīze, Novērotie gadījumi).
Ievērojams ieguvums tika novērots "galapunkts primārais 2 no 4 pētījumiem, kas veikti ASV ar ELONTRIL (300-450 mg). No 2 pozitīvajiem pētījumiem viens bija placebo kontrolēts pētījums pacientiem ar smagu depresiju, bet otrs bija aktīvs salīdzināms kontrolēts pētījums pacientiem ar smagu depresiju.
Recidīvu novēršanas pētījumā pacienti, kuri reaģēja uz 8 nedēļu akūtu ārstēšanu ar atklātām WELLBUTRIN ilgstošās darbības tabletēm (300 mg dienā), tika randomizētas vai nu WELLBUTRIN ilgstošās darbības tabletēm, vai placebo vēl 44 nedēļas. WELLBUTRIN ilgstošās darbības tabletes uzrādīja statistiski nozīmīgu pārākumu salīdzinājumā ar placebo (primārais iznākums. Efekta saglabāšanas biežums ārstēšanas laikā sekot līdzi 44 nedēļu dubultmaskētajā pētījumā attiecīgi 64% un 48% lietoja WELLBUTRIN ilgstošās darbības tabletes un placebo.
Klīniskā drošība
Iedzimtu sirds defektu īpatsvars grūtniecības laikā, kas tika novērots prospektīvi, pirmsdzemdību bupropiona iedarbības pirmajā trimestrī bija 9/675 (1,3%) Starptautiskajā grūtniecības reģistrā. Retrospektīvā pētījumā nebija lielāka iedzimtu anomāliju vai sirds un asinsvadu anomāliju proporcija starp vairākām nekā tūkstotis pirmo trimestru bupropiona iedarbībai, salīdzinot ar citu antidepresantu lietošanu.
Retrospektīvā analīzē, izmantojot Nacionālā dzimstības defektu novēršanas pētījuma datus, tika novērota statistiski nozīmīga saistība starp sirds defekta rašanos jaundzimušā kreisajā aizplūšanas traktā un pašapziņotu mātes bupropiona lietošanu zīdaiņiem. : Netika novērota saistība starp mātes bupropiona lietošanu un jebkura cita veida sirds defektu vai ar visām sirds defektu kategorijām kopā.
Turpmākā Slone Epidemioloģijas centra iedzimto defektu pētījuma datu analīzē netika konstatēts statistiski nozīmīgs kreisā kambara aizplūšanas trakta sirds defektu pieaugums, lietojot bupropionu mātei. Tomēr statistiski nozīmīga saistība tika novērota kambaru starpsienas defektiem pēc bupropiona lietošanas tikai pirmajā trimestrī.
Pētījumā ar veseliem brīvprātīgajiem netika novērota klīniski nozīmīga modificētas darbības bupropiona tablešu (450 mg / dienā) ietekme uz QTcF intervālu, salīdzinot ar placebo pēc 14 dienu ilgas līdzsvara koncentrācijas.
05.2 "Farmakokinētiskās īpašības -
Uzsūkšanās
Veseliem brīvprātīgajiem, lietojot perorāli 300 mg bupropiona hidrohlorīda modificētas darbības tabletes vienu reizi dienā, maksimālā koncentrācija plazmā (Cmax) ir aptuveni 160 ng / ml pēc aptuveni 5 stundām. Pie miera stāvoklis hidroksibupropiona Cmax un AUC vērtības ir attiecīgi aptuveni 3 un 14 reizes lielākas nekā bupropionam. Trehidrobupropiona Cmax plkst miera stāvoklis ir līdzīgs bupropionam un AUC ir aptuveni 5 reizes lielāks, bet eritrohidrobupropiona koncentrācija plazmā ir salīdzināma ar bupropiona koncentrāciju. Maksimālais hidroksibupropiona līmenis plazmā tiek sasniegts pēc 7 stundām, bet treohidrobupropiona un eritrohidrobupropiona līmenis tiek sasniegts pēc 8 stundām. Bupropiona un tā aktīvo metabolītu hidroksibupropiona un treohidrobupropiona AUC un Cmax proporcionāli palielina devu diapazons 50-200 mg devu pēc vienreizējām devām un a diapazons 300-450 mg dienā pēc hroniskas lietošanas.
Bupropiona absolūtā biopieejamība nav zināma; tomēr dati par urīna izdalīšanos rāda, ka tiek absorbēti vismaz 87% bupropiona devas.
Lietojot kopā ar pārtiku, būtiski neietekmē bupropiona modificētās darbības tablešu uzsūkšanos.
Izplatīšana
Bupropions ir plaši izplatīts ar šķietamo izkliedes tilpumu aptuveni 2000 litri.
Bupropions, hidroksibupropions un treohidrobupropions mēreni saistās ar plazmas olbaltumvielām (attiecīgi 84%, 77%un 42%).
Bupropions un tā aktīvie metabolīti izdalās mātes pienā. Pētījumi ar dzīvniekiem liecina, ka bupropions un tā aktīvie metabolīti šķērso hematoencefālisko barjeru un placentu.
Pozitronu emisijas tomogrāfijas (PET) pētījumi, kas veikti veseliem brīvprātīgajiem, liecina, ka bupropions iekļūst centrālajā nervu sistēmā un saistās ar striatālo transportētāju dopamīna atpakaļsaistes uzņemšanai (aptuveni 25%, lietojot 150 mg divas reizes dienā).
Biotransformācija
Bupropions tiek plaši metabolizēts cilvēkiem. Plazmā ir identificēti trīs farmakoloģiski aktīvi metabolīti: hidroksibupropions un aminospirta izomēri, treohidrobupropions un eritrohidrobupropions. Tiem var būt klīniska nozīme, jo to koncentrācija plazmā ir tikpat augsta kā bupropiona. Aktīvie metabolīti tiek tālāk metabolizēti par neaktīviem metabolītiem (daži no tiem nav pilnībā raksturoti, bet var ietvert konjugātus) un izdalās ar urīnu.
Izglītība in vitro norāda, ka bupropions tiek metabolizēts par galveno aktīvo metabolītu hidroksibupropionu, galvenokārt CYP2B6, bet CYP1A2, 2A6, 2C9, 3A4 un 2E1 ir mazāk iesaistīti. Un otrādi, treohidrobupropiona veidošanās ietver karbonilredukciju, bet ne citohroma P450 izoenzīmus (skatīt 4.5. Apakšpunktu).
Trehidrobupropiona un eritrohidrobupropiona inhibīcijas potenciāls pret citohromu P450 nav pētīts.
Abi bupropions un hidroksibupropions ir CYP2D6 izoenzīma inhibitori ar Ki vērtībām attiecīgi 21 un 13,3 mikroM (skatīt apakšpunktu 4.5).
Ir pierādīts, ka dzīvniekiem pēc subhroniskas ievadīšanas bupropions inducē tā metabolismu.Cilvēkiem nav pierādījumu par bupropiona vai hidroksibupropiona enzīmu indukciju brīvprātīgajiem vai pacientiem, kuri 10-45 dienas saņem ieteicamās bupropiona hidrohlorīda devas.
Eliminācija
Pēc 200 mg 14C-bupropiona iekšķīgas lietošanas cilvēkiem 87% un 10% radioaktīvās devas tika konstatēti attiecīgi urīnā un izkārnījumos. Bupropiona devas daļa, kas izdalījās nemainīta, bija tikai 0,5%, kas atbilst plašajam bupropiona metabolismam. Mazāk nekā 10% no šīs 14C devas tika izmērīti urīnā kā aktīvie metabolīti.
Tur klīrenss šķietamais vidējais rādītājs pēc perorālas bupropiona hidrohlorīda lietošanas ir aptuveni 200 litri stundā, un vidējais bupropiona eliminācijas pusperiods ir aptuveni 20 stundas.
Hidroksibupropiona eliminācijas pusperiods ir aptuveni 20 stundas. Trehidrobupropiona un eritrohidrobupropiona eliminācijas pusperiods ir garāks (attiecīgi 37 un 33 stundas), un AUC vērtības miera stāvoklis tie ir attiecīgi 8 un 1,6 reizes augstāki nekā bupropionam. The miera stāvoklis bupropionam un tā metabolītiem tas tiek sasniegts 8 dienu laikā.
Modificētās darbības tabletes nešķīstošais apvalks var palikt neskarts kuņģa -zarnu trakta tranzīta laikā un izdalīties ar izkārnījumiem.
Īpašas pacientu grupas:
Pacienti ar nieru darbības traucējumiem
Pacientiem ar nieru darbības traucējumiem var samazināties bupropiona un tā galveno aktīvo metabolītu eliminācija. Ierobežoti dati par pacientiem ar nieru mazspēju beigu stadijā vai vidēji smagiem vai smagiem nieru darbības traucējumiem liecina, ka bupropiona un / vai tā metabolītu iedarbība ir palielināta (skatīt apakšpunktu 4.4). .
Pacienti ar aknu darbības traucējumiem
Bupropiona un tā aktīvo metabolītu farmakokinētika statistiski nozīmīgi neatšķīrās pacientiem ar vieglu vai vidēji smagu cirozi, salīdzinot ar veseliem brīvprātīgajiem, lai gan tika novērota lielāka atšķirība starp pacientiem (skatīt apakšpunktu 4.4). Pacientiem ar smagu aknu cirozi bupropiona Cmax un AUC bija ievērojami palielināti (vidējā atšķirība attiecīgi aptuveni 70% un 3 reizes) un mainīgāka, salīdzinot ar veseliem brīvprātīgajiem; vidējais pussabrukšanas periods bija arī garāks (par aptuveni 40%). Hidroksibupropionam vidējais Cmax bija zemāks (par aptuveni 70%), vidējais AUC bija augstāks (par aptuveni 30%), vidējais T bija aizkavēts ( aptuveni 20 stundas), un vidējais eliminācijas pusperiods bija garāks (aptuveni 4 reizes) nekā veseliem brīvprātīgajiem. Trehidrobupropionam un eritrohidrobupropionam vidējais Cmax bija zemāks (par aptuveni 30%), vidējais AUC bija augstāks (par aptuveni 50%), vidējais Tmax tika aizkavēts (aptuveni par 20 stundām) un "vidējais pussabrukšanas periods bija garāks (aptuveni 2 reizes) nekā veseliem brīvprātīgajiem (skatīt apakšpunktu 4.3).
Pensionāriem
Farmakokinētikas pētījumi gados vecākiem cilvēkiem parādīja mainīgus rezultātus. Vienas devas pētījums parādīja, ka bupropiona un tā metabolītu farmakokinētika gados vecākiem cilvēkiem neatšķīrās no jauniem pieaugušajiem. Vēl viens vienas un vairāku devu farmakokinētikas pētījums liecināja, ka gados vecākiem cilvēkiem bupropiona un tā metabolītu uzkrāšanās var notikt plašāk. Klīniskā pieredze nav atklājusi atšķirības panesamībā starp gados vecākiem un jaunākiem pacientiem, bet nevar izslēgt paaugstinātu jutību gados vecākiem pacientiem (skatīt sadaļu 4.4).
Atlaidiet in vitro bupropions kopā ar alkoholu
Pārbaude in vitro liecina, ka pie lielas alkohola koncentrācijas (līdz 40%) bupropions ātrāk izdalās no modificētās darbības zāļu formas (līdz 20% izšķīst 2 stundu laikā) (skatīt 4.5. apakšpunktu).
05.3 Preklīniskie drošības dati -
Reproduktīvās toksicitātes pētījumos ar žurkām iedarbības līmeņos, kas līdzīgi tiem, kas iegūti, lietojot maksimālo ieteicamo devu cilvēkiem (pamatojoties uz sistēmiskās iedarbības datiem), netika atklāta nelabvēlīga ietekme uz auglību, grūtniecību un augļa attīstību.
Reproduktīvās toksicitātes pētījumos ar trušiem, kuri tika ārstēti ar devām, kas līdz 7 reizēm pārsniedza maksimālo ieteicamo devu cilvēkam, pamatojoties uz mg / m² (nav pieejami dati par sistēmisko iedarbību), tika atklāts tikai neliels skeleta izmaiņu pieaugums (palielināts krūšu kurvja anatomisko izmaiņu biežums) ribas un falangu pārkaulošanās). Turklāt, lietojot mātītēm toksiskas devas, tika novērots trušu augļa svara samazinājums.
Pētījumos ar dzīvniekiem daudz lielākas bupropiona devas nekā cilvēkiem lietotās terapeitiskās devas cita starpā izraisīja šādus ar devu saistītus simptomus: ataksija un krampji žurkām, vispārējs vājums, trīce un vemšana suņiem un paaugstināts asinsspiediens. sugas. Sakarā ar enzīmu indukciju dzīvniekiem, bet ne cilvēkiem, sistēmiskā iedarbība uz dzīvniekiem bija līdzīga sistēmiskai iedarbībai, kas novērota cilvēkiem, lietojot maksimālo ieteicamo devu.
Pētījumos ar dzīvniekiem novērotas izmaiņas aknās, taču tās atspoguļo aknu enzīmu inducētāja darbību.Pie ieteicamajām devām cilvēkiem bupropions neizraisa savu metabolismu. Tas liek domāt, ka aknu konstatējumiem laboratorijas dzīvniekiem ir tikai ierobežota nozīme, novērtējot un definējot ar bupropionu saistīto risku.
Dati par genotoksicitāti norāda, ka bupropions ir vājš baktēriju mutagēns, bet ne mutagēns zīdītājiem, un tāpēc tas nav interesants kā genotoksisks līdzeklis cilvēkiem.Pētījumi ar pelēm un žurkām apstiprina, ka šīm sugām nav kancerogenitātes.
06.0 FARMACEITISKĀ INFORMĀCIJA -
06.1 Palīgvielas
Planšetdatora kodols:
Polivinilspirts
Glicerila dibeenāts
Tabletes pārklājums:
Tinte:
Melnā drukas tinte (Opacode S-1-17823).
Opacode S-1-17823, kas satur ≈45% šellaka fiksatoru (20% esterificēts), melno dzelzs oksīdu (E172) un 28% amonija hidroksīdu.
06.2 Nesaderība "-
Nav būtisks.
06.3 Derīguma termiņš "-
18 mēneši.
06.4 Īpaši uzglabāšanas nosacījumi -
Uzglabāt oriģinālajā iepakojumā, lai pasargātu no mitruma un gaismas.
06.5 Tiešā iepakojuma veids un iepakojuma saturs -
Necaurspīdīga balta augsta blīvuma polietilēna (ABPE) pudele ar metāla iesaiņojumu ar oglekļa / silikagela kombināciju un aprīkota ar bērniem necaurlaidīgu membrānu.
150 mg: 7, 30 un 90 (3x30) tabletes.
300 mg: 7, 30 un 90 (3x30) tabletes.
Visi iepakojuma lielumi tirgū var nebūt pieejami.
06.6 Lietošanas un lietošanas instrukcijas -
Nav īpašu norādījumu par iznīcināšanu.
07.0 "REĢISTRĀCIJAS APLIECĪBAS" ĪPAŠNIEKS
GlaxoSmithKline S.p.A. - Via A. Flemings, 2 - Verona
Pārdodams dīleris:
Sigma Tau Industrie Farmaceutiche Riunite S.p.A. - Viale Shakespeare, 47 - Roma
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS -
150 mg modificētas darbības tabletes - 7 A.I.C. nr .: 037697012
150 mg modificētas darbības tabletes - 30 A.I.C. nr .: 037697024
150 mg modificētas darbības tabletes - 90 A.I.C. nr .: 037697036
300 mg modificētas darbības tabletes - 7 A.I.C. nr .: 037697048
300 mg modificētas darbības tabletes - 30 A.I.C. nr .: 037697051
300 mg modificētas darbības tabletes - 90 tabletes A.I.C. nr .: 037697063
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS -
2008. gada 22. janvāris
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS -
02/2015