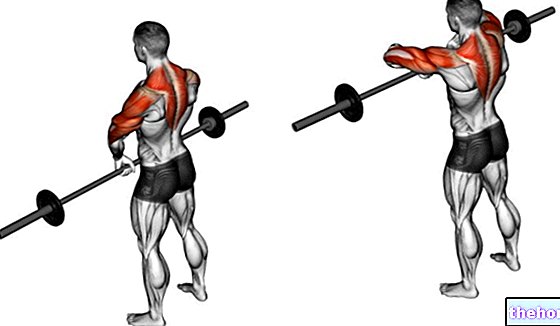
Aktīvās sastāvdaļas: Tenofovira dizoproksiils
Viread 33 mg / g granulas
Viread iepakojuma ieliktņi ir pieejami šādu izmēru iepakojumiem:- Viread 123 mg apvalkotās tabletes
- Viread 163 mg apvalkotās tabletes
- Viread 204 mg apvalkotās tabletes
- Viread 245 mg apvalkotās tabletes
- Viread 33 mg / g granulas
Indikācijas Kāpēc lieto Viread? Kam tas paredzēts?
Viread satur aktīvo vielu tenofovira dizoproksiilu. Šī aktīvā viela ir pretretrovīrusu vai pretvīrusu zāles, ko lieto HIV infekcijas ārstēšanai. Tenofovirs ir nukleotīdu reversās transkriptāzes inhibitors, vispārīgi pazīstams kā NRTI, un darbojas, traucējot normālu fermenta (reversās transkriptāzes) darbību, kas ir būtiska Viread HIV infekcijas ārstēšanai vienmēr jālieto kombinācijā ar citām zālēm.
Viread 33 mg / g granulas ir zāles HIV (cilvēka imūndeficīta vīrusa) infekcijas ārstēšanai. Tas ir paredzēts:
- pieaugušajiem
- bērni un pusaudži vecumā no 2 līdz 18 gadiem, kuri jau ir ārstēti ar citām HIV zālēm, kas vairs nav pilnībā efektīvas rezistences veidošanās dēļ vai ir izraisījušas blakusparādības
Viread 33 mg / g granulas ir arī līdzeklis hroniska B hepatīta, HBV (B hepatīta vīrusa) infekcijas ārstēšanai. Tas ir indicēts:
- pieaugušajiem
- pusaudžiem vecumā no 12 līdz mazāk nekā 18 gadiem
Jums nedrīkst būt HIV infekcija, lai ārstētos ar Viread pret HBV.
Šīs zāles neārstē HIV infekciju. Viread lietošanas laikā jūs joprojām varat iegūt infekcijas vai citas ar HIV infekciju saistītas slimības. Jūs varat arī nodot HIV vai HBV citiem, tāpēc ir svarīgi ievērot piesardzības pasākumus, lai izvairītos no citu cilvēku inficēšanās.
Kontrindikācijas Kad Viread nedrīkst lietot
Nelietojiet Viread
- Ja Jums ir alerģija pret tenofoviru, tenofovira dizoproksila fumarātu vai kādu citu (6. punktā minēto) šo zāļu sastāvdaļu.
Ja tas attiecas uz jums, nekavējoties informējiet ārstu un nelietojiet Viread.
Piesardzība lietošanā Kas jāzina pirms Viread lietošanas
Pirms Viread lietošanas konsultējieties ar ārstu vai farmaceitu.
- Uzmanieties, lai infekcija netiktu nodota citiem cilvēkiem. Jūs joprojām varat pārnēsāt HIV, kamēr lietojat šīs zāles, lai gan risku samazina antiretrovīrusu terapijas iedarbība. Apspriediet ar ārstu nepieciešamos piesardzības pasākumus, lai izvairītos no šo zāļu nodošanas. Infekcija citiem cilvēkiem. Viread nesamazina risku pārnēsāt HBV citiem seksuāla kontakta vai asins piesārņojuma dēļ. Jums jāturpina veikt piesardzības pasākumus, lai no tā izvairītos.
- Pastāstiet ārstam vai farmaceitam, ja Jums ir bijusi nieru slimība vai ja testi liecina par nieru darbības traucējumiem. Viread nedrīkst lietot pusaudžiem, kuriem jau ir nieru darbības traucējumi. Pirms ārstēšanas uzsākšanas ārsts var pasūtīt asins analīzes, lai novērtētu jūsu nieru darbību. Viread ārstēšanas laikā var ietekmēt nieres. Ārsts ārstēšanas laikā var pasūtīt asins analīzes, lai uzraudzītu nieru darbību. Nieres. Ja esat pieaugušais, ārsts Jums var ieteikt lietot tabletes retāk. Nesamaziniet noteikto devu, ja vien ārsts to nav teicis.
Viread nedrīkst lietot kopā ar citām zālēm, kas var bojāt jūsu nieres (skatīt Citas zāles un Viread). Ja tas ir neizbēgami, ārsts reizi nedēļā uzraudzīs mazuļa nieru darbību.
- Kaulu problēmas. Dažiem pieaugušiem HIV pacientiem, kuri lieto kombinētu pretretrovīrusu terapiju, var attīstīties kaulu slimība, ko sauc par osteonekrozi (kaulu audu nāve, ko izraisa asins piegādes trūkums kaulā). Kombinētās pretretrovīrusu terapijas ilgums, kortikosteroīdu lietošana, alkohola lietošana, smaga imūnsupresija, augstāks ķermeņa masas indekss, cita starpā, var būt daži no daudzajiem šīs slimības attīstības riska faktoriem. Osteonekrozes pazīmes ir locītavu stīvums, sāpes (īpaši gurnos, ceļos un plecos) un grūtības pārvietoties. Sazinieties ar savu ārstu, ja pamanāt kādu no šiem simptomiem.
Kaulu problēmas (dažkārt var rasties lūzumi) var rasties arī nieru cauruļveida šūnu bojājumu dēļ (skatīt 4. punktu, Iespējamās blakusparādības).
- Pastāstiet ārstam, ja Jums kādreiz ir bijuši aknu darbības traucējumi, tai skaitā hepatīts. Pacientiem ar aknu darbības traucējumiem, tostarp hronisku B vai C hepatītu, kuri tiek ārstēti ar pretretrovīrusu līdzekļiem, ir lielāks nopietnu un dzīvībai bīstamu aknu komplikāciju risks.Ja Jums ir B hepatīts, ārsts rūpīgi apsvērs Jums piemērotāko ārstēšanas shēmu. Ja Jums ir bijusi aknu slimība vai hronisks B hepatīts, ārsts var pasūtīt asins analīzes, lai kontrolētu aknu darbību.
- Pievērsiet uzmanību infekcijām. Ja Jums ir progresējis HIV (AIDS) un Jums ir "infekcija", Jums var attīstīties "infekcijas simptomi un iekaisums vai esošās infekcijas simptomu pasliktināšanās, uzsākot ārstēšanu ar Viread. Šie simptomi var liecināt, ka Jūsu organisma imūnsistēma ir cīņa ar infekciju. Tūlīt pēc Viread lietošanas pārbaudiet, vai nav iekaisuma vai infekcijas pazīmju. Ja pamanāt jebkādas iekaisuma vai infekcijas pazīmes, nekavējoties informējiet ārstu.
Papildus oportūnistiskām infekcijām autoimūnas traucējumi (stāvoklis, kas rodas, kad imūnsistēma uzbrūk veseliem ķermeņa audiem) var rasties arī pēc tam, kad sākat lietot zāles HIV infekcijas ārstēšanai. Autoimūnas traucējumi var rasties daudzus mēnešus pēc ārstēšanas uzsākšanas. Ja pamanāt jebkādus infekcijas simptomus vai citus simptomus, piemēram, muskuļu vājumu, sākotnēju roku un kāju vājumu, kas paceļas līdz ķermeņa stumbram, sirdsklauves, trīci vai hiperaktivitāti, lūdzu, nekavējoties informējiet par to Jūsu ārsts pieprasīs nepieciešamo ārstēšanu.
- Pastāstiet ārstam vai farmaceitam, ja esat vecāks par 65 gadiem. Viread nav pētīts pacientiem, kas vecāki par 65 gadiem. Ja esat vecāks par šo vecumu un esat izrakstījis Viread, ārsts Jūs rūpīgi uzraudzīs.
Bērni un pusaudži
Viread 33 mg / g granulas ir paredzētas tikai:
- HIV-1 inficēti bērni un pusaudži vecumā no 2 līdz 18 gadiem, kuri jau ir ārstēti ar citām HIV zālēm, kas vairs nav pilnībā efektīvas rezistences veidošanās dēļ vai ir izraisījušas nevēlamas sekas
- pusaudžiem vecumā no 12 līdz 18 gadiem, kas inficēti ar HBV
Viread 33 mg / g granulas nav piemērotas šādām kategorijām:
- nav indicēts HIV inficētiem bērniem līdz 2 gadu vecumam
- nav indicēts bērniem līdz 12 gadu vecumam, kas inficēti ar HBV (B hepatīta vīrusu)
Devas skatīt 3. sadaļā, Kā lietot Viread.
Mijiedarbība Kādas zāles vai pārtikas produkti var mainīt Viread iedarbību
Pastāstiet ārstam vai farmaceitam par visām zālēm, kuras lietojat, pēdējā laikā esat lietojis vai varētu lietot.
- Uzsākot Viread lietošanu, nepārtrauciet ārsta izrakstīto pret HIV zāļu lietošanu, ja Jums ir gan HBV, gan HIV infekcija.
- Jūs nedrīkstat lietot Viread, ja jau lietojat citas zāles, kas satur tenofovira dizoproksila fumarātu vai tenofovira alafenamīdu. Nelietojiet Viread kopā ar zālēm, kas satur adefovira dipivoksilu (zāles hroniska B hepatīta ārstēšanai).
- Īpaši svarīgi pastāstīt ārstam, ja lietojat citas zāles, kas var kaitēt jūsu nierēm. Tie ietver:
- aminoglikozīdi, pentamidīns vai vankomicīns (bakteriālas infekcijas ārstēšanai)
- amfotericīns B (sēnīšu infekcijas ārstēšanai)
- foskarnetu, gancikloviru vai cidofoviru (vīrusu infekcijas ārstēšanai)
- interleikīns-2 (vēža ārstēšanai)
- adefovira dipivoksils (HBV)
- takrolīms (imūnsistēmas nomākšanai)
- nesteroīdie pretiekaisuma līdzekļi (NPL, lieto kaulu vai muskuļu sāpju mazināšanai)
- Citas zāles, kas satur didanozīnu (HIV infekcijas ārstēšanai): Viread lietošana kopā ar citām pretvīrusu zālēm, kas satur didanozīnu, var paaugstināt didanozīna līmeni asinīs un samazināt CD4 šūnu skaitu. Lietojot kopā zāles, kas satur tenofovira dizoproksila fumarātu un didanozīnu, reti tika ziņots par aizkuņģa dziedzera iekaisumu un pienskābes acidozi (pienskābes pārpalikums asinīs), kas dažkārt izraisīja nāvi. Ārstam rūpīgi jāizvērtē, vai ārstēt jūs ar tenofoviru un didanozīnu kombinācijā.
- Ir arī svarīgi pastāstīt ārstam, ja lietojat ledipasviru / sofosbuvīru C hepatīta infekcijas ārstēšanai.
Viread kopā ar ēdienu un dzērienu
Viread granulas jāsajauc ar kādu mīkstu ēdienu, ko nedrīkst sakošļāt (piemēram, jogurtu, ābolu biezeni, bērnu pārtiku) .Ja košļājamā, maisījumam, kas satur granulas, ir izteikti rūgta garša.
Brīdinājumi Ir svarīgi zināt, ka:
Grūtniecība un zīdīšanas periods
Ja esat grūtniece vai barojat bērnu ar krūti, ja domājat, ka Jums varētu būt grūtniecība vai plānojat grūtniecību, pirms šo zāļu lietošanas konsultējieties ar ārstu vai farmaceitu.
- Jūs nedrīkstat lietot Viread grūtniecības laikā, ja vien tas nav īpaši apspriests ar ārstu. Lai gan klīnisko datu par Viread lietošanu grūtniecēm ir ierobežoti, to parasti neizmanto, ja vien tas nav absolūti nepieciešams.
- Ārstēšanas laikā ar Viread mēģiniet izvairīties no grūtniecības. Lai izvairītos no grūtniecības, jums jāizmanto efektīva kontracepcijas metode.
- Ja zināt, ka esat grūtniece vai plānojat grūtniecību, jautājiet savam ārstam par antiretrovīrusu terapijas iespējamo ieguvumu un risku jums un mazulim.
- Ja esat jau lietojis Viread grūtniecības laikā, ārsts var regulāri pieprasīt asins analīzes un citus diagnostikas testus, lai uzraudzītu bērna attīstību. Bērniem, kuru mātes grūtniecības laikā lietoja NRTI, ieguvums no HIV aizsardzības bija lielāks par blakusparādību risku.
- Ārstēšanas laikā ar Viread nedrīkst barot bērnu ar krūti. Iemesls ir tas, ka šo zāļu aktīvā sastāvdaļa izdalās mātes pienā.
- Ja esat sieviete, kas inficēta ar HIV vai HBV, ieteicams nebarot bērnu ar krūti, lai izvairītos no vīrusu pārnešanas bērnam caur pienu.
Transportlīdzekļu vadīšana un mehānismu apkalpošana
Viread var izraisīt reiboni. Ja Viread lietošanas laikā jūtat reiboni, nevadiet transportlīdzekli un nebrauciet ar velosipēdu, kā arī nelietojiet nekādus instrumentus vai mehānismus.
Viread granulas satur mannītu
Mannīts var izraisīt vieglu caureju.
Deva, lietošanas veids un laiks Kā lietot Viread: Devas
- Vienmēr lietojiet šīs zāles tieši tā, kā ārsts vai farmaceits Jums teicis. Ja rodas šaubas, konsultējieties ar ārstu vai farmaceitu.
Ieteicamā deva ir:
- Pieaugušie un pusaudži vecumā no 12 līdz 18 gadiem, kas sver vismaz 35 kg: 245 mg, kas atbilst 7,5 liekšķerēm granulu, vienu reizi dienā.
- Bērni vecumā no 2 līdz 12 gadiem: dienas deva bērniem ir atkarīga no ķermeņa svara. Jūsu ārsts noteiks pareizo Viread granulu devu, ņemot vērā jūsu bērna svaru.
Viread granulas jāievada komplektā ar mērglāzi:
Katra mērkarote satur 1 g granulu, kas satur 33 mg tenofovira dizoproksila (fumarāta veidā).
- Piepildiet mērglāzi līdz malām.
- Izmantojiet tīra naža asmeni, lai izlīdzinātu lieko granulu.
- ½ mērkarotei:
- Piepildiet mērglāzi līdz atzīmei "½" sānos.
- Bļodā ielejiet pareizo daudzumu granulu līmeņa kausiņu.
- Granulas jāsajauc ar mīkstu pārtiku, ko nedrīkst sakošļāt, piemēram, jogurtu, ābolu biezeni, bērnu pārtiku. Viena līmeņa granulu mērkarote jāsajauc ar vienu ēdamkaroti (15 ml) mīksta ēdiena. Nejauciet granulas ar šķidrām vielām.
- Granulas, kas sajauktas ar pārtiku, nekavējoties jānorij.
- Katru reizi jāņem viss sagatavotais maisījums.
- Vienmēr lietojiet ārsta ieteikto devu. Tas tiek darīts, lai pārliecinātos, ka zāles ir pilnībā efektīvas, un lai samazinātu rezistences pret ārstēšanu risku. Nemainiet devu, ja vien ārsts to nav teicis.
- Ja esat pieaugušais un Jums ir nieru darbības traucējumi, ārsts var Jums parakstīt granulu dienas devu.
- Ja Jums ir HBV, ārsts var Jums piedāvāt HIV testu, lai noskaidrotu, vai Jums ir gan HBV, gan HIV.
Norādījumus par šo zāļu lietošanu skatiet citu pretretrovīrusu līdzekļu lietošanas instrukcijās.
un aizmirstiet lietot Viread
Ir svarīgi nepalaist garām Viread devu. Ja esat aizmirsis devu, aprēķiniet, cik ilgs laiks pagājis kopš izlaišanas.
- Ja ir pagājušas mazāk nekā 12 stundas kopš parastās lietošanas, ieņemiet to pēc iespējas ātrāk un pēc tam lietojiet nākamo devu parastajā laikā.
- Ja kopš parastās devas ir pagājušas vairāk nekā 12 stundas, nelietojiet aizmirsto devu. Pagaidiet un regulāri lietojiet nākamo devu. Nelietojiet dubultu devu, lai aizvietotu aizmirsto tableti.
Ja 1 stundas laikā pēc Viread lietošanas Jums ir slikta dūša, ieņemiet vēl vienu tableti. Jūs nedrīkstat lietot vēl vienu tableti, ja pēc Viread lietošanas esat vemusi vairāk nekā vienu stundu.
Ja pārtraucat lietot Viread
Nepārtrauciet Viread lietošanu bez konsultēšanās ar ārstu. Viread lietošanas pārtraukšana var samazināt ārsta noteiktās terapijas efektivitāti.
Ja Jums ir B hepatīta infekcija vai HIV un B hepatīts kopā (vienlaicīga infekcija), ir īpaši svarīgi nepārtraukt ārstēšanu ar Viread, iepriekš nesazinoties ar savu ārstu. Dažiem pacientiem pēc ārstēšanas pārtraukšanas ir pasliktinājies hepatīts, kā norādīts simptomos vai asins analīzēs Viread. Jums var būt nepieciešams atkārtot asins analīzes vairākus mēnešus pēc ārstēšanas pārtraukšanas. Pacientiem ar progresējošu aknu slimību vai cirozi terapijas pārtraukšana nav ieteicama, jo dažiem pacientiem tas var pasliktināt hepatītu.
- Konsultējieties ar savu ārstu, pirms jebkādu iemeslu dēļ pārtraucat lietot Viread, īpaši, ja Jums ir bijusi blakusparādība vai ja Jums ir kāda cita slimība.
- Nekavējoties ziņojiet ārstam par visiem jauniem vai neparastiem simptomiem, kas novēroti pēc ārstēšanas pārtraukšanas, jo īpaši par simptomiem, kas parasti ir saistīti ar B hepatīta infekciju.
- Pirms Viread granulu atsākšanas sazinieties ar savu ārstu.
Ja jums ir kādi jautājumi par šo zāļu lietošanu, jautājiet savam ārstam vai farmaceitam.
Pārdozēšana Ko darīt, ja esat lietojis pārāk daudz Viread
Ja nejauši esat lietojis pārāk daudz Viread, jūs varētu palielināt šo zāļu iespējamo blakusparādību rašanās risku (skatīt 4. punktu, Iespējamās blakusparādības). Sazinieties ar savu ārstu vai tuvāko neatliekamās palīdzības centru. Ņemiet līdzi granulu pudeli, lai varētu viegli aprakstīt, ko esat paņēmis.
Blakusparādības Kādas ir Viread blakusparādības?
HIV terapijas laikā var palielināties svars, kā arī paaugstināties lipīdu un glikozes līmenis asinīs, kas daļēji ir saistīts ar veselības un dzīvesveida atjaunošanos, un, ja lipīdu līmenis asinīs ir dažkārt, tās pašas zāles pret HIV. Ārsts pārbaudīs, vai bērnam nav šīs izmaiņas.
Tāpat kā citas zāles, šīs zāles var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas.
Iespējamās nopietnās blakusparādības: Nekavējoties pastāstiet ārstam
- Pienskābe (pārmērīgs pienskābes līmenis asinīs) ir reta parādība (var skart līdz 1 no 1000 pacientiem), bet nopietna blakusparādība, kas var būt letāla. Tālāk minētās blakusparādības var būt pienskābes acidozes pazīmes:
- dziļa un ātra elpošana
- miegainība
- slikta dūša, vemšana un sāpes vēderā
Ja domājat, ka jūsu bērnam ir laktacidoze, nekavējoties sazinieties ar savu ārstu.
Citas iespējamās nopietnās blakusparādības
Tālāk minētās blakusparādības ir retākas (var rasties līdz 1 no 100 ārstētajiem pacientiem):
- sāpes vēderā (vēderā), ko izraisa aizkuņģa dziedzera iekaisums
- atsevišķu nieru šūnu bojājumi (cauruļveida šūnas)
Tālāk minētās blakusparādības ir retas (var rasties līdz 1 no 1000 ārstētajiem pacientiem):
- nieru iekaisums, smags urīns un slāpes
- izmaiņas urīnā un muguras sāpes, ko izraisa nieru darbības traucējumi, tai skaitā nieru mazspēja
- kaulu mīkstināšana (ar sāpēm kaulos un dažreiz lūzumiem), kas var rasties nieru cauruļveida šūnu bojājumu dēļ
- tauku aknas
Ja domājat, ka jūsu bērnam ir kāda no šīm nopietnajām blakusparādībām, lūdzu, sazinieties ar savu ārstu.
Biežākas blakusparādības
Tālāk minētās blakusparādības ir ļoti bieži sastopamas (rodas vismaz 10 no katriem 100 ārstētajiem pacientiem):
- caureja, vemšana, slikta dūša, reibonis, izsitumi, vājuma sajūta
Laboratorijas testi arī parādīja:
- fosfātu samazināšanās asinīs
Citas iespējamās blakusparādības
Bieži sastopamas šādas blakusparādības (var rasties līdz 10 no katriem 100 ārstētajiem pacientiem):
- zarnu gāze
Laboratorijas testi arī parādīja:
- aknu darbības traucējumi
Tālāk minētās blakusparādības ir retākas (var rasties līdz 1 no 100 ārstētajiem pacientiem):
- muskuļu sabrukums, muskuļu sāpes vai muskuļu vājums
Laboratorijas testi arī parādīja:
- kālija līmeņa samazināšanās asinīs
- kreatinīna līmeņa paaugstināšanās asinīs
- aizkuņģa dziedzera problēmas
Muskuļu sabrukšana, kaulu mīkstināšana (ar kaulu sāpēm un dažreiz lūzumiem), muskuļu sāpes, muskuļu vājums un samazināts kālija vai fosfāta līmenis asinīs var rasties nieru kanāliņu šūnu bojājumu dēļ.
Tālāk minētās blakusparādības ir retas (var rasties līdz 1 no 1000 ārstētajiem pacientiem):
- sāpes vēderā (vēderā), ko izraisa aknu iekaisums
- sejas, lūpu, mēles vai rīkles pietūkums
Ziņošana par blakusparādībām
Ja Jums rodas jebkādas blakusparādības, konsultējieties ar ārstu vai farmaceitu. Tas attiecas arī uz iespējamām blakusparādībām, kas nav minētas šajā instrukcijā. Jūs varat ziņot par blakusparādībām arī tieši, izmantojot V pielikumā minēto valsts ziņošanas sistēmu. Ziņojot par blakusparādībām, jūs varat palīdzēt iegūt vairāk informācijas par šo zāļu drošumu.
Derīguma termiņš un saglabāšana
Uzglabāt šīs zāles bērniem neredzamā un nepieejamā vietā.
Nelietot šīs zāles pēc derīguma termiņa beigām, kas norādīts uz pudeles un kastītes pēc {EXP}. Derīguma termiņš attiecas uz norādītā mēneša pēdējo dienu.
Uzglabāt temperatūrā līdz 25 ° C.
Neizmetiet zāles kanalizācijā vai sadzīves atkritumos. Jautājiet farmaceitam, kā izmest zāles, kuras vairs nelietojat.Tas palīdzēs aizsargāt vidi.
Cita informācija
Ko Viread satur
- Aktīvā viela ir tenofovirs. Viens grams Viread granulu satur 33 mg tenofovira dizoproksila (fumarāta veidā).
- Citas sastāvdaļas ir etilceluloze (E462), hidroksipropilceluloze (E463), mannīts (E421) un silīcija dioksīds (E551). Skatīt 2. sadaļu "Viread granulas satur mannītu".
Viread ārējais izskats un iepakojums
Šīs zāles sastāv no baltām granulām. Granulas tiek piegādātas pudelē, kurā ir 60 g granulu, un iepakojumā ir mērglāze.
Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī. Pašlaik pieejamā informācija var nebūt atjaunināta.
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija.
01.0 ZĀĻU NOSAUKUMS
VIREAD 33 MG / G granulas
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS
Katra mērkarote satur vienu gramu granulu, kas satur 33 mg tenofovira dizoproksila (fumarāta veidā).
Palīgviela ar zināmu iedarbību: viens grams granulu satur 622 mg mannīta.
Pilnu palīgvielu sarakstu skatīt apakšpunktā 6.1.
03.0 ZĀĻU FORMA
Granulēts.
Balta granulēta granula ar maskētu garšu.
04.0 KLĪNISKĀ INFORMĀCIJA
04.1 Terapeitiskās indikācijas
HIV-1 infekcija
Viread 33 mg / g granulas ir indicētas kombinācijā ar citām pretretrovīrusu zālēm, lai ārstētu bērnus vecumā no 2 līdz
Viread 33 mg / g granulas ir indicētas arī kombinācijā ar citām pretretrovīrusu zālēm HIV-1 inficētiem pieaugušajiem, kuriem cieta zāļu forma nav piemērota.
Pieaugušajiem pierādījumi par Viread ieguvumu HIV-1 infekcijas gadījumā ir balstīti uz pētījuma rezultātiem ar iepriekš neapstrādātiem pacientiem, kas ietvēra pacientus ar augstu vīrusu slodzi (> 100 000 kopijas / ml) un pētījumus, kuros Viread tika pievienots optimizētai fona terapijai (galvenokārt trīskāršai terapijai) pacientiem, kuri iepriekš tika ārstēti ar pretretrovīrusu zālēm un kuriem agrīna vīrusu atbildes reakcija bija nepietiekama (
Izvēloties lietot Viread HIV-1 inficētu pacientu ārstēšanai ar iepriekšēju pretretrovīrusu terapijas pieredzi, jābalstās uz atsevišķu vīrusu rezistences testu un / vai iepriekšējo terapiju rezultātiem.
B hepatīta infekcija
Viread 33 mg / g granulas ir indicētas hroniska B hepatīta ārstēšanai pieaugušajiem, kuriem cieta zāļu forma nav piemērota, ar:
• kompensēta aknu slimība ar pierādījumiem par aktīvu vīrusu replikāciju, pastāvīgi paaugstinātu alanīna aminotransferāzes (ALAT) līmeni serumā un histoloģiskiem pierādījumiem par aktīvu iekaisumu un / vai fibrozi (skatīt 5.1. Apakšpunktu)
• pierādījumi par lamivudīnrezistentu B hepatīta vīrusu (skatīt 4.8. Un 5.1. Apakšpunktu).
• dekompensēta aknu slimība (skatīt 4.4., 4.8. Un 5.1. Apakšpunktu).
Viread 33 mg / g granulas ir indicētas arī hroniska B hepatīta ārstēšanai pusaudžiem vecumā no 12 līdz
• kompensēta aknu slimība un pierādījumi par aktīvu imūno slimību, ti, aktīva vīrusu replikācija, pastāvīgi paaugstināts ALAT līmenis serumā un histoloģiski pierādījumi par aktīvu iekaisumu un / vai fibrozi (skatīt 4.4., 4.8. Un 5.1. Apakšpunktu).
04.2 Devas un lietošanas veids
Terapiju drīkst uzsākt ārsts, kam ir pieredze HIV infekcijas ārstēšanā un / vai hroniska B hepatīta ārstēšanā.
Devas
HIV-1Ieteicamā deva ir 6,5 mg tenofovira dizoproksila (fumarāta veidā) uz kilogramu ķermeņa masas vienu reizi dienā, lietojot kopā ar ēdienu. Skatīt 1. tabulu.
Ir pieejami ierobežoti klīniskie dati par devu 6,5 mg / kg granulu. & EGRAVE; tādēļ ir rūpīgi jāuzrauga šīs devas efektivitāte un drošība.
1. tabula: Devas bērniem vecumā no 2 līdz
Viread ir pieejams arī 123 mg, 163 mg un 204 mg apvalkotās tabletes HIV-1 inficētiem bērniem vecumā no 6 līdz
Viread ir pieejams arī 245 mg apvalkoto tablešu veidā HIV-1 infekcijas un hroniska B hepatīta ārstēšanai pusaudžiem no 12 gadu vecuma, kuru ķermeņa masa ir ≥ 35 kg.
Pieaugušie un pusaudži vecumā no 12 gadiem un ieteicamā Viread deva HIV infekcijas ārstēšanai vai hroniska B hepatīta ārstēšanai ir 245 mg, kas atbilst 7,5 kausiņiem granulu, vienu reizi dienā, iekšķīgi kopā ar ēdienu.
Viread ir pieejams arī 245 mg apvalkoto tablešu veidā HIV-1 infekcijas un hroniska B hepatīta ārstēšanai pieaugušajiem.
Hronisks B hepatīts: optimālais ārstēšanas ilgums nav zināms. Ārstēšanas pārtraukšanu var apsvērt šādos gadījumos:
• HBeAg pozitīviem pacientiem bez cirozes ārstēšana jāveic vismaz 6-12 mēnešus pēc HBe serokonversijas apstiprināšanas (HBeAg un HBV DNS zudums ar anti-HBe) vai līdz HBs serokonversijai vai efektivitātes zuduma gadījumā (sk. 4.4). Pēc ārstēšanas pārtraukšanas regulāri jāpārbauda ALAT un HBV DNS līmenis serumā, lai novērstu vēlīnus vīrusu recidīvus.
• HBeAg negatīviem pacientiem bez cirozes ārstēšana jāveic vismaz līdz HBs serokonversijai vai ir pierādījumi par efektivitātes zudumu. Ilgstoši ārstējot ilgāk par 2 gadiem, ieteicams regulāri atkārtoti izvērtēt izvēlētās terapijas piemērotību.
Izlaista deva
Ja pacients izlaiž Viread devu 12 stundu laikā pēc parastā laika, viņam pēc iespējas ātrāk jālieto Viread kopā ar ēdienu un jāturpina lietot parastā dozēšanas shēma. Ja pacients izlaiž Viread devu ilgāk par 12 stundām un ir gandrīz pienācis laiks nākamajai devai, nelietojiet aizmirsto devu un vienkārši turpiniet lietot ierasto devu grafiku.
Ja pacients vemj 1 stundas laikā pēc Viread lietošanas, viņam jālieto vēl viena deva. Ja pacients vemj vairāk nekā 1 stundu pēc Viread lietošanas, viņam nav jālieto cita deva.
Īpašas populācijas
Vecāki cilvēki
Nav pieejami dati, uz kuriem balstīt ieteikumus par devu pacientiem vecākiem par 65 gadiem (skatīt apakšpunktu 4.4).
Nieru darbības traucējumi
Tenofovīrs tiek izvadīts caur nierēm, un pacientiem ar nieru darbības traucējumiem palielinās tenofovira iedarbība.
Pieaugušie
Dati par tenofovira dizoproksila fumarāta drošību un efektivitāti pieaugušiem pacientiem ar vidēji smagiem un smagiem nieru darbības traucējumiem (kreatinīna klīrenss, kreatinīna klīrenss no 50 līdz 80 ml / min). Tādēļ tenofovira dizoproksila fumarātu pieaugušiem pacientiem ar nieru darbības traucējumiem drīkst lietot tikai tad, ja tiek uzskatīts, ka iespējamais ārstēšanas ieguvums atsver iespējamo risku. Pacientiem ar kreatinīna klīrensu ieteicams pielāgot tenofovira dizoproksila (fumarāta veidā) 33 mg / g granulu devu
Viegli nieru darbības traucējumi (kreatinīna klīrenss no 50 līdz 80 ml / min)
Daži dati no klīniskajiem pētījumiem apstiprina 245 mg tenofovira dizoproksila (fumarāta veidā) vienreizējas dienas devas ievadīšanu pacientiem ar viegliem nieru darbības traucējumiem.
Pacientiem ar vidēji smagiem (kreatinīna klīrenss no 30 līdz 49 ml / min) vai smagiem nieru darbības traucējumiem (vienreizējas devas farmakokinētiskais kreatinīna klīrenss HIV negatīviem cilvēkiem un pacientiem, kuriem nav HBV inficēti pacienti ar dažādas pakāpes nieru darbības traucējumiem, ieskaitot nieru slimību beigu stadijā, kam nepieciešama hemodialīze. Šie farmakokinētiskās modelēšanas dati nav apstiprināti klīniskajos pētījumos. Tādēļ šiem pacientiem rūpīgi jāuzrauga klīniskā reakcija uz ārstēšanu un nieru darbība (skatīt apakšpunktu). 4.4 un 5.2).
Vidēji smagi nieru darbības traucējumi (kreatinīna klīrenss no 30 līdz 49 ml / min)
Ieteicams vienu reizi dienā ievadīt 132 mg (4 mērkarotes) tenofovira dizoproksila (fumarāta veidā) 33 mg / g granulu veidā.
Smagi nieru darbības traucējumi (kreatinīna klīrenss
Pacientiem ar kreatinīna klīrensu 20-29 ml / min: vienu reizi dienā ieteicams lietot 65 mg (2 mērkarotes) tenofovira dizoproksila (fumarāta veidā) 33 mg / g granulu.
Pacientiem ar kreatinīna klīrensu 10-19 ml / min: ieteicams lietot 33 mg (1 mērkarote) tenofovira dizoproksila (fumarāta veidā) 33 mg / g granulās vienu reizi dienā.
Pacienti, kuriem tiek veikta hemodialīze: Pēc katras 4 stundu hemodialīzes sesijas var ievadīt 16,5 mg (0,5 mērkarotes) tenofovira dizoproksila (fumarāta veidā) 33 mg / g granulu.
Šie devu pielāgojumi nav apstiprināti klīniskajos pētījumos. Tādēļ rūpīgi jāuzrauga klīniskā atbildes reakcija uz ārstēšanu un nieru darbība (skatīt apakšpunktus 4.4 un 5.2).
Pacientiem, kuriem nav hemodialīzes un kuriem ir kreatinīna klīrenss, nevar sniegt ieteikumus par devu
Pediatriskie pacienti
Tenofovira dizoproksila fumarāta lietošana nav ieteicama pediatriskiem pacientiem ar nieru darbības traucējumiem (skatīt apakšpunktu 4.4).
Aknu darbības traucējumi
Pacientiem ar aknu darbības traucējumiem devas pielāgošana nav nepieciešama (skatīt 4.4. Un 5.2. Apakšpunktu).
Ja Viread terapija tiek pārtraukta pacientiem ar hronisku B hepatītu ar vai bez HIV infekcijas, šādi pacienti rūpīgi jānovēro, vai nav hepatīta paasinājumu (skatīt 4.4. Apakšpunktu).
Pediatriskā populācija
Tenofovira dizoproksila fumarāta drošība un efektivitāte, lietojot bērniem, kas jaunāki par 2 gadiem, nav pierādīta. Dati nav pieejami.
Tenofovira dizoproksila fumarāta drošība un efektivitāte bērniem ar hronisku B hepatītu vecumā no 2 līdz
Lietošanas veids
Viread granulas jā dozē ar komplektā esošo mērglāzi. Viena līmeņa liekšķere satur 1 g granulu, kas satur 33 mg tenofovira dizoproksila (fumarāta veidā). Viread granulas jāsajauc traukā ar mīkstu pārtiku, kas nav jāsakošļā, piemēram, jogurtu, ābolu biezeni, bērnu pārtiku. Viena līmeņa granulu mērkarote jāsajauc ar vienu ēdamkaroti (15 ml) mīksta ēdiena. Maisījums jānorij nekavējoties un pilnībā. Viread granulas nedrīkst sajaukt ar šķidrām vielām.
Viread jālieto vienu reizi dienā, iekšķīgi, kopā ar ēdienu.
04.3 Kontrindikācijas
Paaugstināta jutība pret aktīvo vielu vai jebkuru no 6.1. Apakšpunktā uzskaitītajām palīgvielām.
04.4 Īpaši brīdinājumi un piesardzība lietošanā
Vispār
Pirms terapijas ar tenofovira dizoproksila fumarātu uzsākšanas visiem HBV inficētiem pacientiem jāpiedāvā HIV antivielu pārbaude (skatīt zemāk esošo sadaļu) Vienlaicīga infekcija ar HIV-1 un B hepatītu).
HIV-1
Lai gan ir pierādīts, ka efektīva vīrusu nomākšana ar pretretrovīrusu terapiju ievērojami samazina seksuālās transmisijas risku, nevar izslēgt atlikušo risku. Jāveic piesardzības pasākumi, lai novērstu pārnešanu saskaņā ar valsts vadlīnijām.
Hronisks B hepatīts
Pacienti jābrīdina, ka nav pierādīts, ka tenofovira dizoproksila fumarāts novērš HBV pārnešanas risku trešām personām seksuāla kontakta vai asiņu piesārņojuma dēļ. Jums jāturpina veikt atbilstošus piesardzības pasākumus.
Vienlaicīga lietošana ar citām zālēm
• Viread nedrīkst lietot vienlaikus ar citām zālēm, kas satur tenofovira dizoproksila fumarātu.
• Viread nedrīkst lietot vienlaikus ar adefovira dipivoksilu.
• Tenofovira dizoproksila fumarāta un didanozīna vienlaicīga lietošana nav ieteicama. Tenofovira dizoproksila fumarāta un didanozīna vienlaicīga lietošana palielināja sistēmisko didanozīna iedarbību par 40–60%, kas var palielināt ar didanozīnu saistītu blakusparādību risku (skatīt 4.5. Apakšpunktu). Retos gadījumos ziņots par pankreatītu un acidozi. Tenofovira dizoproksila fumarāta un didanozīna vienlaicīga lietošana 400 mg dienas devā bija saistīta ar ievērojamu CD4 šūnu skaita samazināšanos, iespējams, "intracelulārās mijiedarbības dēļ, kas palielina fosforilētā didanozīna (aktīvā) līmeni".Daudzās kombinācijās, kas pārbaudītas HIV-1 infekcijas ārstēšanai, didanozīna devas samazināšana kopā ar tenofovira dizoproksila fumarātu līdz 250 mg ir saistīta ar "augstu viroloģisko neveiksmju biežumu".
Trīskārša terapija ar nukleozīdiem / nukleotīdiem
Lietojot tenofovira dizoproksila fumarātu HIV pacientiem kombinācijā ar lamivudīnu un abakaviru, kā arī lamivudīnu un didanozīnu, lietojot vienu reizi dienā, tika novērots "augsts viroloģisko neveiksmju līmenis un agrīna rezistences parādīšanās.
Ietekme uz nierēm un kauliem pieaugušo populācijā
Ietekme uz nierēm
Tenofovīrs galvenokārt tiek izvadīts caur nierēm. Lietojot tenofovira dizoproksila fumarātu klīniskajā praksē, ziņots par nieru mazspējas, nieru darbības traucējumu, paaugstināta kreatinīna līmeņa, hipofosfatēmijas un proksimālās tubulopātijas gadījumiem (ieskaitot Fankoni sindromu) (skatīt 4.8. Apakšpunktu).
Nieru darbības uzraudzība
Visiem pacientiem pirms tenofovira dizoproksila fumarāta terapijas uzsākšanas ieteicams izmērīt kreatinīna klīrensu, bet nieru darbība (kreatinīna klīrenss un seruma fosfāts) jākontrolē pēc divām līdz četrām ārstēšanas nedēļām, pēc trīs ārstēšanas mēnešiem un ik pēc trim līdz sešus mēnešus pēc tam pacientiem bez nieru riska faktoriem Pacientiem ar nieru darbības traucējumu risku biežāk jāpārbauda nieru darbība.
Nieru darbības vadība
Glikozes līmeņa asinīs un kālija fosfāta koncentrācijas asinīs un glikozes urīnā gadījumā (skatīt 4.8. Apakšpunktu, Proksimālā tubulopātija). Jāapsver iespēja arī pārtraukt tenofovira dizoproksila fumarāta terapiju pieaugušiem pacientiem ar samazinātu kreatinīna klīrensu.
Vienlaicīga lietošana un nieru toksicitātes risks
Jāizvairās no tenofovira dizoproksila fumarāta lietošanas, ja pacients tiek ārstēts vai nesen ir lietojis nefrotoksiskas zāles (piemēram, aminoglikozīdus, amfotericīnu B, foskarnetu, gancikloviru, pentamidīnu, vankomicīnu, cidofoviru vai interleikīnu-2). " nevar izvairīties no fumarāta un nefrotoksiskiem līdzekļiem.Nieru darbība jāpārbauda katru nedēļu.
Pēc vairāku vai lielu devu nesteroīdo pretiekaisuma līdzekļu (NPL) lietošanas uzsākšanas ir ziņots par akūtas nieru mazspējas gadījumiem pacientiem, kuri ārstēti ar tenofovira dizoproksila fumarātu un kuriem ir nieru darbības traucējumu riska faktori. NPL gadījumā ir pienācīgi jākontrolē nieru darbība.
Ir ziņots par lielāku nieru darbības traucējumu risku pacientiem, kuri saņem tenofovira dizoproksila fumarātu kombinācijā ar ritonavīru vai ar kobicistatu pastiprinātu proteāzes inhibitoru. Šiem pacientiem nepieciešama rūpīga nieru darbības kontrole (skatīt apakšpunktu 4.5). Pacientiem ar nieru riska faktoriem rūpīgi jāapsver tenofovira dizoproksila fumarāta lietošana kopā ar pastiprinātu proteāzes inhibitoru.
Tenofovira dizoproksila fumarāta klīniskais novērtējums nav veikts pacientiem, kuri ārstēti ar zālēm, kas izdalās pa to pašu nieru ceļu, ieskaitot olbaltumvielu transportēšanu, izmantojot cilvēka organisko anjonu 1. un 3. transportētāju (cilvēka organisko anjonu nesējs -hOAT) vai MRP 4 (piemēram, cidofovirs, zāles ar zināmām nefrotoksiskām īpašībām). Šie nieru proteīnu transportētāji var būt atbildīgi par kanāliņu sekrēciju un daļēji par tenofovira un cidofovira elimināciju caur nierēm. Līdz ar to šo zāļu farmakokinētika, ko izdala viens un tas pats nieru ceļš, ieskaitot olbaltumvielu transportētāju hOAT 1 un 3 vai MRP 4 var tikt mainītas, ja tās lieto kombinācijā. Ja vien tas nav absolūti nepieciešams, nav ieteicams vienlaikus lietot šīs zāles, kas izdalās pa vienu un to pašu nieru ceļu, bet, ja šāda lietošana ir neizbēgama, nieru darbība jākontrolē katru nedēļu (skatīt 4.5. apakšpunktu). .
Nieru darbības traucējumi
Nieru drošums, lietojot tenofovira dizoproksila dumarātu, ir pētīts tikai ļoti ierobežoti pieaugušiem pacientiem ar nieru darbības traucējumiem (kreatinīna klīrenss).
Pieaugušiem pacientiem ar kreatinīna klīrensu
Dati par tenofovira dizoproksila fumarāta drošību un efektivitāti pacientiem ar nieru darbības traucējumiem ir ierobežoti. Tādēļ tenofovira dizoproksila fumarātu drīkst lietot tikai tad, ja var uzskatīt, ka iespējamie ārstēšanas ieguvumi atsver iespējamos riskus. Pacientiem ar vidēji smagiem vai smagiem nieru darbības traucējumiem (kreatinīna klīrenss
Ietekme kaulu līmenī
Kontrolētā klīniskā pētījumā, kas tika veikts 144 nedēļas, ar HIV inficētiem pacientiem, kuriem tenofovira dizoproksila fumarātu salīdzināja ar stavudīnu kombinācijā ar lamivudīnu un efavirenzu, pieaugušiem pacientiem, kuri iepriekš nebija ārstēti ar pretretrovīrusu līdzekļiem, tika novērots neliels kaulu minerālvielu blīvuma samazinājums. (kaulu minerālu blīvums, KMB) gūžā un mugurkaulā abās grupās. KMB samazināšanās mugurkaulā un izmaiņas kaulu bioloģiskajos marķieros, salīdzinot ar sākotnējo rādītāju, bija ievērojami lielāka tenofovira dizoproksila fumarāta grupā 144. nedēļā. KMB gūžā bija ievērojami augstāks šajā grupā. līdz 96. nedēļai. Tomēr tas nepalielina lūzumu risku vai pierādījumus par būtiskām kaulu novirzēm pēc 144 ārstēšanas nedēļām.
Kaulu patoloģijas (retos gadījumos izraisa lūzumus) var būt saistītas ar proksimālo nieru tubulopātiju (skatīt apakšpunktu 4.8).
Ja ir aizdomas par kaulu patoloģijām vai tās tiek atklātas, jāmeklē atbilstoša konsultācija.
Ietekme uz nierēm un kauliem pediatriskā populācijā
Kaulu un nieru toksicitātes ilgtermiņa ietekme nav droši zināma. Turklāt nav iespējams pilnībā noskaidrot nieru toksicitātes atgriezeniskumu. Tāpēc ir ieteicama daudzdisciplīnu pieeja, lai katrā atsevišķā gadījumā adekvāti novērtētu ārstēšanas ieguvuma un riska attiecību, lai lemtu par atbilstošu uzraudzību ārstēšanas laikā (ieskaitot lēmumu pārtraukt ārstēšanu) un apsvērtu papildinājumu nepieciešamību.
Ietekme uz nierēm
Klīniskajā pētījumā GS-US-104-0352 ar HIV-1 inficētiem bērniem vecumā no 2 līdz
Nieru darbības uzraudzība
Pirms ārstēšanas jānosaka nieru darbība (kreatinīna klīrenss un fosfāta līmenis serumā) un jāuzrauga ārstēšanas laikā, tāpat kā pieaugušajiem (skatīt iepriekš).
Nieru darbības vadība
Ja apstiprināta fosfātu koncentrācija serumā urīnā (skatīt 4.8. Apakšpunktu, Proksimālā tubulopātija). Ja ir aizdomas vai atklāti nieru darbības traucējumi, jākonsultējas ar nefrologu, lai novērtētu iespējamo terapijas ar tenofovira dizoproksila fumarātu pārtraukšanu. Ja nav konstatēts cits cēlonis, jāapsver arī tenofovira dizoproksila fumarāta lietošanas pārtraukšana, ja pakāpeniski samazinās nieru funkcija.
Vienlaicīga lietošana un nieru toksicitātes risks
Tie paši ieteikumi attiecas uz pieaugušajiem (skatīt iepriekš).
Nieru darbības traucējumi
Tenofovira dizoproksila fumarāta lietošana nav ieteicama pediatriskiem pacientiem ar nieru darbības traucējumiem (skatīt 4.2. Apakšpunktu). Tenofovira dizoproksila fumarātu nedrīkst sākt lietot pediatriskiem pacientiem ar nieru darbības traucējumiem, un tas jāpārtrauc pediatriskiem pacientiem, kuriem terapijas laikā ar tenofovira dizoproksilu rodas nieru darbības traucējumi. fumarāts.
Ietekme kaulu līmenī
Viread var izraisīt KMB samazināšanos. Ar tenofovira dizoproksila fumarātu saistīto KMB izmaiņu ietekme uz ilgtermiņa kaulu stāvokli un turpmāko lūzumu risku vēl nav zināma (skatīt apakšpunktu 5.1).
Ja pediatriskiem pacientiem tiek konstatētas vai rodas aizdomas par kaulu novirzēm, jākonsultējas ar endokrinologu un / vai nefrologu.
Aknu slimība
Dati par drošību un efektivitāti pacientiem ar aknu transplantāciju ir ierobežoti.
Dati par tenofovira dizoproksila fumarāta drošību un efektivitāti ir ierobežoti HBV inficētiem pacientiem ar dekompensētu aknu slimību un Child-Pugh-Turcotte (CPT) rādītājs> 9. Šiem pacientiem var būt paaugstināts aknu vai nieru blakusparādību risks. Tādēļ šai pacientu grupai rūpīgi jāuzrauga aknu un žultsceļu un nieru parametri.
Hepatīta paasinājumi
Uzliesmojums ārstēšanas laikā: Hroniska B hepatīta spontāni paasinājumi ir salīdzinoši bieži, un tiem raksturīga pārejoša ALAT līmeņa paaugstināšanās serumā.Pēc pretvīrusu terapijas uzsākšanas dažiem pacientiem ALAT līmenis var palielināties (skatīt 4.8. Apakšpunktu).
Pacientiem ar kompensētu aknu slimību šiem ALAT līmeņa paaugstināšanās serumā parasti nepavada paaugstināta bilirubīna koncentrācija serumā vai aknu dekompensācija. Pacientiem ar cirozi pēc hepatīta paasinājuma var būt lielāks aknu dekompensācijas risks, tādēļ terapijas laikā viņi rūpīgi jāuzrauga.
Paasinājums pēc ārstēšanas pārtraukšanas: Ir ziņots arī par akūtu hepatīta paasinājumu pacientiem, kuri ir pārtraukuši B hepatīta terapiju. Pēc ārstēšanas paasinājumi parasti ir saistīti ar HBV DNS līmeņa paaugstināšanos, un lielākā daļa no tiem šķiet pašierobežojoši. Tomēr ir ziņots par smagiem paasinājumiem, tai skaitā letāli gadījumi Aknu darbība jākontrolē ar atkārtotiem intervāliem ar sekot līdzi gan klīniski, gan laboratoriski vismaz 6 mēnešus pēc B hepatīta terapijas pārtraukšanas. Vajadzības gadījumā terapijas atsākšana ir pamatota. Pacientiem ar progresējošu aknu slimību vai cirozi terapijas pārtraukšana nav ieteicama, jo hepatīta paasinājums pēc ārstēšanas var izraisīt aknu dekompensāciju.
Aknu uzliesmojumi ir īpaši smagi un dažreiz letāli pacientiem ar dekompensētu aknu slimību.
Vienlaicīga infekcija ar C vai D hepatītu: Nav datu par tenofovira efektivitāti pacientiem, kas vienlaikus inficēti ar C vai D hepatīta vīrusu.
HIV-1 un B hepatīta vienlaicīga infekcija: HIV / HBV vienlaikus inficētiem pacientiem, ņemot vērā HIV rezistences veidošanās risku, tenofovira dizoproksila fumarātu drīkst lietot tikai kā daļu no atbilstošas kombinētas pretretrovīrusu terapijas shēmas. terapija (kombinēta pretretrovīrusu terapija(CART) liecina par aknu darbības traucējumu biežuma palielināšanos, un tie jākontrolē saskaņā ar kopējo klīnisko praksi. Ja šādiem pacientiem pasliktinās aknu slimība, jāapsver ārstēšanas pārtraukšana vai pārtraukšana. Tomēr jāņem vērā, ka ALAT līmeņa paaugstināšanās var būt daļa no HBV klīrensa tenofovira terapijas laikā. (Skatīt iepriekš Hepatīta paasinājumi).
Lipodistrofija
CART ir saistīts ar ķermeņa tauku pārdali (lipodistrofiju) pacientiem ar HIV. Šo notikumu ilgtermiņa sekas pašlaik nav zināmas. Zināšanas par mehānismu ir nepilnīgas. Ir izvirzīta hipotēze par saistību starp viscerālo lipomatozi un proteāzes inhibitoriem un lipoatrofiju un nukleozīdu reversās transkriptāzes inhibitoriem. Palielināts lipodistrofijas risks ir saistīts ar atsevišķu faktoru klātbūtni, piemēram, vecumu, un ar narkotikām saistītiem faktoriem, piemēram, ilgāku pretretrovīrusu terapija un ar to saistītie vielmaiņas traucējumi. Klīniskajā pārbaudē jāiekļauj tauku pārdales fizisko pazīmju novērtējums. Jāapsver lipīdu līmeņa noteikšana serumā un glikozes mērīšana tukšā dūšā. Lipīdu metabolisma traucējumi jāārstē atbilstoši klīniski piemērotiem (skatīt 4.8. Apakšpunktu).
Tā kā tenofovirs ir strukturāli saistīts ar nukleozīdu analogiem, nevar izslēgt lipodistrofijas risku. Tomēr klīniskie dati par 144 ārstēšanas nedēļām ar HIV inficētiem pieaugušiem pacientiem, kuri iepriekš nebija ārstēti ar pretretrovīrusu līdzekļiem, liecina, ka, lietojot kopā ar lamivudīnu un efavirenzu, lipodistrofijas risks bija mazāks, lietojot tenofovira dizoproksila fumarātu, salīdzinot ar stavudīnu.
Mitohondriju disfunkcija
Tas ir arī pierādīts in vivo ka in vitro, ka nukleozīdi un nukleotīdu analogi izraisa dažāda līmeņa mitohondriju bojājumus. Ir bijuši ziņojumi par mitohondriju disfunkciju atklātiem HIV negatīviem zīdaiņiem, dzemdē un / vai pēc dzimšanas - uz nukleozīdu analogiem. Galvenās blakusparādības, par kurām ziņots, ir hematoloģiski traucējumi (anēmija, neitropēnija), vielmaiņas traucējumi (hiperlaktatēmija, hiperlipasēmija). Šie notikumi bieži ir pārejoši. Par dažiem neiroloģiskiem traucējumiem (hipertoniju, krampjiem, patoloģisku uzvedību) ziņots kā par vēlīnām epizodēm. Pašlaik nav zināms, vai neiroloģiski traucējumi ir pārejoši vai pastāvīgi. Jebkuram pakļautam bērnam dzemdē uz nukleozīdiem vai nukleotīdu analogiem, pat ja HIV negatīvs, a sekot līdzi klīniskā un laboratoriskā un attiecīgo pazīmju vai simptomu gadījumā pilnīga pārbaude, lai atklātu iespējamās mitohondriju disfunkcijas. Šie atklājumi nemaina pašreizējos valsts ieteikumus par pretretrovīrusu terapijas lietošanu grūtniecēm, lai novērstu HIV vertikālu pārnešanu.
Imūnās reaktivācijas sindroms
HIV inficētiem pacientiem ar smagu imūndeficītu CART uzsākšanas laikā var rasties iekaisuma reakcija uz asimptomātiskiem vai atlikušiem oportūnistiskiem patogēniem un izraisīt nopietnus klīniskos stāvokļus vai simptomu pasliktināšanos. Parasti šādas reakcijas ir novērotas dažu pirmo nedēļu vai mēnešu laikā pēc CART uzsākšanas.Svarīgi piemēri tam ir citomegalovīrusa retinīts, ģeneralizētas un / vai fokālas mikobaktēriju infekcijas un Pneumocystis jirovecii. Visi iekaisuma simptomi jānovērtē un, ja nepieciešams, jāuzsāk ārstēšana.
Ir ziņots arī par autoimūnu traucējumu (piemēram, Greivsa slimības) rašanos saistībā ar imūnreaktivāciju; tomēr reģistrētais laiks līdz slimības sākumam ir mainīgāks, un šie notikumi var rasties pat daudzus mēnešus pēc ārstēšanas uzsākšanas.
Osteonekroze
Lai gan etioloģija tiek uzskatīta par daudzfaktorālu (ieskaitot kortikosteroīdu lietošanu, alkohola lietošanu, smagu imūnsupresiju, augstāku ķermeņa masas indeksu), ir ziņots par osteonekrozes gadījumiem galvenokārt pacientiem ar progresējošu HIV slimību. Un / vai ilgstošu CART slimnieku iedarbību ieteicams konsultēties ar ārstu, ja rodas diskomforts locītavās, sāpes un stīvums vai apgrūtināta kustība.
Vecāki cilvēki
Tenofovira dizoproksila fumarāts nav pētīts pacientiem, kas vecāki par 65 gadiem. Gados vecākiem cilvēkiem nieru darbības traucējumi ir biežāk sastopami, tādēļ ārstēšana ar tenofovira dizoproksila fumarātu gados vecākiem cilvēkiem jāveic piesardzīgi.
Viread granulas satur mannītu, kam var būt viegla caureju veicinoša iedarbība.
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi
Mijiedarbības pētījumi veikti tikai pieaugušajiem.
Pamatojoties uz eksperimentos iegūtajiem rezultātiem in vitro un zināmi dati par tenofovīra eliminācijas ceļu, CYP450 mediētās mijiedarbības iespēja starp tenofovīru un citām zālēm ir zema.
Vienlaicīga terapija nav ieteicama
Viread nedrīkst lietot vienlaikus ar citām zālēm, kas satur tenofovira dizoproksila fumarātu.
Viread nedrīkst lietot vienlaikus ar adefovira dipivoksilu.
Didanozīns
Tenofovira dizoproksila fumarāta un didanozīna vienlaicīga lietošana nav ieteicama (skatīt apakšpunktu 4.4 un 2. tabulu).
Zāles, kas izdalās caur nierēm
Tā kā tenofovīrs galvenokārt tiek izvadīts caur nierēm, tenofovira dizoproksila fumarāta vienlaicīga lietošana ar zālēm, kas samazina nieru darbību vai sacenšas par aktīvo kanāliņu sekrēciju, izmantojot proteīnu transportētāju hOAT 1, hOAT 3 vai MRP 4 (piemēram, cidofoviru), var palielināt koncentrāciju serumā tenofovira un / vai citu vienlaikus lietotu zāļu lietošana.
Jāizvairās no tenofovira dizoproksila fumarāta lietošanas, vienlaikus vai nesen lietojot nefrotoksiskas zāles. Daži piemēri ir, bet ne tikai: aminoglikozīdi, amfotericīns B, foskarnets, ganciklovirs, pentamidīns, vankomicīns, cidofovirs vai interleikīns-2 (skatīt apakšpunktu 4.4).
Tā kā takrolīms var ietekmēt nieru darbību, ieteicams rūpīgi uzraudzīt, ja to lieto kopā ar tenofovira dizoproksila fumarātu.
Cita mijiedarbība
Mijiedarbība starp tenofovira dizoproksila fumarātu un proteāzes inhibitoriem un pretretrovīrusu līdzekļiem, kas nav proteāzes inhibitori, ir parādīta 2. tabulā ("pieaugums norādīts kā" ↑ ", samazinājums kā"? ", Bez izmaiņām kā", ", divas reizes dienā kā" cena " , reizi dienā kā “qd”).
2. tabula. Tenofovira dizoproksila fumarāta un citu zāļu mijiedarbība
Pētījumi, kas veikti ar citām zālēm
Klīniski nozīmīga farmakokinētiska mijiedarbība nenotika, ja tenofovira dizoproksila fumarātu lietoja vienlaikus ar emtricitabīnu, lamivudīnu, indinavīru, efavirenzu, nelfinavīru, sakvinavīru (pastiprināts ar ritonavīru), metadonu, ribavirīnu, rifestampicīnu, takrolīmu vai takrolīma hormonu.
Tenofovira dizoproksila fumarāts jālieto kopā ar pārtiku, jo pārtika palielina tenofovira biopieejamību (skatīt 5.2. Apakšpunktu).
04.6 Grūtniecība un zīdīšana
Grūtniecība
Mēreni daudz datu par grūtniecēm (no 300 līdz 1000 grūtniecēm) norāda, ka ar tenofovira dizoproksila fumarātu nav radušās malformācijas vai augļa / jaundzimušā toksicitāte. Pētījumi ar dzīvniekiem neuzrāda reproduktīvo toksicitāti (skatīt apakšpunktu 5.3). Vajadzības gadījumā var apsvērt tenofovira dizoproksila fumarāta lietošanu grūtniecības laikā.
Barošanas laiks
Ir pierādīts, ka tenofovirs izdalās mātes pienā. Nav pietiekami daudz informācijas par tenofovira ietekmi uz jaundzimušajiem / zīdaiņiem. Tāpēc Viread nedrīkst lietot zīdīšanas laikā.
Lai izvairītos no HIV un HBV pārnešanas jaundzimušajam, parasti ar HIV un HBV inficētām sievietēm nav ieteicams barot bērnu ar krūti.
Auglība
Klīniskie dati par tenofovira dizoproksila fumarāta ietekmi uz auglību ir ierobežoti Pētījumi ar dzīvniekiem neliecina par tenofovira dizoproksila fumarāta kaitīgo ietekmi uz auglību.
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus
Nav veikti pētījumi par spēju vadīt transportlīdzekļus un apkalpot mehānismus, tomēr pacienti jābrīdina, ka ārstēšanas laikā ar tenofovira dizoproksila fumarātu ir novērots reibonis.
04.8 Nevēlamās blakusparādības
Drošības profila kopsavilkums
HIV-1 un B hepatīts: Pacientiem, kuri lieto tenofovira dizoproksila fumarātu, ziņots par retiem gadījumiem, nieru darbības traucējumiem, nieru mazspēju un proksimālo nieru tubulopātiju (ieskaitot Fankoni sindromu), kas dažkārt izraisa kaulu izmaiņas (un reti lūzumus). Pacientiem, kuri lieto Viread, ieteicams kontrolēt nieru darbību (skatīt apakšpunktu 4.4).
HIV-1: Pēc ārstēšanas ar tenofovira dizoproksila fumarātu kombinācijā ar citiem pretretrovīrusu līdzekļiem aptuveni trešdaļai pacientu var rasties blakusparādības. Šīs reakcijas parasti sastāv no vieglām vai vidēji smagām kuņģa -zarnu trakta epizodēm. Aptuveni 1% pieaugušo pacientu, kuri tika ārstēti ar tenofovira dizoproksila fumarātu, pārtrauca ārstēšanu kuņģa -zarnu trakta iedarbības dēļ.
Lipodistrofija ir saistīta ar tenofovira dizoproksila fumarātu (skatīt 4.4. Un 4.8. Apakšpunktu) Izvēlēto blakusparādību apraksts).
Viread un didanozīna vienlaicīga lietošana nav ieteicama, jo tas var palielināt blakusparādību risku (skatīt 4.5. Apakšpunktu). Retos gadījumos ziņots par pankreatītu un laktātacidozi, dažkārt letālu (skatīt apakšpunktu 4.4).
B hepatīts: Aptuveni ceturtdaļai pacientu, kuri lieto tenofovira dizoproksila fumarātu, var rasties blakusparādības, no kurām lielākā daļa ir vieglas. Klīniskajos pētījumos ar HBV inficētiem pacientiem biežākā blakusparādība bija slikta dūša (5,4%).
Ir ziņots par akūtu hepatīta paasinājumu gan ārstētiem pacientiem, gan pacientiem, kuri ir pārtraukuši B hepatīta terapiju (skatīt apakšpunktu 4.4).
Nevēlamo blakusparādību kopsavilkuma tabula
Tenofovira dizoproksila fumarāta blakusparādību novērtējums ir balstīts uz drošuma datiem, kas iegūti klīniskajos pētījumos un pēcreģistrācijas pieredzē.Visas blakusparādības ir parādītas 3. tabulā.
Klīniskie pētījumi par HIV-1: Nevēlamo blakusparādību novērtējums no HIV-1 klīniskajiem pētījumiem ir balstīts uz divu pētījumu pieredzi, kuros 653 pieaugušie pacienti ar iepriekšēju ārstēšanas pieredzi tika ārstēti ar tenofovira dizoproksila fumarātu (n = 443) vai placebo (n = 210) kombinācijā ar citiem antiretrovīrusu zāles 24 nedēļas, kā arī dubultmaskēts kontrolēts salīdzinošs pētījums, kurā 600 pieaugušie pacienti, kuri iepriekš nebija ārstēti, tika ārstēti ar 245 mg tenofovira dizoproksila (fumarāta veidā) (n = 299) vai stavudīna (n = 301) kombinācijā ar lamivudīnu un efavirenzu 144 nedēļas.
B hepatīta klīniskie pētījumi: Nevēlamo blakusparādību novērtējums no klīnisko pētījumu datiem galvenokārt balstīts uz pieredzi divos dubultmaskētos, kontrolētos salīdzinošos pētījumos, kuros piedalījās 641 pieaugušs pacients ar hronisku B hepatītu un kompensētu aknu slimību, ārstējot ar 245 mg tenofovira dizoproksila (fumarāta veidā) dienā (n = 426) vai adefovira dipivoksila 10 mg dienā (n = 215) 48 nedēļas. Blakusparādības, kas novērotas ilgstošas 384 nedēļas ilgas ārstēšanas laikā, atbilst tenofovira dizoproksila fumarāta drošības profilam. Pēc sākotnējā samazinājuma par aptuveni - 4,9 ml / min ( izmantojot Kokrofta -Golla vienādojumu) vai -3,9 ml / min / 1,73 m2 (izmantojot uztura modifikācijas vienādojumu nieru slimību gadījumā [uztura izmaiņas nieru slimību gadījumā(MDRD])) pēc pirmajām 4 ārstēšanas nedēļām pacientiem, kuri tika ārstēti ar tenofovira dizoproksila fumarātu, ikgadējais nieru darbības samazināšanās ātrums pēc sākotnējā līmeņa bija -1,41 ml / min gadā (izmantojot Kokrofta vienādojumu -Gault) un -0,74 ml / min / 1,73 m2 gadā (izmantojot MDRD vienādojumu).
Pacienti ar dekompensētu aknu slimību: Tenofovira dizoproksila fumarāta drošības profils pacientiem ar dekompensētu aknu slimību tika novērtēts dubultmaskētā kontrolētā pētījumā (GS-US-174-0108), kurā pieaugušie pacienti 48 nedēļas tika ārstēti ar tenofovira dizoproksila fumarātu (n = 45) vai emtricitabīns plus tenofovira dizoproksila fumarāts (n = 45) vai entekavīrs (n = 22).
Tenofovira dizoproksila fumarāta grupā 7% pacientu pārtrauca terapiju nevēlamas parādības dēļ; 9% pacientu bija apstiprināts kreatinīna līmeņa paaugstināšanās serumā ≥ 0,5 mg / dl vai apstiprināta seruma fosfātu vērtība ≥ 0,5 mg / dL vai apstiprināta fosfāta vērtība serumā
168. nedēļā šajā dekompensētās aknu slimības pacientu grupā mirstība bija 13% (6/45) tenofovira dizoproksila fumarāta grupā, 11% (5/45) emtricitabīna plus tenofovira dizoproksila fumarāta grupā un 14% (3 /22) entekavīra grupā. Hepatocelulārās karcinomas biežums bija 18% (8/45) tenofovira dizoproksila fumarāta grupā, 7% (3/45) emtricitabīna plus tenofovira dizoproksila fumarāta grupā un 9% (2/ 22) entekavīra grupā.
Tika konstatēts, ka pacientiem ar augstu sākotnējo CPT punktu ir paaugstināts nopietnu blakusparādību attīstības risks (skatīt apakšpunktu 4.4).
Pacienti ar hronisku pret lamivudīnu rezistentu B hepatītu: Randomizētā dubultmaskētā pētījumā (GS-US-174-0121), kurā 280 pret lamivudīnu rezistenti pacienti tika ārstēti ar tenofovira dizoproksila fumarātu (n = 141) vai emtricitabīna / tenofovira dizoproksila fumarātu (n = 139) līdz 96 nedēļām netika konstatētas jaunas tenofovira dizoproksila fumarāta blakusparādības.
Blakusparādības, kurām ir aizdomas (vai vismaz iespējama) korelācija ar ārstēšanu, ir uzskaitītas zemāk, dalītas ar orgānu sistēmu klasi un biežumu. Katrā sastopamības biežuma klasē blakusparādības ir uzskaitītas to smaguma pakāpes samazināšanās secībā. Biežums ir definēts kā ļoti bieži (≥ 1/10), bieži (≥ 1/100,
3. tabula. Kopsavilkuma tabula par blakusparādībām, kas saistītas ar tenofovira dizoproksila fumarātu, pamatojoties uz klīniskajiem pētījumiem un pēcreģistrācijas pieredzi
1 Šī blakusparādība var rasties proksimālās nieru tubulopātijas rezultātā. Ja šī stāvokļa nav, to neuzskata par saistītu ar tenofovira dizoproksila fumarātu.
2 Šī blakusparādība tika konstatēta pēcreģistrācijas uzraudzībā, bet netika novērota randomizētos kontrolētos klīniskos pētījumos vai paplašinātās piekļuves programmās ar tenofovira dizoproksila fumarātu. Biežumu novērtēja ar statistisku aprēķinu, pamatojoties uz kopējo pacientu skaitu, kuri tika pakļauti tenofovira dizoproksila fumarāta iedarbībai randomizētos kontrolētos pētījumos un paplašinātās piekļuves programmās (n = 7319).
Izvēlēto blakusparādību apraksts
HIV-1 un B hepatīts:
Nieru darbības traucējumi
Tā kā Viread var izraisīt nieru bojājumus, ieteicams kontrolēt nieru darbību (skatīt 4.4. Un 4.8. Apakšpunktu) Drošības profila kopsavilkums). Proksimālā nieru tubulopātija parasti izzuda vai uzlabojās pēc tenofovira dizoproksila fumarāta lietošanas pārtraukšanas. Tomēr dažiem pacientiem samazināts kreatinīna klīrenss pilnībā neizzuda, neskatoties uz tenofovira dizoproksila fumarāta lietošanas pārtraukšanu. Pacientiem ar nieru darbības traucējumu risku (piemēram, pacientiem ar sākotnējiem nieru riska faktoriem, HIV slimību vai pacientiem, kuri vienlaikus lieto nefrotoksiskas zāles) funkcija, visticamāk, būs nepilnīga, neskatoties uz tenofovira dizoproksila fumarāta lietošanas pārtraukšanu (skatīt apakšpunktu 4.4).
HIV-1:
Mijiedarbība ar didanozīnu
Tenofovira dizoproksila fumarāta un didanozīna vienlaicīga lietošana nav ieteicama, jo tas palielina par 40–60% didanozīna sistēmisko iedarbību un var palielināt ar didanozīnu saistītu blakusparādību risku (skatīt 4.5. Apakšpunktu). Retos gadījumos ir ziņots par pankreatītu un pienskābes acidozi, kas dažreiz ir letāla.
Lipīdi, lipodistrofija un vielmaiņas izmaiņas
CART ir saistīts ar vielmaiņas traucējumiem, piemēram, hipertrigliceridēmiju, hiperholesterinēmiju, rezistenci pret insulīnu, hiperglikēmiju un hiperlaktatēmiju (skatīt apakšpunktu 4.4).
CARt ir saistīts ar ķermeņa tauku pārdali (lipodistrofiju) HIV inficētiem pacientiem, tostarp perifēro un sejas zemādas tauku zudumu, palielinātu vēdera un iekšējo orgānu tauku daudzumu, "krūšu hipertrofiju un" dorsocervikālo tauku uzkrāšanos (bifeļa kupris) (sk. 4.4).
144 nedēļas ilgā kontrolētā pētījumā, kas tika veikts pieaugušiem pacientiem, kuri iepriekš nebija ārstēti ar pretretrovīrusu līdzekļiem, salīdzinot tenofovira dizoproksila fumarātu ar stavudīnu kombinācijā ar lamivudīnu un efavirenzu, pacientiem, kuri tika ārstēti ar tenofovira dizoproksila fumarātu, lipodistrofijas biežums bija ievērojami mazāks nekā pacientiem, kuri ārstēts ar stavudīnu. Tenofovira dizoproksila fumarāta grupā arī bija ievērojami zemāks vidējais triglicerīdu un kopējā holesterīna līmeņa tukšā dūšā pieaugums salīdzinājumā ar salīdzinošo grupu.
Imūnās reaktivācijas sindroms
HIV inficētiem pacientiem ar smagu imūndeficītu CART uzsākšanas laikā var rasties iekaisuma reakcija uz asimptomātiskām vai atlikušām oportūnistiskām infekcijām. Ir ziņots arī par autoimūniem traucējumiem (piemēram, Greivsa slimību); tomēr reģistrēts laiks līdz slimības sākumam tas ir mainīgāks un šie notikumi var rasties pat daudzus mēnešus pēc ārstēšanas uzsākšanas (skatīt 4.4. apakšpunktu).
Osteonekroze
Par osteonekrozes gadījumiem ziņots galvenokārt pacientiem ar vispārzināmiem riska faktoriem, ar progresējošu HIV slimību un / vai ilgstošu CART iedarbību. Šādu gadījumu biežums nav zināms (skatīt apakšpunktu 4.4).
B hepatīts:
Ārstēšanas laikā hepatīta paasinājumi
Pētījumos ar pacientiem, kas iepriekš nebija ārstēti ar nukleozīdiem, 2,6% pacientu, kuri tika ārstēti ar tenofovira dizoproksila fumarātu, ALAT līmeņa paaugstināšanās> 10 reizes pārsniedz NAR, ULN un> 2 reizes pārsniedza sākotnējo līmeni. ALAT līmeņa paaugstināšanās ilga vidēji 8 nedēļas, izzuda, turpinot terapiju, un vairumā gadījumu bija saistīta ar vīrusu slodzes samazināšanos ≥ 2 log 10 kopijas / ml, kas bija pirms vai sakrita ar ALAT palielināšanos. Ārstēšanas laikā ieteicams periodiski kontrolēt aknu darbību (skatīt apakšpunktu 4.4).
Hepatīta paasinājumi pēc ārstēšanas pārtraukšanas
Klīniskie un laboratoriskie pierādījumi par hepatīta paasinājumu parādījās pacientiem ar HBV infekciju pēc HBV terapijas pārtraukšanas (skatīt apakšpunktu 4.4).
Pediatriskā populācija
HIV-1
Nevēlamo blakusparādību novērtējums ir balstīts uz diviem nejaušinātiem pētījumiem (pētījumi GS-US-104-0321 un GS-US-104-0352), kas veikti 184 bērniem (2 gadu vecumā un blakusparādību kopsavilkuma tabula un 5.1.).
Ir ziņots par KMB samazināšanos bērniem. HIV-1 inficētiem pusaudžiem KMB Z rādītāji, kas novēroti pacientiem, kuri lietoja tenofovira dizoproksila fumarātu, bija zemāki nekā pacientiem, kuri lietoja placebo. Bērniem, kas inficēti ar HIV-1, KMB Z rādītāji, kas novēroti pacientiem, kuri pārgāja uz tenofovira dizoproksila fumarātu, bija zemāki nekā tiem, kas tika novēroti pacientiem, kuri turpināja ārstēt ar stavudīnu vai zidovudīnu (skatīt apakšpunktus 4.4 un 5.1).
No 89 pacientiem (vecumā no 2 līdz
Hronisks B hepatīts
Nevēlamo blakusparādību novērtējums ir balstīts uz randomizētu pētījumu (pētījums GS-US-174-0115), kas veikts 106 pusaudžiem (12 gadu vecumā un blakusparādību kopsavilkuma tabula un 5.1.).
Pusaudžiem, kas inficēti ar HBV, tika novērots KMB samazinājums. KMB Z rādītāji, kas novēroti pacientiem, kuri lietoja tenofovira dizoproksila fumarātu, bija zemāki nekā pacientiem, kuri lietoja placebo (skatīt 4.4. Un 5.1. Apakšpunktu).
Citas īpašas populācijas
Vecāki cilvēki
Tenofovira dizoproksila fumarāts nav pētīts pacientiem, kas vecāki par 65 gadiem. Gados vecākiem pacientiem, visticamāk, ir pavājināta nieru darbība, tādēļ šo pacientu ārstēšanā tenofovira dizoproksila fumarāts jālieto piesardzīgi (skatīt apakšpunktu 4.4).
Pacienti ar nieru darbības traucējumiem
Tā kā tenofovira dizoproksila fumarāts var izraisīt nieru toksicitāti, pieaugušiem pacientiem ar nieru darbības traucējumiem, kas tiek ārstēti ar Viread, ieteicams rūpīgi uzraudzīt nieru darbību (skatīt 4.2., 4.4. Un 5.2. Apakšpunktu). Tenofovira dizoproksila fumarāta lietošana nav ieteicama pediatriskiem pacientiem ar nieru darbības traucējumiem (skatīt 4.2. Un 4.4. Apakšpunktu).
Ziņošana par iespējamām blakusparādībām
Ir svarīgi ziņot par iespējamām blakusparādībām, kas radušās pēc zāļu reģistrācijas, jo tas ļauj nepārtraukti uzraudzīt zāļu ieguvuma un riska attiecību. Veselības aprūpes speciālistus lūdz ziņot par visām iespējamām blakusparādībām, izmantojot valsts ziņošanas sistēmu:
Itālijas zāļu aģentūra
Vietne: http://www.agenziafarmaco.gov.it/it/responsabili
04.9 Pārdozēšana
Simptomi
Pārdozēšanas gadījumā pacients jānovēro, vai nav toksicitātes pazīmju (skatīt 4.8. Un 5.3. Apakšpunktu), un, ja nepieciešams, piemēro parasto atbalstošo aprūpi.
Vadība
Tenofoviru var izvadīt ar hemodialīzi; vidējais klīrenss hemodialīzei ir 134 ml / min. Nav zināms, vai tenofovīru var izvadīt ar peritoneālo dialīzi.
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS
05.1 Farmakodinamiskās īpašības
Farmakoterapeitiskā grupa: pretvīrusu līdzekļi sistēmiskai lietošanai; nukleozīdi un reversās transkriptāzes inhibējošie nukleotīdi, ATĶ kods: J05AF07
Darbības mehānisms un farmakodinamiskā iedarbība
Tenofovira dizoproksila fumarāts ir tenofovira dizoproksila priekšteča fumarāta sāls. Tenofovira dizoproksiils uzsūcas un pārvēršas par aktīvo vielu tenofoviru, kas ir monofosfāta (nukleotīda) nukleozīda analogs. Pēc tam tenofovīrs tiek pārveidots par aktīvo metabolītu tenofovira difosfātu, kas ir obligāts ķēdes izbeigšanas līdzeklis, izmantojot konstitutīvi izteiktus šūnu fermentus. Tenofovira difosfāta eliminācijas pusperiods aktivētajās perifēro asiņu mononukleārajās šūnās (PBMC) ir 10 stundas, bet atpūtas šūnās-50 stundas. Tenofovira difosfāts inhibē HIV-1 reverso transkriptāzi un vīrusu HBV polimerāzes, saistoties tiešā konkurencē ar dabisko substrātu dezoksiribonukleotīdu un caur DNS beigu ķēdi pēc iekļaušanas pašā DNS. Vai Tenofovira difosfāts ir vājš šūnu polimerāzes inhibitors? Un ?. Tenofovīrs testos neparādīja nekādu ietekmi uz mitohondriju DNS sintēzi vai pienskābes ražošanu in vitro, koncentrācijā līdz 300 mcmol / l.
Dati, kas saistīti ar HIV
HIV pretvīrusu līdzekļu aktivitāte in vitro: Tenofovira koncentrācija, kas nepieciešama 50% (EC50) inhibīcijai Mežonīgais tips laboratorijas HIV-1IIIB ir 1-6 μmol / l limfoīdo šūnu līnijās un 1,1 μmol / l pret primāriem HIV-1 B apakštipa izolātiem PBMC. Tenofovirs ir aktīvs arī pret HIV-1 A, C, D, E, F, G un O apakštipiem un pret HIVBaL primārajās monocītu / makrofāgu šūnās. Tenofovirs ir aktīvs in vitro pret HIV-2, ar EC50 4,9 μmol / l MT-4 šūnās.
Izturība: Viņi ir izvēlēti in vitro un dažiem pacientiem (skatīt Klīniskā efektivitāte un drošība) HIV-1 celmus ar zemāku jutību pret tenofovīru un reversās transkriptāzes K65R mutāciju. Jāizvairās no tenofovira dizoproksila fumarāta lietošanas pacientiem, kas iepriekš ārstēti ar pretretrovīrusu līdzekļiem un kuriem ir K65R mutācija (skatīt apakšpunktu 4.4). Turklāt tika izvēlēta K70E aizvietošana HIV-1 reversajā transkriptāzē ar tenofoviru, kā rezultātā nedaudz samazinājās jutība pret tenofoviru.
Klīniskajos pētījumos ar iepriekš ārstētiem pacientiem tika novērtēta 245 mg tenofovira dizoproksila (kā fumarāta) anti-HIV aktivitāte pret nukleozīdu inhibitoriem rezistentiem HIV-1 celmiem. Rezultāti liecina, ka pacientiem ar HIV, kuriem bija 3 vai vairākas mutācijas, kas saistītas ar timidīna analogiem ( TAM), kas ietvēra vai nu M41L, vai L210W reversās transkriptāzes mutāciju, bija samazināta jutība pret terapiju ar 245 mg tenofovira dizoproksila (fumarāta veidā).
Klīniskā efektivitāte un drošība
Tenofovira dizoproksila fumarāta aktivitātes pierādīšana HIV-1 inficētiem pacientiem ar iepriekšēju ārstēšanas pieredzi un iepriekš neapstrādātiem pacientiem ir pierādīta attiecīgi 48 nedēļas un 144 nedēļas ilgušos klīniskajos pētījumos.
Pētījumā GS-99-907 550 pieaugušiem pacientiem ar iepriekšēju ārstēšanas pieredzi 24 nedēļas tika dots vai nu placebo, vai 245 mg tenofovira dizoproksila (fumarāta veidā). Vidējais sākotnējais CD4 skaits bija 427 šūnas / mm3, vidējais sākotnējais plazmas HIV-1 RNS bija 3,4 log10 kopijas / ml (78% pacientu vīrusu slodze bija
24. nedēļā vidējās ar laiku svērtās izmaiņas plazmas HIV -1 RNS līmeņos log10 (DAVG24) bija -0,03 log10 kopijas / ml un -0,61 log10 kopijas / ml personām, kuras lietoja placebo un 245 mg tenofovira dizoproksila (fumarāta veidā) ) (lpp
144 nedēļu dubultmaskētā, kontrolētā pētījuma GS-99-903 fāzē tika novērtēta 245 mg tenofovira dizoproksila (fumarāta veidā) efektivitāte un drošums. pret stavudīnu, lietojot kombinācijā ar lamivudīnu un efavirenzu pieaugušiem HIV-1 inficētiem pacientiem, kuri iepriekš nav ārstēti ar pretretrovīrusu terapiju. Vidējais sākotnējais CD4 šūnu skaits bija 279 šūnas / mm3, vidējais sākotnējais HIV-1 RNS līmenis plazmā bija 4,91 log10 kopijas / ml, 19% pacientu bija simptomātiska HIV infekcija un 18% bija AIDS. Pacienti tika stratificēti pēc HIV-1 RNS un sākotnējā CD4 43% pacientu sākotnējā vīrusu slodze bija> 100 000 kopiju / ml, bet 39% - CD4 šūnu skaits
No "nodoma ārstēties" analīzes (trūkstošie dati un slēdži pretretrovīrusu terapijā (ART) tika uzskatīti par neveiksmīgiem)) pacientu īpatsvars ar HIV-1 RNS zem 400 kopijām / ml un 50 kopijām / ml 48 ārstēšanas nedēļās, tenofovira dizoproksila 245 mg grupā (fumarāta veidā) tas bija attiecīgi 80% un 76%, salīdzinot ar 84% un 80% stavudīna grupā. 144. nedēļā pacientu procentuālā daļa ar HIV-1 RNS zem 400 kopijām / ml un 50 kopijas / ml bija 71% un 68% tenofovira dizoproksila 245 mg grupā (fumarāta veidā), salīdzinot ar 64% un 63% stavudīna grupā.
Vidējās HIV-1 RNS un CD4 skaita izmaiņas ārstēšanas sākumā 48. nedēļā abās grupās bija līdzīgas (-3,09 un -3,09 log10 kopijas / ml; attiecīgi +169 un 167 šūnas / mm3. Grupa, kas tika ārstēta ar tenofovira dizoproksiilu 245 mg (fumarāta veidā) un grupā, kas ārstēta ar stavudīnu). Pēc 144 ārstēšanas nedēļām vidējās izmaiņas salīdzinājumā ar sākotnējo stāvokli abās grupās saglabājās līdzīgas (-3,07 un -3,03 log10 kopijas / ml; attiecīgi +263 un +283 šūnas / mm3 tenofovira dizoproksila (piemēram, fumarāta) un stavudīna grupās ). Neatkarīgi no sākotnējā HIV-1 RNS un CD4 skaita tika novērota konsekventa atbildes reakcija uz ārstēšanu ar 245 mg tenofovira dizoproksila (fumarāta veidā).
K65R mutācija radās nedaudz augstākai pacientu daļai tenofovira dizoproksila fumarāta grupā nekā aktīvajā kontroles grupā (2,7% pret 0,7%).Visos gadījumos rezistence pret efavirenzu vai lamivudīnu bija vai nu pirms, vai arī sakrita ar K65R attīstību. Astoņi pacienti, kuriem bija HIV ar K65R, 245 mg tenofovira dizoproksila grupā (fumarāta veidā); 7 no tiem tas notika pirmajās 48 ārstēšanas nedēļās un pēdējās - 96 nedēļās. Turpmāka K65R attīstība netika novērota līdz 144 nedēļām. Vienam pacientam tenofovira dizoproksila (fumarāta veidā) grupā attīstījās aizstāšana. vīruss Ne genotipiskā, ne fenotipiskā analīze neatklāja pierādījumus par citu rezistenci pret tenofoviru.
Dati, kas saistīti ar "HBV
Pretvīrusu HBV aktivitāte in vitro: Pretvīrusu aktivitāte in vitro Tenofovira un HBV līmenis tika novērtēts HepG2 2.2.15 šūnu līnijā. EC50 vērtības tenofovīram bija robežās no 0,14 līdz 1,5 μmol / l, un CC50 vērtības (50% citotoksiskā koncentrācija)> 100 mcmol / l .
Izturība: Nav konstatētas HBV mutācijas, kas saistītas ar rezistenci pret tenofovira dizoproksila fumarātu (skatīt Klīniskā efektivitāte un drošība). Šūnu testos HBV celmi, kas ekspresē rtV173L, rtL180M un rtM & SUP2; 04I / V mutācijas, kas saistītas ar lamivudīna un telbivudīna rezistenci, parādīja jutību pret tenofoviru 0,7 līdz 3,4 reizes vairāk nekā savvaļas tipa vīruss.
Klīniskā efektivitāte un drošība
HBV celmi, kas ekspresē rtL180M, rtT184G, rtS202G / I, rtM & SUP2; 04V un rtM & SUP2; 50V mutācijas, kas saistītas ar entekavīra rezistenci, parādīja jutību pret tenofoviru savvaļas tipa vīrusa 0,6 līdz 6,9 reižu diapazonā. rtA181V un rtN236T mutācijas, kas saistītas ar rezistenci pret adefovira dipivoksilu, parādīja jutību pret tenofoviru 2,9 līdz 10 reizes, salīdzinot ar savvaļas tipa vīrusu. Vīrusi, kas satur rtA181T mutāciju, paliek jutīgi pret tenofoviru ar EK vērtībām
Tenofovira dizoproksila fumarāta ieguvumu pierādījums kompensētas un dekompensētas slimības gadījumā ir balstīts uz viroloģiskām, bioķīmiskām un seroloģiskām reakcijām, ārstējot pieaugušos ar HBeAg pozitīvu un HBeAg negatīvu hronisku B hepatītu. Ārstētie pacienti bija pacienti, kuri iepriekš nebija ārstēti, pacienti ar iepriekšēju ārstēšanu ar lamivudīnu, pacienti ar iepriekšēju adefovira dipivoksila terapijas pieredzi un pacienti ar lamivudīna un / vai adefovira dipivoksila rezistences mutācijām. Ieguvumi ir pierādīti arī, pamatojoties uz histoloģiskām reakcijām kompensētiem pacientiem.
Pieredze pacientiem ar kompensētu aknu slimību 48. nedēļā (pētījumi GS-US-174-0102 un GS-US-174-0103)
48 nedēļu rezultāti no diviem dubultmaskētiem randomizētiem III fāzes pētījumiem, kuros salīdzināja tenofovira dizoproksiilu un adefovira dipivoksilu pieaugušiem pacientiem ar kompensētu aknu slimību, ir parādīti 4. tabulā. Pētījums GS-US-174-0103 tika veikts 266 HBeAg pozitīviem pacientiem (randomizēti un ārstēti), savukārt pētījums GS-US-174-0102 tika veikts 375 pacientiem (nejaušināti un ārstēti), kuriem bija negatīvs HBeAg un pozitīvs HBeAb.
Abos šajos pētījumos tika konstatēts, ka tenofovira dizoproksila fumarāts ir ievērojami pārāks par adefovira dipivoksilu attiecībā uz pilnīgas atbildes reakcijas primāro efektivitātes parametru (definēts kā HBV DNS līmenis).
Pētījumā GS-US-174-0103 ievērojami lielāka pacientu daļa, kuri lietoja tenofovira dizoproksila fumarātu, salīdzinot ar adefovira dipivoksila grupu, 48. nedēļā sasniedza ALAT normalizāciju un HBsAg zudumu (skatīt 4. tabulu zemāk) .50 1,5 reizes lielāks nekā savvaļas tipa vīruss.
4. tabula. Efektivitātes parametri 48 nedēļu laikā pacientiem ar HBeAg negatīvu un HBeAg pozitīvu kompensāciju
* P vērtība pret adefovira dipivoksils
pilnīga reakcija, kas definēta kā HBV DNS līmenis
b Knodela nekroiekaisuma indeksa uzlabošana par vismaz 2 punktiem, nepasliktinot Knodela fibrozi.
c HBV DNS vidējās izmaiņas salīdzinājumā ar sākotnējo līmeni tikai atspoguļo atšķirību starp "HBV DNS sākotnējā stāvoklī un identifikācijas robežu" (Noteikšanas robeža, LOD).
d ALAT normalizācijas analīzēs izmantotajā populācijā tika iekļauti tikai pacienti ar ALAT virs normas (ULN) sākotnēji.
n / a = nav piemērojams.
Tenofovira dizoproksila fumarāts bija saistīts ar ievērojami lielāku pacientu daļu ar nenosakāmu HBV DNS (
Kad pētījumi GS-US-174-0102 un GS-US-174-0103 tika apvienoti, atbildes reakcija uz ārstēšanu ar tenofovira dizoproksila fumarātu bija līdzīga pacientiem, kuri iepriekš bija ārstēti ar nukleozīdiem (n = 51), un pacientiem, kuri iepriekš nebija ārstēti ar nukleozīdiem (n = 375) un pacientiem ar normālu (n = 21) un nenormālu (n = 405) ALAT sākotnēji. Četrdesmit deviņi no 51 pacienta, kas iepriekš bija ārstēti ar nukleozīdu, iepriekš tika ārstēti ar lamivudīnu. Septiņdesmit trīs procenti pacientu, kas iepriekš bija ārstēti ar nukleozīdiem, un 69 procenti pacientu, kuri iepriekš nebija ārstēti, sasniedza pilnīgu atbildes reakciju uz ārstēšanu; 90% pacientu, kuri iepriekš bija ārstēti ar nukleozīdiem, un 88% pacientu, kuri iepriekš nebija ārstēti, sasniedza HBV DNS nomākumu
Pieredze ilgāk par 48 nedēļām pētījumos GS-US-174-0102 un GS-US-174-0103
Pētījumos GS-US-174-0102 un GS-US-174-0103 pēc 48 nedēļu dubultmaskētas terapijas (gan 245 mg tenofovira dizoproksila (fumarāta veidā), gan 10 mg adefovira dipivoksila) saņemšanas pacienti tika mainīti bez pārtraukuma. Ārstēšana ar atklātu terapiju ar tenofovira dizoproksila fumarātu. 77% un 61% pacientu, kas piedalījās attiecīgi pētījumos GS-US-174-0102 un GS-US-174-0103, turpināja pētījumu 384 nedēļas. 96., 144., 192., 240., 288. un 384. nedēļā virusoloģiskie pētījumi nomākums, bioķīmiskās un seroloģiskās reakcijas saglabājās, ilgstoši ārstējot ar tenofovira dizoproksila fumarātu (skatīt 5. un 6. tabulu zemāk).
5. tabula. Efektivitātes parametri 96, 144, 192, 240, 288 un 384 nedēļas pēc atklāta ārstēšanas pacientiem ar HBeAg negatīvu kompensāciju
Pētījums 174-0102 (HBeAg negatīvs)
Pamatojoties uz algoritmu Ilgtermiņa novērtējums (LTE analīze) - saucējā ir iekļauti pacienti, kuri pārtrauca terapiju pirms 384. nedēļas noteiktā protokola mērķa dēļ, kā arī tie, kuri terapiju pabeidza līdz 384. nedēļai.
b 48 nedēļas dubultmaskēts tenofovira dizoproksila fumarāts, kam seko 48 nedēļas atklāts marķējums.
c 48 nedēļas dubultmaskēts adefovira dipivoksils, kam seko 48 nedēļas atklāts tenofovira dizoproksila fumarāts.
d ALAT normalizācijas analīzēs izmantotajā populācijā tika iekļauti tikai pacienti ar ALAT virs normālā sākuma līmeņa.
un 48 nedēļas dubultmaskētu tenofovira dizoproksila fumarātu, kam sekoja 96 nedēļas atklāta etiķete.
f 48 nedēļas dubultaklā adefovira dipivoksila, kam sekoja 96 nedēļas atklāta tenofovira dizoproksila fumarāta lietošana.
g 48 nedēļas dubultmaskēts tenofovira dizoproksila fumarāts, kam sekoja 144 nedēļas atklāts marķējums.
h 48 nedēļas dubultmaskēts adefovira dipivoksils, kam seko 144 nedēļas atklāts tenofovira dizoproksila fumarāts.
48 nedēļas dubultmaskēts tenofovira dizoproksila fumarāts, kam sekoja 192 nedēļas atklāts marķējums.
48 nedēļas dubultmaskēts adefovira dipivoksils, kam seko 192 nedēļas atklāts tenofovira dizoproksila fumarāts.
k Viens šīs grupas pacients 240. nedēļas apmeklējuma laikā vispirms kļuva par HBsAg negatīvu un datu izslēgšanas brīdī vēl piedalījās pētījumā. Tomēr subjekta HBsAg zudums tika galīgi apstiprināts nākamajā vizītē.
l 48 nedēļas dubultmaskēts tenofovira dizoproksila fumarāts, kam seko 240 nedēļas ilga atklāta marķēšana.
m 48 nedēļas dubultmaskētā adefovira dipivoksila, kam sekoja 240 nedēļas atklāta tenofovira dizoproksila fumarāta lietošana.
n Parādītie skaitļi attiecas uz kumulatīvajiem procentiem, pamatojoties uz Kaplana Meiera analīzi, izņemot datus, kas savākti pēc emtricitabīna pievienošanas atklātam tenofovira dizoproksila fumarātam (KM-TDF).
vai 48 nedēļas dubultmaskētu tenofovira dizoproksila fumarātu, kam sekoja 336 nedēļas atklāts marķējums.
p 48 nedēļas dubultmaskētā adefovira dipivoksila, kam seko 336 nedēļas atklāta tenofovira dizoproksila fumarāta lietošana.
n / a = nav piemērojams.
6. tabula. Efektivitātes parametri 96, 144, 192, 240, 288 un 384 nedēļas pēc atklāta ārstēšanas pacientiem ar HBeAg pozitīvu kompensāciju
Pētījums 174-0103 (HBeAg pozitīvs)
Pamatojoties uz algoritmu Ilgtermiņa novērtējums (LTE analīze) - saucējā ir iekļauti pacienti, kuri pārtrauca terapiju pirms 384. nedēļas noteiktā protokola mērķa dēļ, kā arī tie, kuri terapiju pabeidza līdz 384. nedēļai.
b 48 nedēļas dubultmaskēts tenofovira dizoproksila fumarāts, kam seko 48 nedēļas atklāts marķējums.
c 48 nedēļas dubultmaskēts adefovira dipivoksils, kam seko 48 nedēļas atklāts tenofovira dizoproksila fumarāts.
d ALAT normalizācijas analīzēs izmantotajā populācijā tika iekļauti tikai pacienti ar ALAT virs normālā sākuma līmeņa.
un 48 nedēļas dubultmaskētu tenofovira dizoproksila fumarātu, kam sekoja 96 nedēļas atklāta etiķete.
f 48 nedēļas dubultaklā adefovira dipivoksila, kam sekoja 96 nedēļas atklāta tenofovira dizoproksila fumarāta lietošana.
g Parādītie skaitļi attiecas uz kumulatīvajiem procentiem, pamatojoties uz Kaplana Meiera analīzi, ieskaitot datus, kas savākti pēc emtricitabīna pievienošanas atklātajam tenofovira dizoproksila fumarātam (KM-ITT).
h 48 nedēļas dubultmaskēts tenofovira dizoproksila fumarāts, kam seko 144 nedēļas atklāts marķējums.
48 nedēļas dubultmaskēts adefovira dipivoksils, kam sekoja 144 nedēļas atklāts tenofovira dizoproksila fumarāts.
48 nedēļas dubultmaskēts tenofovira dizoproksila fumarāts, kam sekoja 192 nedēļas atklāts marķējums.
k 48 nedēļas dubultmaskēts adefovira dipivoksils, kam seko 192 nedēļas atklāts tenofovira dizoproksila fumarāts.
l Parādītie skaitļi attiecas uz kumulatīvajiem procentiem, pamatojoties uz Kaplana Meiera analīzi, izņemot datus, kas savākti pēc emtricitabīna pievienošanas atklātam tenofovira dizoproksila fumarātam (KM-TDF).
m 48 nedēļas dubultmaskēts tenofovira dizoproksila fumarāts, kam seko 240 nedēļas ilga atklāta marķēšana.
n 48 nedēļas dubultmaskēts adefovira dipivoksils, kam seko 240 nedēļas atklāts tenofovira dizoproksila fumarāts.
vai 48 nedēļas dubultmaskētu tenofovira dizoproksila fumarātu, kam sekoja 336 nedēļas atklāts marķējums.
p 48 nedēļas dubultmaskētā adefovira dipivoksila, kam seko 336 nedēļas atklāta tenofovira dizoproksila fumarāta lietošana.
Ir pieejami dati par sākotnējo stāvokli un 240. nedēļas aknu biopsiju par 331/489 pacientiem, kuri 240 nedēļas bija turpinājuši pētījumus GS-US-174-0102 un GS-US-174-0103 (skatīt 7. tabulu zemāk). Deviņdesmit pieci procenti (225/237) pacientu, kuriem sākotnēji nebija cirozes, un 99% (93/94) pacientu, kuriem sākotnēji bija ciroze, nemainīja vai uzlaboja fibrozi (Ishak fibrozes rādītājs). No 94 pacientiem, kuriem sākotnēji bija ciroze (Ishak fibrozes rādītājs: 5-6), 26% Ishak fibrozes rādītāju nemainījās un 72% bija cirozes regresija līdz 240. nedēļai, Ishaka fibrozes rādītājs samazinājās vismaz par 2 punktiem.
7. tabula. Histoloģiskā atbildreakcija (%) 240. nedēļā, salīdzinot ar sākotnējo stāvokli pacientiem ar HBeAg negatīvu un HBeAg pozitīvu kompensāciju
a Histoloģiskajā analīzē izmantotā populācija ietvēra tikai pacientus, kuriem bija pieejami aknu biopsijas dati (trūka = izslēgts) 240. nedēļā. Atbilde pēc emtricitabīna pievienošanas ir izslēgta (kopā 17 subjekti abos pētījumos).
b Knodell nekro -iekaisuma indeksa uzlabošana par vismaz 2 punktiem, nepasliktinoties Knodell fibrozes indeksam.
c 48 nedēļas dubultmaskēts tenofovira dizoproksila fumarāts, kam seko līdz 192 nedēļām atklāta etiķete.
d 48 nedēļas dubultmaskēts adefovira dipivoksils, kam seko līdz 192 nedēļām atklāts tenofovira dizoproksila fumarāts.
Pieredze ar HIV inficētiem pacientiem un iepriekšēja ārstēšana ar lamivudīnu
48 nedēļu randomizētā, dubultmaskētā kontrolētā 245 mg tenofovira dizoproksila (fumarāta veidā) pētījumā pieaugušiem pacientiem, kuri vienlaikus bija inficēti ar HIV-1 un hronisku B hepatītu, iepriekš ārstējot lamivudīnu (ACTG pētījums 5127), vidējais HBV līmenis plazmā sākotnēji Tenofovira grupā randomizētu pacientu DNS bija 9,45 log kopijas / ml (n = 27).Ārstēšana ar 245 mg tenofovira dizoproksila (fumarāta veidā) bija saistīta ar vidējām HBV DNS izmaiņām salīdzinājumā ar sākotnējo vērtību -5,74 log 10 kopijas / ml (n = 18). Turklāt 61% pacientu tika konstatēts normāls ALAT līmenis 48 nedēļu laikā.
Pieredze pacientiem ar pastāvīgu vīrusu replikāciju (pētījums GS-US-174-0106)
245 mg tenofovira dizoproksila (fumarāta veidā) vai 245 mg tenofovira dizoproksila (fumarāta veidā) plus 200 mg emtricitabīna efektivitāte un drošums tika novērtēts nejaušinātā dubultmaskētā pētījumā (pētījums GS-US-174-0106) HBeAg. pozitīvi un HBeAg negatīvi pieaugušie pacienti ar pastāvīgu virēmiju (HBV DNS ≥ 1000 kopijas / ml) terapijas laikā ar 10 mg adefovira dipivoksila ilgāk par 24 nedēļām. Sākotnēji 57% pacientu, kuri tika randomizēti tenofovira dizoproksila rokas fumarātam, salīdzinot ar 60% pacientu randomizēti emtricitabīna un tenofovira dizoproksila fumarāta grupai, iepriekš tika ārstēti ar lamivudīnu. Kopumā pēc 24 nedēļām ārstēšana ar tenofovira dizoproksila fumarātu izraisīja 66% (35/53) pacientu HBV DNS
Pieredze pacientiem ar dekompensētu aknu slimību 48 nedēļu laikā (pētījums GS-US-174-0108)
Pētījums GS-US-174-0108 ir randomizēts, dubultmaskēts, kontrolēts pētījums, lai novērtētu tenofovira dizoproksila fumarāta (n = 45), emtricitabīna plus tenofovira dizoproksila fumarāta (n = 45) un entekavīra (n = 45) drošību un efektivitāti. 22), pacientiem ar dekompensētu aknu slimību. Tenofovira dizoproksila fumarāta terapijas grupā pacientiem vidējais CPT rādītājs bija 7,2, vidējais HBV DNS līmenis 5,8 log kopijas / ml un vidējais plazmas ALAT līmenis 61 U / I sākotnēji . Četrdesmit divi procenti (19/45) pacientu iepriekšējo ārstēšanu ar lamivudīnu bija saņēmuši vismaz sešus mēnešus, 20% (9/45) pacienti iepriekš bija ārstēti ar adefovira dipivoksilu, bet 9 procentiem 45 pacientu (20%) bija rezistences mutācijas. sākotnēji saistīts ar lamivudīnu un / vai adefovira dipivoksilu. Primārie drošības mērķi bija pārtraukšana nevēlamas parādības dēļ un apstiprināts kreatinīna līmeņa paaugstināšanās plazmā ≥ 0,5 mg / dl vai apstiprinātā seruma fosfāta vērtība
Pacientiem ar CPT rādītāju ≤ 9 74% (29/39) tenofovira dizoproksila fumarāta grupas un 94% (33/35) emtricitabīna plus tenofovira dizoproksila fumarāta grupas sasniedza HBV DNS līmeni
Kopumā šī pētījuma dati ir pārāk ierobežoti, lai izdarītu stingrus secinājumus par emtricitabīna + tenofovira dizoproksila fumarāta salīdzinājumu. pret tenofovira dizoproksila fumarātu (skatīt 8. tabulu zemāk).
8. tabula. Drošības un efektivitātes parametri dekompensētiem pacientiem 48 nedēļu laikā
vērtībā lpp tenofovīru saturošu kombinēto roku salīdzinājums pret entekavīra grupa = 0,622,
b vērtība lpp tenofovīru saturošu kombinēto roku salīdzinājums pret entekavīra grupa = 1000.
Pieredze ilgāk par 48 nedēļām pētījumā GS-US-174-0108
"Ar vienādojumu balstītā analīzē" subjektiem, kuri nepabeidza ārstēšanu/kuri mainīja ārstēšanu = neveiksme ", 50% (21/42) pacientu, kuri saņēma tenofovira dizoproksila fumarātu, 76% (28/37) pacientu, kuri saņēma emtricitabīnu plus tenofovira dizoproksila fumarāts un 52% (11/21) pacientu, kuri saņēma entekavīru, sasniedza HBV DNS vērtības
Pieredze 96 nedēļu laikā pacientiem ar lamivudīnu rezistentu HBV (pētījums GS-US-174-0121)
245 mg tenofovira dizoproksila (fumarāta veidā) efektivitāte un drošums tika novērtēts randomizētā, dubultaklā pētījumā (GS-US-174-0121) ar HBeAg pozitīviem un HBeAg negatīviem (n = 280) pacientiem ar aknu slimību. virēmija (HBV DNS ≥ 1000 SV / ml) un genotipiski pierādījumi par rezistenci pret lamivudīnu (rtM & SUP2; 04I / V +/- rtL180M). Tikai pieciem sākotnēji bija ar adefoviru rezistenci saistītas mutācijas. Simts četrdesmit viens un 139 pieaugušie tika randomizēti attiecīgi tenofovira dizoproksila fumarāta un emtricitabīna plus tenofovira dizoproksila fumarāta terapijas grupām. Sākotnējā demogrāfija starp abām ārstēšanas grupām bija līdzīga: sākotnēji 52,5% pacientu bija HBeAg negatīvi, 47,5% bija HBeAg pozitīvi, vidējais HBV DNS līmenis bija attiecīgi 6,5 log kopijas / ml, un vidējais ALAT bija 79 V / L.
Pēc 96 ārstēšanas nedēļām 126 no 141 (89%) indivīdiem, kuri tika randomizēti tenofovira dizoproksila fumarātam, bija HBV DNS
Klīniskā rezistence
Četri simti divdesmit seši HBeAg negatīvi (GS-US-174-0102, n = 250) un HBeAg pozitīvi (GS-US-174-0103, n = 176) pacienti, kuri sākotnēji tika randomizēti dubultaklā ārstēšanai ar tenofovira dizoproksila fumarātu un pēc tam pārcelta uz ārstēšanu ar atklātu tenofovira dizoproksila fumarātu, tika novērtētas genotipiskās izmaiņas HBV polimerāzē, salīdzinot ar sākotnējo. Genotipiskie novērtējumi tika veikti visiem pacientiem ar HBV DNS> 400 kopijas / ml pie 48 (n = 39), 96 (n = 24) ), 144 (n = 6), 192 (n = 5), 240 (n = 4), 288 (n = 6) un 384 (n = 2) nedēļas, lietojot tenofovira dizoproksila fumarāta monoterapiju, parādīja, ka viņiem nav radušās saistītas mutācijas ar rezistenci pret tenofovira dizoproksila fumarātu.
Divi simti piecpadsmit HBeAg negatīvi (GS-US-174-0102, n = 125) un HBeAg pozitīvi (GS-US-174-0103, n = 90) pacienti, kuri sākotnēji tika randomizēti dubultaklā ārstēšanai ar adefovira dipivoksilu un pēc tam pārcelti uz ārstēšanu ar atklātu tenofovira dizoproksila fumarātu tika novērtētas genotipiskās izmaiņas HBV polimerāzē, salīdzinot ar sākotnējo. Genotipiskie novērtējumi tika veikti visiem pacientiem ar HBV DNS> 400 kopijas / ml pie 48 (n = 16), 96 (n = 5), 144 (n = 1), 192 (n = 2), 240 (n = 1), 288 (n = 1) un 384 (n = 2) nedēļas pēc tenofovira dizoproksila fumarāta monoterapijas parādīja, ka nav izveidojušās mutācijas, kas saistītas ar rezistenci pret tenofovira dizoproksila fumarātu.
Pētījumā GS-US-174-0108 45 pacienti (ieskaitot 9 pacientus ar lamivudīna un / vai adefovira dipivoksila rezistentajām mutācijām sākotnēji) saņēma tenofovira dizoproksila fumarātu līdz 168 nedēļām. 48. nedēļā 6/8 pacientiem ar HBV DNS> 400 kopijas / ml bija pieejami genotipiski dati no sākotnējiem un ārstēšanas HBV pāru izolātiem. Šajos izolātos netika konstatētas aminoskābju aizvietošanas, kas saistītas ar rezistenci pret tenofoviru. Dizoproksila fumarāts. pēc 48. nedēļas tika veikta 5 subjektiem tenofovira dizoproksila fumarāta grupā. Netika konstatētas aminoskābju aizvietošanas, kas saistītas ar rezistenci pret tenofovira dizoproksila fumarātu.
Pētījumā GS-US-174-0121 141 pacients ar lamivudīna rezistences aizstāšanu sākotnēji lietoja tenofovira dizoproksila fumarātu līdz 96 nedēļām. Genotipiskie dati no sākotnējiem un ārstēšanas HBV pāru izolātiem bija pieejami 6 no 9 pacientiem ar HBV DNS> 400 kopijas / ml pēdējā tenofovira dizoproksila fumarāta periodā. Šajos izolātos nav konstatētas aminoskābju aizvietošanas, kas saistītas ar rezistenci pret tenofovira dizoproksila fumarātu.
Pediatrijas pētījumā (GS-US-174-0115) 52 pacienti (ieskaitot 6 pacientus ar lamivudīna rezistences mutācijām sākotnēji) saņēma tenofovira dizoproksila fumarātu līdz 72 nedēļām. Genotipiskie novērtējumi tika veikti visiem pacientiem ar HBV DNS> 400 kopijas / ml 48 nedēļas (n = 6) un 72 nedēļas (n = 5). Šajos izolātos nav konstatētas aminoskābju aizvietošanas, kas saistītas ar rezistenci pret tenofovira dizoproksila fumarātu.
Pediatriskā populācija
HIV-1: Pētījumā GS-US-104-0321 87 ar HIV-1 inficēti pacienti ar iepriekšēju ārstēšanas pieredzi, 12 gadus veci un optimizētu fona režīmu (OBR) 48 nedēļas. Pētījuma ierobežojumu dēļ nav pierādīts tenofovira dizoproksila fumarāta ieguvums salīdzinājumā ar placebo, pamatojoties uz HIV-1 RNS līmeni plazmā 24. nedēļā. Tomēr ir sagaidāms ieguvums pusaudžu populācijai, pamatojoties uz "pieaugušo datu ekstrapolāciju un salīdzinošo farmakokinētiku" datus (skatīt 5.2. apakšpunktu).
Pacientiem, kuri tika ārstēti ar tenofovira dizoproksila fumarātu vai placebo, vidējais mugurkaula jostas daļas KMB Z rādītājs bija attiecīgi -1,004 un -0,809, un vidējais kopējais KMB Z rādītājs bija attiecīgi -0,866 un -0,584. Vidējās izmaiņas 48. nedēļā (dubultmaskētās fāzes beigās) bija -0.215 un -0.165 mugurkaula jostas daļas KMB Z rādītājam un -0.254 un -0.179 kopējam KMB Z rādītājam tenofovira grupās. , attiecīgi. Tenofovira dizoproksila fumarāta grupā vidējais KMB pieauguma temps bija mazāks nekā placebo grupā. 48. nedēļā sešiem pusaudžiem tenofovira dizoproksila fumarāta grupā un vienam pusaudzim placebo grupā ievērojami samazinājās mugurkaula jostas daļas KMB (definēts kā> 4% samazinājums). 28 pacientiem, kuri 96 nedēļas tika ārstēti ar tenofovira dizoproksila fumarātu, KMB Z rādītāji samazinājās par -0,341 mugurkaula jostas daļā un -0,458 visam ķermenim.
Pētījumā GS-US-104-0352 97 iepriekš ārstēti pacienti vecumā no 2 līdz zidovudīnam tika randomizēti, lai aizstātu stavudīnu vai zidovudīnu ar tenofovira dizoproksila fumarātu (n = 48) vai turpinātu sākotnējo režīmu (n = 49) 48 nedēļas. 48. nedēļā 83% pacientu tenofovira dizoproksila fumarāta terapijas grupā un 92% pacientu stavudīna vai zidovudīna terapijas grupā bija HIV-1 RNS koncentrācija.
Ir ziņots par KMB samazināšanos bērniem. Pacientiem, kuri tika ārstēti ar tenofovira dizoproksila fumarātu vai stavudīnu vai zidovudīnu, vidējais mugurkaula jostas daļas KMB Z rādītājs bija attiecīgi -1,034 un -0,489, un vidējais kopējais KMB Z rādītājs sākotnēji bija -0,471 un -0,386. Vidējās izmaiņas 48. nedēļā (randomizētās fāzes beigās) bija 0,032 un 0,087 mugurkaula jostas daļas KMB Z rādītājam un -0,184 un -0,027 kopējam KMB Z rādītājam attiecīgi tenofovira dizoproksila fumarāta grupās un stavudīns vai zidovudīns . Vidējais mugurkaula jostas daļas kaulu pieauguma ātrums 48. nedēļā bija līdzīgs tenofovira dizoproksila fumarāta grupā un stavudīna vai zidovudīna grupā. Kopējais kaulu audu pieaugums bija mazāks tenofovira dizoproksila fumarāta grupā, salīdzinot ar stavudīna vai zidovudīna grupu. Vienam pacientam, kas tika ārstēts ar tenofovira dizoproksila fumarātu, un nevienam subjektam, kas ārstēts ar stavudīnu vai zidovudīnu, KMB ievērojami (> 4%) samazinājās. mugurkaula jostas daļa 48. nedēļā. 64 pacientiem, kuri 96 nedēļas tika ārstēti ar tenofovira dizoproksila fumarātu, KMB Z rādītāji samazinājās par -0,012 mugurkaula jostas daļā un par -0,338 visam ķermenim, tie tika koriģēti atbilstoši svaram un augumam.
Pētījumā GS-US-104-0352 4 no 89 pediatriskiem pacientiem, kuri bija pakļauti tenofovira dizoproksila fumarātam, pārtrauca ārstēšanu, jo radās blakusparādības, kas atbilst proksimālajai nieru tubulopātijai (vidējā tenofovira dizoproksila fumarāta iedarbība: 104 nedēļas).
Hronisks B hepatīts: Pētījumā GS-US-174-0115 106 HBeAg negatīvi un HBeAg pozitīvi pacienti 12 gadu vecumā un interferons (> 6 mēnešus pirms skrīninga) vai jebkura cita anti-HBV perorāla nukleozīdu / nukleotīdu terapija, kas nesatur tenofovira dizoproksila fumarātu (> 16 nedēļas) pirms skrīninga). 72. nedēļā kopumā 88% (46/52) pacientu tenofovira dizoproksila fumarāta grupā un 0% (0/54) pacientu placebo grupā bija 1,5 reizes lielākas HBV DNS vērtības, salīdzinot ar “ULN”. tenofovira dizoproksila fumarāta grupā un 0% (0/32) pacientu placebo grupā bija HBV DNS vērtības
Neviens pacients neatbilda primārajam drošības mērķim -mugurkaula jostas daļas KMB samazinājums par 6%. Pacientiem, kuri tika ārstēti ar tenofovira dizoproksila fumarātu vai placebo, vidējais (SD) mugurkaula jostas daļas KMB Z rādītājs bija attiecīgi -0,43 un -0,28 un vidējais kopējais KMB Z rādītājs sākotnēji bija attiecīgi -0,20 un -0,26. no sākuma līdz 72. nedēļai bija -0,05 pacientiem, kuri tika ārstēti ar tenofovira dizoproksila fumarātu, un 0,07 pacientiem, kuri saņēma placebo. Vidējās izmaiņas kopējā KMB Z -0,15 ārstētiem pacientiem ar tenofovira dizoproksila fumarātu un 0,06 pacientiem, kuri saņēma placebo.KMB Z rādītāji netika pielāgoti svaram un augumam. Kopējais KMB un mugurkaula jostas daļas vidējais procentuālais pieaugums no sākotnējā stāvokļa līdz 72. nedēļai bija attiecīgi 2,84% un 4,95% pacientiem, kuri tika ārstēti ar tenofovira dizoproksila fumarātu. Šis vidējais kopējā KMB un mugurkaula jostas daļas procentuālais pieaugums bija par 2,53% un 3,19% mazāks, Trīs pacientiem no tenofovira dizoproksila fumarāta grupas un 2 pacientiem placebo grupā mugurkaula KMB samazinājās par> 4%.
Eiropas Zāļu aģentūra ir atlikusi pienākumu iesniegt pētījumu rezultātus ar Viread vienā vai vairākās pediatriskās populācijas apakšgrupās ar HIV un hronisku B hepatītu (informāciju par lietošanu bērniem skatīt 4.2. Apakšpunktā).
05.2 Farmakokinētiskās īpašības
Tenofovira dizoproksila fumarāts ir ūdenī šķīstošs esteris, kas ātri pārvēršas in vivo tenofovirā un formaldehīdā.
Šūnā tenofovirs tiek pārveidots par tenofovira monofosfātu un aktīvo sastāvdaļu - tenofovira difosfātu.
Uzsūkšanās
Pēc tenofovira dizoproksila fumarāta iekšķīgas lietošanas HIV inficētiem pacientiem šis savienojums ātri uzsūcas un pārvēršas par tenofoviru. Tenofovira dizoproksila fumarāta vairāku devu lietošana kopā ar maltīti HIV inficētiem pacientiem izraisīja tenofovira vidējās (% CV) Cmax, AUC un Cmin vērtības attiecīgi 326 (36,6%) ng / ml, 3,324 (41), 2 %) ng • h / ml un 64,4 (39,4%) ng / ml. Maksimālā tenofovira koncentrācija serumā tika novērota 1 stundas laikā pēc tukšā dūšā un 2 stundu laikā pēc ēšanas. Tenofovira perorālā biopieejamība no tenofovira dizoproksila fumarāta tukšā dūšā pacientiem bija aptuveni 25%. Tenofovira dizoproksila fumarāta ar augsta tauku satura maltīti palielināta iekšķīga lietošana biopieejamība, kā rezultātā tenofovira AUC palielinās par aptuveni 40% un Cmax par aptuveni 14%. Pēc tenofovira dizoproksila fumarāta pirmās ievadīšanas pacientiem pēc ēšanas vidējais seruma Cmax bija robežās no 213 līdz 375 ng / ml. Tomēr tenofovira dizoproksila fumarāta lietošana kopā ar vieglu maltīti būtiski neizraisīja tenofovira farmakokinētiku.
Izplatīšana
Pēc intravenozas ievadīšanas tenofovira līdzsvara stāvokļa tilpums tika lēsts aptuveni 800 ml / kg. Pēc tenofovira dizoproksila fumarāta iekšķīgas lietošanas tenofovirs izplatās lielākajā daļā audu, palielinoties koncentrācijai nierēs, aknās un zarnu saturā (preklīniskie pētījumi). Tenofovira koncentrācijas diapazonā no 0,01 līdz 25 mcg / ml saistīšanās in vitro tenofovira plazmas vai seruma proteīna bija attiecīgi mazāk nekā 0,7 un 7,2%.
Biotransformācija
Studijas in vitro konstatēja, ka ne tenofovira dizoproksila fumarāts, ne tenofovirs nav CYP450 enzīmu substrāti. Turklāt ievērojami augstākā koncentrācijā (aptuveni 300 reizes) nekā novērotā in vivo, tenofovirs neinhibēja in vitro zāļu metabolismu, ko nodrošina viena no galvenajām cilvēka CYP450 izoformām, kas iesaistīta zāļu biotransformācijā (CYP3A4, CYP2D6, CYP2C9, CYP2E1 vai CYP1A1 / 2). Koncentrācijās 100 μmol / l tenofovira dizoproksila fumarāts neietekmēja CYP450 izoformas, izņemot CYP1A1 / 2, kur tika novērots neliels (6%), bet statistiski nozīmīgs CYP1A1 / substrāta metabolisma samazinājums. Pamatojoties uz šiem datiem, klīniski nozīmīga mijiedarbība starp tenofovira dizoproksila fumarātu un zālēm, kuras metabolizējas caur CYP450, ir maz ticama.
Eliminācija
Tenofovirs galvenokārt tiek izvadīts caur nierēm, filtrējot un izmantojot aktīvu cauruļveida transporta sistēmu, un aptuveni 70-80% devas pēc intravenozas ievadīšanas izdalās nemainītā veidā ar urīnu. Tiek lēsts, ka kopējais klīrenss ir aptuveni 230 ml / stundā / kg (aptuveni 300 ml / min). Nieru klīrenss tika novērtēts aptuveni 160 ml / stundā / kg (aptuveni 210 ml / min), kas ir augstāka par glomerulārās filtrācijas ātrumu. ka aktīvā tubulārā sekrēcija ir svarīgs tenofovira eliminācijas elements. , tenofovira terminālais pusperiods ir aptuveni 12-18 stundas.
Pētījumos tika identificēts tenofovira aktīvās kanāliņu sekrēcijas ceļš, kas caur cilvēka organisko anjonu nesējiem 1 un 3 nonāk proksimālajās cauruļveida šūnās un ieplūst urīnā, izmantojot daudzrezistentus proteīnus 4 (MRP 4).
Linearitāte / nelinearitāte
Devu diapazonā no 75 līdz 600 mg tenofovira farmakokinētiskās īpašības nebija atkarīgas no tenofovira dizoproksila fumarāta devas, un atkārtotas devas tās neietekmēja.
Vecums
Farmakokinētikas pētījumi gados vecākiem cilvēkiem (vecākiem par 65 gadiem) vēl nav veikti.
Sekss
Ierobežotie dati par tenofovira farmakokinētiku sievietēm neliecina par būtisku ietekmi uz dzimumu.
Tautība
Farmakokinētika dažādās etniskajās grupās nav īpaši pētīta.
Pediatriskā populācija
HIV-1: Tenofovira līdzsvara stāvokļa farmakokinētika tika analizēta 8 pusaudžiem (vecumā no 12 līdz
9. tabula. Tenofovira vidējie (± SD) farmakokinētiskie parametri attiecībā uz vecuma grupu bērniem
Hronisks B hepatīts: Tenofovira līdzsvara stāvokļa iedarbība sasniegta pusaudžiem (vecumā no 12 līdz
Farmakokinētikas pētījumi ar bērniem līdz 2 gadu vecumam vēl nav veikti.
Nieru darbības traucējumi
Tenofovira farmakokinētiskie parametri tika noteikti pēc vienas 245 mg tenofovira dizoproksila devas ievadīšanas 40 pieaugušiem pacientiem, kas nav inficēti ar HIV un HBV, ar dažādas pakāpes nieru darbības traucējumiem, ko nosaka kreatinīna klīrenss (CrCl) pieaugušajiem (normāla nieru darbība, ja CrCl> 80 ml). / min; vidēji ar CrCl = 50-79 ml / min; mērens ar CrCl = 30-49 ml / min un smags ar CrCl = 10-29 ml / min). Salīdzinot ar pacientiem ar normālu nieru darbību, vidējā koncentrācija (%CV) palielinājās no 2185 (12%) ng • h / ml pacientiem ar CrCl> 80 ml / min līdz 3064 (30%) ng • h / ml, 6 009 ( 42%) ng • h / ml un 15 985 (45%) ng • h / ml attiecīgi pacientiem ar viegliem, vidēji smagiem un smagiem nieru darbības traucējumiem.
Farmakokinētikas modeļi, kas izstrādāti no vienas devas farmakokinētikas datiem pieaugušiem cilvēkiem, kas nav inficēti ar HIV un HBV, ar dažādiem nieru darbības traucējumiem, tika izmantoti, lai sniegtu ieteikumus par devām un devu diapazonus pieaugušajiem ar dažādiem nieru darbības traucējumiem (skatīt 4.2. Apakšpunktu).
Pieaugušiem pacientiem ar aprēķināto kreatinīna klīrensu (CrCl) 30–49 ml / min, 20–29 ml / min vai 10–19 ml / min ieteicamas attiecīgi 132 mg, 65 mg un 33 mg devas. Mg tenofovira disoproksila (fumarāta veidā) granulas vienu reizi dienā. Lai gan nav paredzams, ka šīs devas precīzi atspoguļo tenofovira farmakokinētisko profilu pacientiem ar normālu nieru darbību, kuri tiek ārstēti ar tenofovira dizoproksila (fumarāta veidā) 245 mg apvalkotām tabletēm, tiek pieņemts, ka tās ir vislabākā ieguvuma un riska attiecība pacientiem ar traucējumiem . nieru.
Personām ar nieru mazspēju beigu stadijā (beigu stadijas nieru slimība, ESRD) (CrCl
Tenofovira farmakokinētika pacientiem, kuriem nav hemodialīzes, ar peritoneālo dialīzi ar kreatinīna klīrensu vai citiem dialīzes veidiem nav pētīta.
Tenofovira farmakokinētika bērniem ar nieru darbības traucējumiem nav pētīta. Nav pieejami dati, lai ieteiktu devu (skatīt 4.2. Un 4.4. Apakšpunktu).
Vienu 245 mg tenofovira dizoproksila devu ievadīja pieaugušiem pacientiem, kas nav inficēti ar HIV un HBV, ar dažādas pakāpes aknu darbības traucējumiem, kā noteikts Child-Pugh-Turcotte (CPT) klasifikācijā. Pacientiem ar aknu darbības traucējumiem tenofovira farmakokinētika būtiski nemainījās, kas liecina, ka šiem pacientiem deva nav jāpielāgo. Cmax un AUC0-? Vidējais (% CV) tenofovira līmenis bija 223 (34,8%) ng / ml un 2050 (50,8%) ng • h / ml, attiecīgi 289 (46,0%) ng / ml un 2310 (43, 5%) ng • h / ml pacientiem ar vidēji smagiem aknu darbības traucējumiem un 305 (24,8%) ng / ml un 2740 (44,0%) ng • h / ml pacientiem ar smagiem aknu darbības traucējumiem.
Cilvēkiem proliferējošās perifēro asiņu mononukleārajās šūnās (PBMC) tika konstatēts, ka tenofovira difosfāta pusperiods ir aptuveni 50 stundas, bet fitohemoglutinīna stimulēto PBMC pusperiods ir aptuveni 10 stundas.
05.3 Preklīniskie drošības dati
Neklīniskie pētījumi par drošības farmakoloģija Atkārtotu devu toksicitātes pētījumu rezultāti žurkām, suņiem un pērtiķiem, kas bija līdzīgi vai augstāki par klīnisko iedarbību, un ar iespējamu klīnisku nozīmi ietver toksisku ietekmi uz nierēm un kauliem un samazinātu fosfāta koncentrāciju serumā. Kaulu toksicitāte tika diagnosticēta kā osteomalācija (pērtiķiem) un samazināts kaulu minerālais blīvums (KMB) (žurkām un suņiem). Žurkām un jauniem pieaugušiem suņiem kaulu toksicitāte radās, ja iedarbība ≥ 5 reizes pārsniedza pediatrisko vai pieaugušo pacientu iedarbību; inficētiem jauniem pērtiķiem toksicitāte pret kauliem radās pie ļoti lielas iedarbības pēc subkutānas ievadīšanas (≥ 40 reizes l pacienta iedarbības). Pētījumu rezultāti ar žurkām un pērtiķiem liecina par ar vielu saistītu fosfātu uzsūkšanās samazināšanos zarnās un iespējamu sekundāru KMB samazināšanos.
Genotoksicitātes pētījumi sniedza pozitīvus testa rezultātus in vitro uz peles limfomas ir viennozīmīgi rezultāti vienā no Amesa testā izmantotajiem celmiem un vāji pozitīvi rezultāti USD testā primārajiem žurku hepatocītiem. Tomēr tas bija negatīvs, izraisot mutācijas peles kaulu smadzeņu mikrokodolu testā. in vivo.
Aknu darbības traucējumi
Starpšūnu farmakokinētika
Mutes kancerogenitātes pētījumi ar žurkām un pelēm parādīja zemu divpadsmitpirkstu zarnas audzēju sastopamību, lietojot ārkārtīgi lielu devu pelēm. Maz ticams, ka šie audzēji ir nozīmīgi cilvēkiem.
Reproduktīvās toksicitātes pētījumi ar žurkām un trušiem neatklāja ietekmi uz pārošanos, auglību, grūtniecību vai augļa parametriem. Tomēr perioda un pēcdzemdību toksicitātes pētījumos tenofovira dizoproksila fumarāts, lietojot mātes toksiskas devas, samazināja dzīvotspēju un mazuļa svaru.
Aktīvā viela tenofovira dizoproksila fumarāts un tā galvenie transformācijas produkti saglabājas vidē.
06.0 FARMACEITISKĀ INFORMĀCIJA
06.1 Palīgvielas
Etilceluloze (E462)
Hidroksipropilceluloze (E463)
Mannīts (E421)
Silīcija dioksīds (E551)
06.2 Nesaderība
Nav būtisks.
06.3 Derīguma termiņš
3 gadi.
06.4 Īpaši uzglabāšanas nosacījumi
Uzglabāt temperatūrā līdz 25 ° C.
06.5 Tiešā iepakojuma veids un iepakojuma saturs
Augsta blīvuma polietilēna (ABPE) pudele ar bērniem neatveramu polipropilēna aizbāzni, kas satur 60 g granulu un mērglāzi.
06.6 Norādījumi lietošanai un lietošanai
Neizlietotās zāles un šo zāļu atkritumi jāiznīcina saskaņā ar vietējiem noteikumiem.
07.0 REĢISTRĀCIJAS APLIECĪBAS ĪPAŠNIEKS
Uzņēmums Gilead Sciences International Limited
Kembridža
CB21 6GT
Lielbritānija
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS
EU/1/01/200/003
035565035
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS
Reģistrācijas datums: 2002. gada 5. februāris
Pēdējās pārreģistrācijas datums: 2011. gada 14. decembris
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS
05/2015
11.0 RADIOZĀLĒM, PILNĪGI DATI PAR IEKŠĒJO RADIĀCIJAS DOSIMETRIJU
12.0 RADIOZĀLĒM, SĪKĀKAS SĪKĀKAS NORĀDĪJUMI PAR PAGATAVO GATAVOŠANU UN KVALITĀTES KONTROLI