Aktīvās sastāvdaļas: Acitretīns
Neotigason 10 mg cietās kapsulas
Neotigason 25 mg cietās kapsulas
Indikācijas Kāpēc lieto Neotigason? Kam tas paredzēts?
FARMAKOTERAPEUTISKĀ KATEGORIJA
Retinoīdi psoriāzes ārstēšanai
ĀRSTĒŠANAS INDIKĀCIJAS
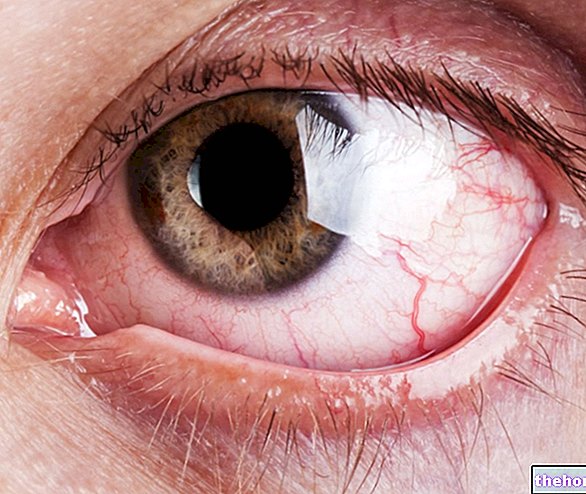
Smagas psoriāzes formas, ieskaitot formas, ko papildina artropātija.
Keratinizācijas traucējumi, piemēram, ihtiozveidīgie stāvokļi, plaukstu keratodermija, Darera slimība un plānais ķērpis.
Citas dermatozes, kas ir jutīgas pret Neotigason terapiju.
Kontrindikācijas Kad Neotigason nedrīkst lietot
- Paaugstināta jutība pret aktīvo vielu, citiem retinoīdiem vai kādu no palīgvielām.
- Neotigason ir ļoti teratogēns, un to nedrīkst dot grūtniecēm. Tas pats attiecas uz sievietēm reproduktīvā vecumā, ja vien viņas nelieto efektīvu kontracepcijas shēmu 4 nedēļas pirms ārstēšanas uzsākšanas, ārstēšanas laikā un trīs gadus pēc ārstēšanas pārtraukšanas (skatīt "Grūtniecība un zīdīšanas periods").
- Barošanas laiks.
- Smagi aknu darbības traucējumi.
- Smagi nieru darbības traucējumi.
- Pastāvīgi paaugstināts lipīdu līmenis serumā.
- Tā kā gan acitretīns, gan tetraciklīni var izraisīt paaugstinātu intrakraniālo spiedienu, to vienlaicīga lietošana ir kontrindicēta (skatīt "Mijiedarbība").
- Ir ziņots par paaugstinātu hepatīta risku pēc vienlaicīgas terapijas ar metotreksātu un etretinātu; līdz ar to arī metotreksāta un acitretīna vienlaicīga lietošana ir kontrindicēta (skatīt "Mijiedarbība").
- Acitretīna lietošana vienlaikus ar A vitamīnu vai citiem retinoīdiem ir kontrindicēta A hipervitaminozes attīstības riska dēļ (skatīt "Mijiedarbība").
Piesardzība lietošanā Kas jāzina pirms Neotigason lietošanas
Ārstam jāsniedz visiem pacientiem, sievietēm un vīriešiem, detalizēta informācija par teratogenitātes risku un veicamajiem stingrajiem kontracepcijas pasākumiem.
Klīniskie dati liecina, ka etretināts var veidoties, vienlaicīgi uzņemot acitretīnu un etilspirtu. Etretināts ir ļoti teratogēns, un tā eliminācijas pusperiods ir ilgāks (aptuveni 120 dienas) nekā acitretīnam.
Tādēļ sievietes reproduktīvā vecumā acitretīna terapijas laikā un divus mēnešus pēc acitretīna terapijas beigām nedrīkst lietot alkoholu (dzērienos, pārtikā vai narkotikās). Kontracepcijas pasākumi un grūtniecības testi jāveic 3 gadus pēc ārstēšanas ar acitretīnu pārtraukšanas (skatīt "Grūtniecība un zīdīšanas periods"). Sievietēm reproduktīvā vecumā nedrīkst saņemt pārlietas asinis no pacientiem, kuri ārstēti ar acitretīnu.
Tādēļ pacientiem, kas ārstēti ar acitretīnu, asiņu ziedošana ir aizliegta ārstēšanas laikā ar acitretīnu un trīs gadus pēc tā lietošanas pārtraukšanas.
Augļa anomāliju riska dēļ zāles nedrīkst dot citiem cilvēkiem. Neizlietotais vai derīguma termiņš ir jāatdod aptiekā iznīcināšanai.
Pirms ārstēšanas ar acitretīnu uzsākšanas jāpārbauda aknu darbība, pirmajos divos mēnešos ik pēc 1-2 nedēļām un pēc tam ik pēc trim mēnešiem.
Gadījumā, ja ir traucēta aknu darbība, monitorings tiks atkārtots ar iknedēļas intervālu. Ja pēc šīm pārbaudēm patoloģiskās vērtības nemainās vai pasliktinās, terapija ar acitretīnu tiek pārtraukta. Tomēr ir ieteicams turpināt uzraudzīt aknu darbību vēl vismaz trīs mēnešus (skatīt "Nevēlamās blakusparādības").
Holesterīna līmenis serumā un (tukšā dūšā) seruma triglicerīdu līmenis jāpārbauda pirms ārstēšanas uzsākšanas, vienu mēnesi pēc ārstēšanas sākuma un pēc tam ik pēc trim mēnešiem ārstēšanas laikā.
Ārstēšanas laikā ar acitretīnu tika novērota redzes samazināšanās naktī. Pacienti jāinformē par šo iespējamo blakusparādību un jābrīdina būt uzmanīgiem, vadot transportlīdzekļus vai apkalpojot mehānismus naktī. Rūpīgi jāuzrauga redzes problēmas (skatīt “Nevēlamās blakusparādības”).
Ir ziņots par retiem labdabīgas intrakraniālas hipertensijas gadījumiem. Pacientiem ar smagām galvassāpēm, sliktu dūšu, vemšanu un redzes traucējumiem nekavējoties jāpārtrauc ārstēšana ar acitretīnu un jāveic neiroloģisks novērtējums un ārstēšana (skatīt "Nevēlamās blakusparādības").
Pieaugušajiem, īpaši gados vecākiem cilvēkiem, kuri ilgstoši lieto acitretīna terapiju, periodiski jāveic atbilstošas pārbaudes, ņemot vērā iespējamās izmaiņas ossifikācijas procesos (skatīt "Nevēlamās blakusparādības"). Kaulēšanās problēmu gadījumā ārstam jāapspriež ar pacientu iespēja turpināt terapiju, pamatojoties uz riska / ieguvuma attiecības novērtējumu.
Ir bijuši ziņojumi par kaulu izmaiņām bērniem, tostarp priekšlaicīgu epifīzes blīvējumu, hiperostozi un skeleta pārkaļķošanos pēc ilgstošas ārstēšanas ar etretinātu; šos efektus var paredzēt, lietojot acitretīnu. Tādēļ bērniem rūpīgi jāuzrauga augšanas parametri un skeleta attīstība.
Jāuzsver, ka līdz šim nav zināmas visas iespējamās ilgstošas ārstēšanas ar acitretīnu sekas.
UV staru iedarbību akcentē retinoīdu terapija; tādēļ pacientiem jāizvairās no pārmērīgas saules gaismas iedarbības un nekontrolētas saules lampu lietošanas. Ja nepieciešams, jāizmanto sauļošanās līdzeklis ar augstu SPF vismaz 15.
Ārstēšana ar lielām retinoīdu devām var izraisīt garastāvokļa izmaiņas, tostarp aizkaitināmību, agresiju un depresiju.
Paaugstināta riska pacienti:
Pacientiem, kuri slimo ar diabētu, alkoholismu, aptaukošanos vai kuriem ir kardiovaskulāri riska faktori vai lipīdu metabolisma traucējumi un kuri tiek ārstēti ar acitretīnu, nepieciešama biežāka seruma lipīdu un / vai glikozes līmeņa asinīs un citu vērtību kontrole. asinsspiediena piemērs.
Diabēta slimniekiem retinoīdi var uzlabot vai pasliktināt glikozes toleranci; tādēļ ārstēšanas sākumposmā glikozes līmenis asinīs jāpārbauda biežāk nekā parasti.
Visiem augsta riska pacientiem, kuriem kardiovaskulārā riska rādītāji neatgriežas normālā stāvoklī vai vēl vairāk nepasliktinās, jāapsver devas samazināšana vai acitretīna terapijas pārtraukšana.
Mijiedarbība Kādas zāles vai pārtikas produkti var mainīt Neotigason iedarbību
Pastāstiet ārstam vai farmaceitam, ja nesen esat lietojis citas zāles, pat ja tās ir bez receptes.
Metotreksāta, tetraciklīnu vai A vitamīna un citu retinoīdu vienlaicīga lietošana ar acitretīnu ir kontrindicēta, skatīt "Kontrindikācijas".
Zema progesterona preparāti (minipillītes) var būt neatbilstoša kontracepcijas metode ārstēšanas laikā ar acitretīnu, skatīt "Grūtniecība un zīdīšanas periods".
Nav novērota mijiedarbība ar estrogēna / progestagēna kombinācijas perorālajiem kontracepcijas līdzekļiem.
Pētījumā, kas tika veikts ar veseliem brīvprātīgajiem, vienlaicīga acitretīna un alkohola devas lietošana izraisīja ļoti teratogēnu etretināta veidošanos.Šāda metabolisma procesa mehānisms nav noskaidrots, un tāpēc nav zināms, vai tas ir iespējams. mijiedarbība ar citām vielām. Tādēļ sievietes reproduktīvā vecumā acitretīna terapijas laikā un divus mēnešus pēc terapijas pārtraukšanas nedrīkst lietot alkoholu (dzērienos, pārtikā vai narkotikās) (skatīt "Piesardzība lietošanā").
Vienlaicīgas terapijas gadījumā ar acitretīnu un fenitoīnu jāpatur prātā, ka acitretīns samazina fenitoīna saistīšanos ar olbaltumvielām. Tā klīniskā nozīme vēl nav zināma.
Līdz šim nav novērota turpmāka mijiedarbība starp acitretīnu un citām vielām (piemēram, digoksīnu, cimetidīnu).
Pētījumi par acitretīna ietekmi uz kumarīna antikoagulantu (varfarīna) saistīšanos ar olbaltumvielām neuzrādīja nekādu mijiedarbību.
Brīdinājumi Ir svarīgi zināt, ka:
Pirms jebkuru zāļu lietošanas konsultējieties ar ārstu vai farmaceitu.
Grūtniecība un zīdīšanas periods
Sievietes reproduktīvā vecumā / Kontracepcija vīriešiem un sievietēm
Acitretīns ir ļoti teratogēns. Tā lietošana ir kontrindicēta sievietēm, kuras ārstēšanas laikā vai trīs gadu laikā pēc ārstēšanas pārtraukšanas var iestāties grūtniecība. Bērna ar nepareizu augšanu risks ir ārkārtīgi augsts, ja acitretīns ir lietots pirms grūtniecības vai grūtniecības laikā, neatkarīgi no ārstēšanas ilgums un devas.
Acitretīns ir kontrindicēts sievietēm reproduktīvā vecumā, izņemot gadījumus, kad ir šādi apstākļi:
- Pacientam ir smagas keratinizācijas izmaiņas, izturīgas pret standarta terapiju;
- Spēj saprast un ievērot ārsta norādījumus;
- Spēj droši un nepārtraukti izmantot saskaņoto kontracepcijas līdzekli, nepieļaujot kļūdas;
- Katrai sievietei reproduktīvā vecumā, kas saņem acitretīna terapiju, ir obligāti jālieto efektīvs kontracepcijas līdzeklis (vēlams divas papildu metodes), kas jāsāk 4 nedēļas pirms ārstēšanas un jāturpina tās laikā un trīs gadus pēc tās pārtraukšanas. Ja ir aizdomas par grūtniecību, pacientam nekavējoties jāsazinās ar ārstu.
- Terapiju nedrīkst sākt līdz nākamās menstruācijas otrajai vai trešajai dienai;
- Pirms terapijas uzsākšanas trīs dienas pirms pirmās devas ievadīšanas jānosaka negatīvs grūtniecības tests (minimālā jutība ir 25 mIU / ml). Terapijas laikā grūtniecības testi jāplāno ar 28 dienu intervālu. Pirms receptes izrakstīšanas šajās vizītēs obligāti jāveic negatīvs grūtniecības tests, kas nav vecāks par trim dienām. Pēc terapijas pārtraukšanas grūtniecības tests jāveic reizi 1-3 mēnešos 3 gadus pēc pēdējās devas.
- Pirms terapijas uzsākšanas ārstam sīki jāinformē reproduktīvā vecuma pacients par veicamajiem piesardzības pasākumiem, par ļoti nopietnu augļa anomāliju risku un par iespējamām grūtniecības sekām, kas sākās ārstēšanas laikā ar acitretīnu, kā arī trīs gadu laikā pēc tā pārtraukšanas;
- Efektīvu kontracepcijas līdzekļu lietošana jāturpina katru reizi, kad terapija tiek atkārtota, neatkarīgi no ārstēšanas perioda ilguma, un tā jāturpina trīs gadus pēc terapijas beigām;
- Grūtniecības gadījumā, neraugoties uz šiem piesardzības pasākumiem, pastāv augsts nopietnu augļa attīstības traucējumu risks (piemēram: galvaskausa -sejas defekti, sirds un asinsvadu vai CNS malformācijas, skeleta un aizkrūts dziedzera defekti) un palielināts spontānu abortu biežums. Šis risks rodas galvenokārt ārstēšanas laikā ar acitretīnu un 2 mēnešus pēc ārstēšanas. Līdz 3 gadiem pēc ārstēšanas ar acitretīnu pārtraukšanas risks ir mazāks (īpaši sievietēm, kuras nav lietojušas alkoholu), bet to nevar pilnībā izslēgt iespējamās etretināta veidošanās dēļ.
- Tādēļ sievietes reproduktīvā vecumā acitretīna terapijas laikā un divus mēnešus pēc terapijas pārtraukšanas nedrīkst lietot alkoholu (dzērienos, pārtikā vai narkotikās) (skatīt sadaļu "Piesardzība lietošanā" un "Mijiedarbība").
Galvenā kontracepcijas metode ir kombinēts hormonālais kontracepcijas līdzeklis vai intrauterīna ierīce, un ieteicams lietot arī prezervatīvu vai diafragmu. Preparāti, kas satur tikai progesteronu (mazas devas), nav ieteicami, jo tie var traucēt to kontracepcijas efektu.
Attiecībā uz vīriešiem, kas ārstēti ar acitretīnu, pieejamie dati par spermas un spermas iedarbību uz mātēm norāda uz minimālu teratogēnas iedarbības risku, ja tāds ir.
Grūtniecība
Acitretīns ir kontrindicēts grūtniecēm (skatīt "Kontrindikācijas").
Barošanas laiks
Acitretīnu nedrīkst dot sievietēm, kas baro bērnu ar krūti (skatīt "Kontrindikācijas").
Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus
Ārstēšanas laikā ar Neotigason novērota redzes samazināšanās naktī (skatīt "Nevēlamās blakusparādības"). Pacienti jāinformē par šo iespējamo problēmu un jāiesaka būt piesardzīgiem, vadot transportlīdzekli vai apkalpojot mehānismus naktī.
Svarīga informācija par kādu no Neotigason sastāvdaļām
Neotigason satur glikozi. Ja ārsts ir teicis, ka Jums ir kāda cukura nepanesība, pirms šo zāļu lietošanas konsultējieties ar ārstu.
Šīs zāles satur mazāk nekā 1 mmol (23 mg) nātrija katrā devā, ti, tās būtībā ir „nātriju nesaturošas”.
Devas un lietošanas veids Kā lietot Neotigason: Devas
Neotigason drīkst parakstīt tikai ārsti, kuriem ir pieredze sistēmisku retinoīdu lietošanā un kuri apzinās teratogenitātes risku, kas saistīts ar ārstēšanu ar acitretīnu.
Devas
Tā kā acitretīna uzsūkšanās un metabolisma pakāpe atšķiras, devu režīms būs jāpielāgo individuāli. Šīs direktīvas var sniegt tikai kā norādi.
Pieaugušie
Sākotnējā terapija:
25-30 mg dienā divas līdz četras nedēļas (1 kapsula pa 25 mg vai 3 kapsulas pa 10 mg).
Uzturošā terapija:
Uzturošā deva tiks noteikta, pamatojoties uz klīnisko efektivitāti un panesamību.Parasti 25-50 mg dienā, ievadot vēl sešas līdz astoņas nedēļas, tiek sasniegti optimāli terapeitiskie rezultāti.
Dažreiz var būt nepieciešams palielināt devu līdz maksimāli 75 mg dienā (3 kapsulas pa 25 mg). Pacientiem ar pietiekamu psoriātisko bojājumu regresiju terapiju var pārtraukt. Jebkuri recidīvi tiks ārstēti, kā aprakstīts iepriekš.
Ārstējot keratinizācijas traucējumus, bieži vien ir jāturpina uzturēšana pat tad, ja tiek lietotas ļoti mazas devas (pat mazāk nekā 20 mg dienā un ne vairāk kā 50 mg dienā).
Bērni
Ilgstošas ārstēšanas gadījumā, ņemot vērā iespējamu noteiktas smaguma pakāpes blakusparādību rašanos, rūpīgi jāizvērtē riska / ieguvuma attiecība. Acitretīnu drīkst lietot tikai tad, ja alternatīvas terapijas metodes nav efektīvas.
Devas jānosaka, ņemot vērā ķermeņa svaru. Ieteicamā dienas deva ir 0,5 mg / kg. Dažreiz ierobežotu laiku var būt nepieciešamas devas līdz 1 mg / kg dienā. Kopā nedrīkst pārsniegt 35 mg dienā. Uzturošā terapija jāveic ar minimālo efektīvo devu, ņemot vērā iespējamo blakusparādību rašanos ilgstošas ārstēšanas laikā.
Kombinētā terapija
Neotigason kombinācija ar citām terapijām un no tā izrietošā individuālā reakcija var attaisnot zāļu devas samazināšanu.
Vienlaicīga standarta lokālas terapijas lietošana netraucē Neotigason un to var turpināt.
Lietošanas veids
Kapsulas vēlams lietot vienu reizi dienā ēšanas laikā vai uzdzerot nedaudz piena.
Pārdozēšana Ko darīt, ja esat lietojis pārāk daudz Neotigason
Akūtas pārdozēšanas gadījumā Neotigason terapija nekavējoties jāpārtrauc.
Pārdozēšanas simptomi ir identiski akūtas A hipervitaminozes simptomiem, t.i., galvassāpes, reibonis, slikta dūša vai vemšana, miegainība, aizkaitināmība un nieze. Ņemot vērā preparāta akūto pamata toksicitāti, nav jāpiemēro īpaša ārstēšana.
Ja jums ir kādi jautājumi par Neotigason lietošanu, jautājiet savam ārstam vai farmaceitam.
Ja nejauši esat lietojis pārmērīgu Neotigason devu, nekavējoties informējiet par to ārstu vai dodieties uz tuvāko slimnīcu.
Blakusparādības Kādas ir Neotigason blakusparādības
Tāpat kā citas zāles, Neotigason var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas.
Nevēlamās blakusparādības novērotas lielākajai daļai pacientu, kas uzsāk terapiju ar acitretīnu. Tomēr šiem efektiem ir tendence izzust, samazinot devu vai pārtraucot terapiju. Dažreiz terapijas sākumā tika novērota arī sākotnējā psoriāzes simptomu pasliktināšanās.
Visbiežāk novērotās blakusparādības ir A hipervitaminozes simptomi, piemēram, sausas lūpas, kuras var mazināt, uzklājot ziedi.
Blakusparādības, par kurām ziņots acitretīnam klīniskajos pētījumos vai pēcreģistrācijas periodā, ir uzskaitītas zemāk pēc orgānu sistēmas un biežuma.
Biežums ir definēts šādi:
- Ļoti bieži (≥1 / 10)
- Bieži (≥ 1/100 līdz <1/10)
- Retāk (≥1 / 1000 līdz <1/100)
- Reti (≥1 / 10 000 līdz <1/1 000)
- Ļoti reti (<1/10 000)
- Nav zināms (biežumu nevar noteikt pēc pieejamiem datiem)
Infekcijas un invāzijas
- Biežums nav zināms: Candida albicans izraisīts vulvovaginīts
Imūnsistēmas traucējumi
- Biežums nav zināms: paaugstināta jutība
Nervu sistēmas traucējumi
- Bieži: galvassāpes
- Retāk: reibonis
- Reti: perifēra neiropātija
- Ļoti reti Labdabīga intrakraniāla hipertensija (skatīt "Piesardzība lietošanā")
Acu slimības
- Ļoti bieži: gļotādu sausums un iekaisums (piemēram, konjunktivīts, kseroftalmija), kas var izraisīt kontaktlēcu nepanesamību
- Retāk: neskaidra redze
- Ļoti reti: nakts aklums (skatīt "Piesardzība lietošanā"), čūlains keratīts
Ausu un labirinta traucējumi
- Biežums nav zināms: dzirdes traucējumi, troksnis ausīs
Asinsvadu patoloģijas
- Biežums nav zināms: pietvīkums
Elpošanas, krūšu kurvja un videnes slimības
- Ļoti bieži: gļotādu sausums un iekaisums (piemēram, deguna asiņošana un rinīts)
Kuņģa -zarnu trakta traucējumi
- Ļoti bieži: sausa mute, slāpes
- Bieži: stomatīts, kuņģa-zarnu trakta traucējumi (piemēram, sāpes vēderā, caureja, slikta dūša, vemšana)
- Retāk: gingivīts
- Biežums nav zināms: disgeizija, taisnās zarnas asiņošana
Aknu un / vai žultsceļu darbības traucējumi
- Retāk: hepatīts
- Ļoti reti: dzelte
Ādas un zemādas audu bojājumi
- Ļoti bieži: heilīts, nieze, alopēcija, ādas lobīšanās (visā ķermenī, īpaši uz plaukstām un zem kājām)
- Bieži: ādas trauslums, lipīga āda, dermatīts, neparasta matu struktūra, trausli nagi, paronihija, eritēma
- Retāk: plaisas, bullozs dermatīts, fotosensitivitātes reakcijas
- Biežums nav zināms: piogēna granuloma, madaroze, angioneirotiskā tūska, nātrene
Skeleta -muskuļu un saistaudu sistēmas bojājumi
- Bieži: artralģija, mialģija
- Ļoti reti: sāpes kaulos, eksostoze (balstterapija var izraisīt iepriekšējas mugurkaula hiperostozes progresēšanu, jaunus hiperostotiskus bojājumus un ekstrakeleta pārkaļķošanos, kā tas novērots ilgstošā sistēmiskā ārstēšanā ar retinoīdiem) (skatīt apakšpunktu "Piesardzība lietošanā").
Vispārēji traucējumi un reakcijas ievadīšanas vietā
- Bieži: perifēra tūska
Diagnostikas testi
- Ļoti bieži: patoloģiski aknu darbības testi (pārejoši, parasti atgriezeniski, sārmainu transamināžu un fosfatāžu līmeņa paaugstināšanās) (skatīt "Piesardzība lietošanā"). Lipīdu anomālijas (ārstēšanas laikā ar lielām acitretīna devām ir novērots atgriezenisks triglicerīdu un holesterīna līmeņa paaugstināšanās serumā) , īpaši augsta riska pacientiem un ilgstošai ārstēšanai (skatīt "Piesardzība lietošanā"). Nevar izslēgt saistītu ateroģenēzes risku, ja šie apstākļi saglabājas).
Bērni
Reizēm ir bijuši ziņojumi par kaulu izmaiņām bērniem, tostarp priekšlaicīgu epifīzes blīvējumu, hiperostozi un ekstraozu skeleta pārkaļķošanos pēc ilgstošas ārstēšanas ar etretinātu, šo ietekmi var paredzēt arī, lietojot acitretīnu. Bērniem rūpīgi jāuzrauga kaulu augšanas un attīstības parametri.
Diabētiķi
Retinoīdi var uzlabot vai pasliktināt glikozes toleranci (skatīt "Piesardzība lietošanā"). Ievērojot norādījumus lietošanas instrukcijā, samazinās blakusparādību risks.
Ziņošana par blakusparādībām
Ja Jums rodas jebkādas blakusparādības, konsultējieties ar ārstu vai farmaceitu. Tas attiecas arī uz iespējamām blakusparādībām, kas nav minētas šajā instrukcijā. Par nevēlamām blakusparādībām var ziņot arī tieši, izmantojot valsts ziņošanas sistēmu vietnē “www.agenziafarmaco.gov.it/it/responsabili.” Ziņojot par blakusparādībām, jūs varat palīdzēt iegūt vairāk informācijas par šo zāļu drošumu.
Derīguma termiņš un saglabāšana
Derīguma termiņš: skatiet derīguma termiņu, kas uzdrukāts uz iepakojuma. Brīdinājums: nelietojiet zāles pēc derīguma termiņa beigām, kas norādīts uz iepakojuma.
Derīguma termiņš attiecas uz produktu neskartā iepakojumā, pareizi uzglabātu.
Saglabāšanas metodes:
Uzglabāt temperatūrā līdz 25 ° C. Uzglabāt oriģinālajā traukā.
Zāles nedrīkst izmest kanalizācijā vai sadzīves atkritumos. Jautājiet farmaceitam, kā izmest zāles, kuras vairs nelietojat. Tas palīdzēs aizsargāt vidi.
SAGLABĀT ŠO ZĀĻU BĒRNIEM NEREDZAMĀ UN NEPIEEJAMĀ VIETĀ
Termiņš "> Cita informācija
SASTĀVS
Neotigason 10 mg cietās kapsulas
Viena kapsula satur:
- Aktīvā viela: acitretīns 10 mg.
- Palīgvielas: mikrokristāliskā celuloze, žāvēta šķidra izsmidzināta glikoze, želatīns un nātrija askorbāts.
- Kapsulas apvalks satur želatīnu, titāna dioksīdu (E 171), sarkano dzelzs oksīdu (E 172), melno dzelzs oksīdu (E 172) un dzelteno dzelzs oksīdu (E 172).
- Drukas tinte satur šellaku, melno dzelzs oksīdu (E172), propilēnglikolu un amonija hidroksīdu.
Neotigason 25 mg cietās kapsulas
Viena kapsula satur:
- Aktīvā viela: acitretīns 25 mg.
- Palīgvielas: mikrokristāliskā celuloze, žāvēta šķidra izsmidzināta glikoze, želatīns un nātrija askorbāts.
- Kapsulas apvalks satur želatīnu, titāna dioksīdu (E 171), sarkano dzelzs oksīdu (E 172), dzelteno dzelzs oksīdu (E 172) un melno dzelzs oksīdu (E 172).
- Drukas tinte satur šellaku, melno dzelzs hidroksīdu (E172), propilēnglikolu un amonija hidroksīdu.
ZĀĻU FORMA UN SATURS
Cietās kapsulas.
10 mg: kapsulas ar brūnu vāciņu un baltu korpusu ar uzrakstu “Actavis” melnā krāsā uz vāciņa un “10” melnā krāsā uz korpusa; izmēra kapsulas 4.
25 mg: kapsulas ar brūnu vāciņu un dzeltenu korpusu ar uzrakstu "Actavis" melnā krāsā uz vāciņa un "25" melnā krāsā uz korpusa; 1 izmēra kapsulas.
Neotigason 10 mg cietās kapsulas: 30 kapsulas.
Neotigason 25 mg cietās kapsulas: 20 kapsulas.
Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī. Pašlaik pieejamā informācija var nebūt atjaunināta.
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija.
01.0 ZĀĻU NOSAUKUMS -
NEOTIGASON CIETAS KAPSULAS
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS -
10 mg cietās kapsulas
Viena kapsula satur: Aktīvā viela: 10 mg acitretīna.
25 mg cietās kapsulas
Viena kapsula satur: Aktīvā viela: 25 mg acitretīna.
Palīgviela ar zināmu iedarbību: glikoze, nātrija askorbāts
Pilnu palīgvielu sarakstu skatīt apakšpunktā 6.1.
03.0 ZĀĻU FORMA -
Cietās kapsulas.
10 mg: kapsulas ar brūnu vāciņu un baltu korpusu ar uzrakstu “Actavis” melnā krāsā uz vāciņa un “10” melnā krāsā uz korpusa; izmēra kapsulas 4.
25 mg: kapsulas ar brūnu vāciņu un dzeltenu korpusu ar uzrakstu “Actavis” melnā krāsā uz vāciņa un “25” melnā krāsā uz korpusa; 1 izmēra kapsulas.
04.0 KLĪNISKĀ INFORMĀCIJA -
04.1 Terapeitiskās indikācijas -
Smagas psoriāzes formas, ieskaitot formas, ko papildina artropātija.
Keratinizācijas traucējumi, piemēram, ihtiozveidīgie stāvokļi, plaukstas keratoderma, Dārjē slimība, ķērpju plāns.
Citas dermatozes, kas ir jutīgas pret Neotigason terapiju.
04.2 Devas un lietošanas veids -
Neotigason drīkst parakstīt tikai ārsti, kuriem ir pieredze sistēmisku retinoīdu lietošanā un kuri apzinās teratogenitātes risku, kas saistīts ar ārstēšanu ar acitretīnu. Skatīt 4.6.
Devas
Tā kā acitretīna uzsūkšanās un metabolisma pakāpe atšķiras, devu režīms būs jāpielāgo individuāli. Šīs direktīvas var sniegt tikai kā norādi.
Pieaugušie
Sākotnējā terapija:
25-30 mg dienā divas līdz četras nedēļas (1 kapsula pa 25 mg vai 3 kapsulas pa 10 mg).
Uzturošā terapija:
Uzturošā deva tiks noteikta, pamatojoties uz klīnisko efektivitāti un panesamību.Parasti 25-50 mg dienā, ievadot vēl sešas līdz astoņas nedēļas, tiek sasniegti optimāli terapeitiskie rezultāti.
Dažreiz var būt nepieciešams palielināt devu līdz maksimāli 75 mg dienā (3 kapsulas pa 25 mg).
Pacientiem ar pietiekamu psoriātisko bojājumu regresiju terapiju var pārtraukt. Jebkuri recidīvi tiks ārstēti, kā aprakstīts iepriekš.
Ārstējot keratinizācijas traucējumus, bieži vien ir jāturpina uzturēšana pat tad, ja tiek lietotas ļoti mazas devas (pat mazāk nekā 20 mg dienā un ne vairāk kā 50 mg dienā).
Bērni
Ilgstošas ārstēšanas gadījumā, ņemot vērā iespējamu noteiktas smaguma pakāpes blakusparādību rašanos, rūpīgi jāizvērtē riska / ieguvuma attiecība. Acitretīnu drīkst lietot tikai tad, ja alternatīvas terapijas metodes nav efektīvas.
Devas jānosaka, ņemot vērā ķermeņa svaru. Ieteicamā dienas deva ir 0,5 mg / kg. Dažreiz ierobežotu laiku var būt nepieciešamas devas līdz 1 mg / kg dienā. Kopā nedrīkst pārsniegt 35 mg dienā. Uzturošā terapija jāveic ar minimālo efektīvo devu, ņemot vērā iespējamo blakusparādību rašanos ilgstošas ārstēšanas laikā.
Kombinētā terapija:
Neotigason kombinācija ar citām terapijām un no tā izrietošā individuālā reakcija var attaisnot zāļu devas samazināšanu.
Vienlaicīga standarta lokālas terapijas lietošana netraucē Neotigason un to var turpināt.
Lietošanas veids
Kapsulas vēlams lietot vienu reizi dienā ēšanas laikā vai uzdzerot nedaudz piena.
04.3 Kontrindikācijas -
Paaugstināta jutība pret aktīvo vielu, citiem retinoīdiem vai kādu no 6.1. Apakšpunktā uzskaitītajām palīgvielām.
Acitretīns ir ļoti teratogēns, un to nedrīkst ievadīt grūtniecēm. Tas pats attiecas uz sievietēm reproduktīvā vecumā, ja vien viņām 4 nedēļas pirms ārstēšanas uzsākšanas, ārstēšanas laikā un trīs gadus pēc ārstēšanas pārtraukšanas netiek veikta efektīva kontracepcijas shēma (skatīt 4.6. ).
Barošanas laiks.
Smagi aknu darbības traucējumi.
Smagi nieru darbības traucējumi.
Pastāvīgi paaugstināts lipīdu līmenis serumā.
Tā kā gan acitretīns, gan tetraciklīni var izraisīt intrakraniālā spiediena paaugstināšanos, to vienlaicīga lietošana ir kontrindicēta (skatīt apakšpunktu 4.5).
Ir ziņots par paaugstinātu hepatīta risku pēc vienlaicīgas terapijas ar metotreksātu un etretinātu; līdz ar to vienlaicīga metotreksāta un acitretīna lietošana ir kontrindicēta (skatīt 4.5. apakšpunktu).
Vienlaicīga acitretīna lietošana ar A vitamīnu vai citiem retinoīdiem ir kontrindicēta A hipervitaminozes attīstības riska dēļ (skatīt 4.5. Apakšpunktu).
04.4 Īpaši brīdinājumi un piesardzība lietošanā -
Ārstam jāsniedz visiem pacientiem, sievietēm un vīriešiem, detalizēta informācija par teratogenitātes risku un veicamajiem stingrajiem kontracepcijas pasākumiem.
Klīniskie dati liecina, ka etretināts var veidoties, vienlaicīgi uzņemot acitretīnu un etilspirtu. Etretināts ir ļoti teratogēns, un tā eliminācijas pusperiods ir ilgāks (aptuveni 120 dienas) nekā acitretīnam. Tādēļ sievietes reproduktīvā vecumā acitretīna terapijas laikā un divus mēnešus pēc acitretīna terapijas beigām nedrīkst lietot alkoholu (dzērienos, pārtikā vai narkotikās). Kontracepcijas pasākumi un grūtniecības testi jāveic 3 gadus pēc ārstēšanas ar acitretīnu pārtraukšanas (skatīt 4.6. Un 5.2. Apakšpunktu).
Sievietēm reproduktīvā vecumā nedrīkst saņemt pārlietas asinis no pacientiem, kuri ārstēti ar acitretīnu.Tādēļ pacientiem, kas ārstēti ar acitretīnu, asiņu ziedošana ir aizliegta ārstēšanas laikā ar acitretīnu un trīs gadus pēc tā lietošanas pārtraukšanas.
Augļa anomāliju riska dēļ zāles nedrīkst dot citiem cilvēkiem. Neizlietotais vai derīguma termiņš ir jāatdod aptiekā iznīcināšanai.
Aknu funkcijas jāpārbauda pirms ārstēšanas uzsākšanas ar acitretīnu, pirmajos divos mēnešos ik pēc 1-2 nedēļām un pēc tam ik pēc trim mēnešiem ārstēšanas laikā. Gadījumā, ja ir traucēta aknu darbība, monitorings tiks atkārtots ar intervālu. Šīs pārbaudes ļauj noteikt, ka patoloģiskās vērtības nemainās vai pasliktinās, ārstēšana ar acitretīnu tiks pārtraukta, tomēr ieteicams turpināt uzraudzīt aknu darbību vēl vismaz trīs mēnešus (skatīt apakšpunktu 4.8).
Holesterīna līmenis serumā un (tukšā dūšā) seruma triglicerīdu līmenis jāpārbauda pirms ārstēšanas uzsākšanas, vienu mēnesi pēc ārstēšanas sākuma un pēc tam ik pēc trim mēnešiem ārstēšanas laikā.
Ārstēšanas laikā ar acitretīnu tika novērota redzes samazināšanās naktī. Pacienti jāinformē par šo iespējamo nevēlamo ietekmi un jāiesaka būt uzmanīgiem, vadot transportlīdzekļus vai apkalpojot mehānismus naktī.Rūpīgi jāuzrauga redzes problēmas (skatīt 4.8.
Ir ziņots par retiem labdabīgas intrakraniālas hipertensijas gadījumiem. Pacientiem ar smagām galvassāpēm, sliktu dūšu, vemšanu un redzes traucējumiem nekavējoties jāpārtrauc ārstēšana ar acitretīnu un jāveic neiroloģiska izmeklēšana un ārstēšana (skatīt apakšpunktu 4.8).
Pieaugušajiem, īpaši gados vecākiem cilvēkiem, kuri ilgstoši ārstējas ar acitretīnu, periodiski jāveic atbilstošas pārbaudes, ņemot vērā iespējamās izmaiņas ossifikācijas procesos (skatīt 4.8. Apakšpunktu). Kaulēšanās problēmu gadījumā ārstam jāapspriež ar pacientu iespēja turpināt terapiju, pamatojoties uz riska / ieguvuma attiecības novērtējumu.
Ir bijuši ziņojumi par kaulu izmaiņām bērniem, tostarp priekšlaicīgu epifīzes blīvējumu, hiperostozi un skeleta pārkaļķošanos pēc ilgstošas ārstēšanas ar etretinātu; šos efektus var paredzēt, lietojot acitretīnu. Tādēļ bērniem rūpīgi jāuzrauga augšanas parametri un skeleta attīstība.
Jāuzsver, ka līdz šim nav zināmas visas iespējamās ilgstošas ārstēšanas ar acitretīnu sekas.
UV staru iedarbību akcentē retinoīdu terapija; tādēļ pacientiem jāizvairās no pārmērīgas saules gaismas iedarbības un nekontrolētas saules lampu lietošanas. Ja nepieciešams, jāizmanto sauļošanās līdzeklis ar augstu SPF vismaz 15.
Ārstēšana ar lielām retinoīdu devām var izraisīt garastāvokļa izmaiņas, tostarp aizkaitināmību, agresiju un depresiju.
Pacienti ar augstu risku:
Pacientiem, kuri slimo ar diabētu, alkoholismu, aptaukošanos vai kuriem ir kardiovaskulāri riska faktori vai lipīdu metabolisma traucējumi un kuri tiek ārstēti ar acitretīnu, nepieciešama biežāka seruma lipīdu un / vai glikozes līmeņa asinīs un citu vērtību kontrole. asinsspiediena piemērs.
Diabēta slimniekiem retinoīdi var uzlabot vai pasliktināt glikozes toleranci; tādēļ ārstēšanas sākumposmā glikozes līmenis asinīs jāpārbauda biežāk nekā parasti.
Visiem augsta riska pacientiem, kuriem kardiovaskulārā riska rādītāji neatgriežas normālā stāvoklī vai vēl vairāk nepasliktinās, jāapsver devas samazināšana vai acitretīna terapijas pārtraukšana.
Svarīga informācija par dažām sastāvdaļām
Satur glikozi. Pacientiem ar retām glikozes-galaktozes malabsorbcijas problēmām nevajadzētu lietot šīs zāles.
Šīs zāles satur mazāk nekā 1 mmol (23 mg) nātrija katrā devā, ti, tās būtībā ir „nātriju nesaturošas”.
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi -
Metotreksāta, tetraciklīnu vai A vitamīna un citu retinoīdu vienlaicīga lietošana ar acitretīnu ir kontrindicēta, skatīt apakšpunktu 4.3.
Zema progesterona preparāti (minipillītes) var būt neatbilstoša kontracepcijas metode ārstēšanas laikā ar acitretīnu, skatīt apakšpunktu 4.6. Nav novērota mijiedarbība ar estrogēna / progestagēna kombinācijas perorālajiem kontracepcijas līdzekļiem.
Pētījumā, kas tika veikts ar veseliem brīvprātīgajiem, vienlaicīga acitretīna un alkohola devas lietošana izraisīja ļoti teratogēnu etretināta veidošanos.Šāda metabolisma procesa mehānisms nav noskaidrots, un tāpēc nav zināms, vai tas ir iespējams. mijiedarbība ar citām vielām. Tādēļ sievietes reproduktīvā vecumā acitretīna terapijas laikā un divus mēnešus pēc acitretīna terapijas beigām nedrīkst lietot alkoholu (dzērienos, pārtikā vai narkotikās). (skatīt 4.4. un 5.2. apakšpunktu).
Vienlaicīgas terapijas gadījumā ar acitretīnu un fenitoīnu jāpatur prātā, ka acitretīns samazina fenitoīna saistīšanos ar olbaltumvielām. Tā klīniskā nozīme vēl nav zināma.
Līdz šim nav novērota turpmāka mijiedarbība starp acitretīnu un citām vielām (piemēram, digoksīnu, cimetidīnu).
Pētījumi par acitretīna ietekmi uz kumarīna antikoagulantu (varfarīna) saistīšanos ar olbaltumvielām neuzrādīja nekādu mijiedarbību.
04.6 Grūtniecība un zīdīšanas periods -
Sievietes reproduktīvā vecumā / Kontracepcija vīriešiem un sievietēm
Acitretīns ir ļoti teratogēns. Tā lietošana ir kontrindicēta sievietēm, kuras ārstēšanas laikā vai trīs gadu laikā pēc ārstēšanas pārtraukšanas var iestāties grūtniecība. Bērna ar nepareizu augšanu risks ir ārkārtīgi augsts, ja acitretīns ir lietots pirms grūtniecības vai grūtniecības laikā, neatkarīgi no ārstēšanas ilgums un devas.
Acitretīns ir kontrindicēts sievietēm reproduktīvā vecumā, izņemot gadījumus, kad ir šādi apstākļi:
1. Pacientam ir smagas keratinizācijas izmaiņas, izturīgas pret standarta terapiju;
2. Spēj saprast un ievērot ārsta dotos norādījumus;
3. spēj uzticami un nepārtraukti, bez neveiksmēm izmantot saskaņoto kontracepcijas līdzekli;
4. Katrai sievietei reproduktīvā vecumā, kas tiek ārstēta ar acitretīnu, ir obligāti jālieto efektīvs kontracepcijas līdzeklis (vēlams divas papildu metodes), kas jāsāk 4 nedēļas pirms terapijas un jāturpina visas ārstēšanas laikā un trīs gadus pēc tās pārtraukšanas. Ja ir aizdomas par grūtniecību, pacientam nekavējoties jāsazinās ar ārstu.
5. Terapiju nedrīkst uzsākt līdz nākamo menstruāciju otrajai vai trešajai dienai;
6. Pirms terapijas uzsākšanas trīs dienas pirms pirmās devas ievadīšanas jānosaka negatīvs grūtniecības tests (minimālā jutība 25 mIU / ml). Terapijas laikā grūtniecības testi jāplāno ar 28 dienu intervālu. Pirms receptes izrakstīšanas šajās vizītēs obligāti jāveic negatīvs grūtniecības tests, kas nav vecāks par trim dienām. Pēc terapijas pārtraukšanas grūtniecības tests jāveic reizi 1-3 mēnešos 3 gadus pēc pēdējās devas.
7. Pirms terapijas uzsākšanas ārstam ir sīki jāinformē reproduktīvā vecuma pacients par veicamajiem piesardzības pasākumiem, par ļoti nopietnu augļa anomāliju risku un par iespējamām grūtniecības sekām, kas sākās ārstēšanas laikā ar acitretīnu. kā trīs gadus pēc tās pārtraukšanas;
8. Efektīvu kontracepcijas līdzekļu lietošana jāturpina katru reizi, kad terapija tiek atkārtota, neatkarīgi no ārstēšanas perioda ilguma, un tā jāturpina trīs gadus pēc terapijas beigām;
9. Grūtniecības gadījumā, neraugoties uz šiem piesardzības pasākumiem, pastāv augsts nopietnu augļa attīstības traucējumu risks (piemēram: galvaskausa -sejas defekti, sirds un asinsvadu vai CNS malformācijas, skeleta un aizkrūts dziedzera defekti) un palielināts spontāno abortu biežums. Šis risks rodas galvenokārt ārstēšanas laikā ar acitretīnu un 2 mēnešus pēc ārstēšanas. Līdz 3 gadiem pēc ārstēšanas ar acitretīnu pārtraukšanas risks ir mazāks (īpaši sievietēm, kuras nav lietojušas alkoholu), bet to nevar pilnībā izslēgt iespējamās etretināta veidošanās dēļ.
10. Tādēļ sievietes reproduktīvā vecumā acitretīna terapijas laikā un divus mēnešus pēc acitretīna terapijas beigām nedrīkst lietot alkoholu (dzērienos, pārtikā vai narkotikās) (skatīt apakšpunktus 4.4, 4.5 un 4.5).
Galvenā kontracepcijas metode ir kombinēts hormonālais kontracepcijas līdzeklis vai intrauterīna ierīce, un ieteicams lietot arī prezervatīvu vai diafragmu. Preparāti, kas satur tikai progesteronu (mazas devas), nav ieteicami, jo tie var traucēt to kontracepcijas efektu.
Attiecībā uz vīriešiem, kas ārstēti ar acitretīnu, pieejamie dati par spermas un spermas iedarbību uz mātēm norāda uz minimālu teratogēnas iedarbības risku, ja tāds ir.
Grūtniecība
Acitretīns ir kontrindicēts grūtniecēm (skatīt apakšpunktu 4.3).
Barošanas laiks
Acitretīnu nedrīkst ievadīt sievietēm, kas baro bērnu ar krūti (skatīt apakšpunktu 4.3).
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus -
Ārstēšanas laikā ar Neotigason novērota redzes samazināšanās naktī (skatīt apakšpunktu 4.8). Pacienti jāinformē par šo iespējamo problēmu un jāiesaka būt piesardzīgiem, vadot transportlīdzekli vai apkalpojot mehānismus naktī.
04.8 Nevēlamās blakusparādības -
Nevēlamās blakusparādības novērotas lielākajai daļai pacientu, kas uzsāk terapiju ar acitretīnu. Tomēr šiem efektiem ir tendence izzust, samazinot devu vai pārtraucot terapiju. Dažreiz terapijas sākumā tika novērota arī sākotnējā psoriāzes simptomu pasliktināšanās.
Visbiežāk novērotās blakusparādības ir A hipervitaminozes simptomi, piemēram, sausas lūpas, kuras var mazināt, uzklājot ziedi.
Blakusparādības, par kurām ziņots acitretīnam klīniskajos pētījumos vai pēcreģistrācijas periodā, ir uzskaitītas zemāk pēc orgānu sistēmas un biežuma. Biežums ir definēts šādi:
Ļoti bieži (≥1 / 10)
Bieži (≥ 1/100,
Retāk (≥1 / 1000 līdz
Reti (≥1 / 10 000,
Ļoti rets (
Nav zināms (biežumu nevar noteikt pēc pieejamiem datiem).
Bērni
Reizēm ir bijuši ziņojumi par kaulu izmaiņām bērniem, tostarp priekšlaicīgu epifīzes blīvējumu, hiperostozi un ekstraozu skeleta pārkaļķošanos pēc ilgstošas ārstēšanas ar etretinātu, šo ietekmi var paredzēt arī, lietojot acitretīnu.
Bērniem rūpīgi jāuzrauga kaulu augšanas un attīstības parametri.
Diabētiķi
Retinoīdi var uzlabot vai pasliktināt glikozes toleranci (skatīt apakšpunktu 4.4).
Ziņošana par iespējamām blakusparādībām.
Ir svarīgi ziņot par iespējamām blakusparādībām, kas radušās pēc zāļu reģistrācijas, jo tas ļauj nepārtraukti uzraudzīt zāļu ieguvuma un riska attiecību. Veselības aprūpes speciālistus lūdz ziņot par visām iespējamām blakusparādībām, izmantojot valsts ziņošanas sistēmu. "Address:" www.agenziafarmaco.gov.it/it/responsabili ".
04.9 Pārdozēšana -
Akūtas pārdozēšanas gadījumā acitretīna terapija nekavējoties jāpārtrauc.
Pārdozēšanas simptomi ir identiski akūtas A hipervitaminozes simptomiem, t.i., galvassāpes, reibonis, slikta dūša vai vemšana, miegainība, aizkaitināmība un nieze. Ņemot vērā preparāta zemo akūto toksicitāti, nav nepieciešama īpaša apstrāde.
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS -
05.1 "Farmakodinamiskās īpašības -
Farmakoterapeitiskā grupa: retinoīdi psoriāzes ārstēšanai,
ATĶ kods: D05BB02
Acitretīns, Neotigason aktīvā sastāvdaļa, ir retīnskābes sintētisks aromātisks analogs. Klīniskie pētījumi apstiprināja, ka psoriāzes un keratinizācijas traucējumu gadījumā acitretīns normalizē epidermas šūnu proliferāciju, diferenciāciju un keratinizāciju ar parasti labi panesamām blakusparādībām. darbības mehānisms joprojām nav zināms.
05.2 "Farmakokinētiskās īpašības -
Uzsūkšanās
Acitretīns sasniedz maksimālo koncentrāciju plazmā 1 līdz 4 stundas pēc zāļu ievadīšanas.Vienreizējas perorālas devas bioloģiskā pieejamība ir aptuveni 60 %, bet var ievērojami atšķirties atkarībā no pacienta (36-95 %); jebkurā gadījumā tas ir lielāks, ja zāles ievada ēšanas laikā.
Izplatīšana
Acitretīns ir ļoti lipofils un ātri iekļūst audos. Zāļu saistīšanās ar plazmas olbaltumvielām pārsniedz 99%. Pētījumi ar dzīvniekiem liecina, ka acitretīns šķērso placentas barjeru tādā daudzumā, kas ir pietiekams, lai izraisītu augļa anomālijas, un tā lipofilitātes dēļ var pieņemt, ka ka tas nonāk mātes pienā ievērojamā daudzumā.
Vielmaiņa
Acitretīns tiek metabolizēts izomerizācijas ceļā uz tā 13 cis izomēru (Vai tu tur esi-acitretīns) glikuronizācijai un sānu ķēdes šķelšanai.
Eliminācija
Vairāku devu pētījumos pacientiem no 21 līdz 70 gadu vecumam eliminācijas pusperiods acitretīnam bija vidēji aptuveni 50 stundas un tā galvenajam metabolītam-60 stundas, Vai tu tur esi acitretīns, arī teratogēns. Sākot ar galīgo eliminācijas pusperioda vērtību, kas novērota acitretīnam (96 stundas) un Vai tu tur esi-acitretīns (123 stundas) un pieņemot lineāru kinētiku, var paredzēt, ka vairāk nekā 99% vielas tiks izvadīti 36 dienu laikā pēc pēdējās hroniskās terapijas devas ievadīšanas. Jāpiebilst arī, ka acitretīna koncentrācija plazmā un Vai tu tur esi acitretīns ir zem metodes noteikšanas robežas (žults un nieru trakts).
PIEZĪME
Pētījumā ar veseliem brīvprātīgajiem vienlaicīga acitretīna un etilspirta devas lietošana izraisīja etretināta veidošanos. Tas jau bija novērots in vitro. Nesenos pētījumos dažiem pacientiem, kas ārstēti ar acitretīnu, novērota arī etretināta veidošanās. Kamēr šī parādība nav pilnībā izskaidrota, jāņem vērā etretināta farmakokinētika.Etrteināts ir ļoti teratogēns un tam ir ilgāks eliminācijas pusperiods nekā acitretīnam (aptuveni 120 dienas).Tādēļ sievietes reproduktīvā vecumā acitretīna terapijas laikā un divus mēnešus pēc acitretīna terapijas beigām nedrīkst lietot alkoholu (dzērienos, pārtikā vai narkotikās). Kontracepcijas pasākumi jāsaglabā 3 gadus pēc ārstēšanas ar acitretīnu beigām.
05.3 Preklīniskie drošības dati -
Zāļu drošības pētījumi neatklāja mutagēnu vai kancerogēnu iedarbību vai tiešas toksicitātes problēmas aknās. Tika konstatēts, ka dzīvniekiem acitretīns ir ļoti teratogēns pat nelielās devās.
06.0 FARMACEITISKĀ INFORMĀCIJA -
06.1 Palīgvielas
Neotigason 10 mg cietās kapsulas
Mikrokristāliskā celuloze, žāvēta izsmidzināta šķidrā glikoze, želatīns un nātrija askorbāts.
Kapsulas apvalks satur želatīnu, titāna dioksīdu (E 171), sarkano dzelzs oksīdu (E 172), melno dzelzs oksīdu (E 172) un dzelteno dzelzs oksīdu (E 172).
Drukas tinte satur šellaku, melno dzelzs hidroksīdu (E172), propilēnglikolu un amonija hidroksīdu.
Neotigason 25 mg cietās kapsulas
Mikrokristāliskā celuloze, žāvēta izsmidzināta šķidrā glikoze, želatīns un nātrija askorbāts.
Kapsulas apvalks satur želatīnu, titāna dioksīdu (E 171), sarkano dzelzs oksīdu (E 172), dzelteno dzelzs oksīdu (E 172) un melno dzelzs oksīdu (E 172).
Drukas tinte satur šellaku, melno dzelzs hidroksīdu (E172), propilēnglikolu un amonija hidroksīdu.
06.2 Nesaderība "-
Nezinams.
06.3 Derīguma termiņš "-
3 gadi.
06.4 Īpaši uzglabāšanas nosacījumi -
Uzglabāt temperatūrā līdz 25 ° C. Uzglabāt oriģinālajā traukā.
06.5 Tiešā iepakojuma veids un iepakojuma saturs -
Kartona kastē kopā ar lietošanas instrukciju ievietoti alumīnija un plastmasas blistera iepakojumi.
Neotigason 10 mg cietās kapsulas: 30 kapsulas
Neotigason 25 mg cietās kapsulas: 20 kapsulas
06.6 Lietošanas un lietošanas instrukcijas -
Nav īpašu norādījumu par iznīcināšanu.
07.0 "REĢISTRĀCIJAS APLIECĪBAS" ĪPAŠNIEKS
Aurobindo Pharma (Itālija) s.r.l. - Via San Giuseppe, 102 - 21047 Saronno (Varēze)
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS -
Neotigason 10 mg cietās kapsulas - 30 kapsulas: AIC n. 027480019
Neotigason 25 mg cietās kapsulas - 20 kapsulas: AIC n. 027480021
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS -
Pirmās reģistrācijas datums: 26.04.1997
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS -
09/08/2016