Aktīvās sastāvdaļas: esomeprazols
LUCEN 20 mg zarnās šķīstošās tabletes
LUCEN 40 mg zarnās šķīstošās tabletes
Lucen iepakojuma ieliktņi ir pieejami šādu izmēru iepakojumiem: - LUCEN 20 mg zarnās šķīstošās tabletes, LUCEN 40 mg zarnās šķīstošās tabletes
- LUCEN 10 mg zarnās šķīstošās granulas suspensijas pagatavošanai paciņā
- LUCEN 40 mg pulveris injekciju / infūziju šķīduma pagatavošanai
Indikācijas Kāpēc lieto Lucen? Kam tas paredzēts?
LUCEN satur zāles, ko sauc par esomeprazolu. Tas pieder zāļu grupai, ko sauc par “protonu sūkņa inhibitoriem”, kas darbojas, samazinot kuņģa radītās skābes daudzumu.
LUCEN lieto šādu slimību ārstēšanai:
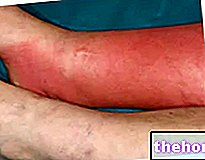
- "Gastroezofageālā refluksa slimība" (GERD). Tas rodas, kad skābe no kuņģa izplūst barības vadā (caurulē, kas savieno kaklu ar kuņģi), izraisot sāpes, iekaisumu un dedzināšanu.
- Kuņģa vai zarnu augšējās čūlas, kas inficētas ar baktērijām, ko sauc par "Helicobacter pylori" .Ja Jums ir šie apstākļi, ārsts var arī izrakstīt antibiotikas, lai ārstētu infekciju un ļautu čūlai dziedēt.
- Kuņģa čūlas, ko izraisa zāles, ko sauc par NPL (nesteroīdiem pretiekaisuma līdzekļiem).LUCEN var lietot arī, lai novērstu kuņģa čūlu veidošanos NPL lietošanas laikā.
- Pārmērīga kuņģa skābe, ko izraisa audzējs aizkuņģa dziedzerī (Zollinger-Ellisson sindroms).
- Ilgstoša čūlu asiņošanas ārstēšana pēc profilakses, ievadot Lucen intravenozi
Kontrindikācijas Kad Lucen nedrīkst lietot
Nelietojiet LUCEN šādos gadījumos:
- ja Jums ir alerģija (paaugstināta jutība) pret ezomeprazolu vai kādu citu (6. punktā minēto) šo zāļu sastāvdaļu.
- ja Jums ir alerģija pret citām protonu sūkņa inhibitoru zālēm (piemēram, pantoprazolu, lansoprazolu, rabeprazolu, omeprazolu).
- ja lietojat zāles, kas satur nelfinavīru (lieto HIV ārstēšanai).
Jums nevajadzētu lietot LUCEN, ja tas ietilpst kādā no iepriekš minētajiem gadījumiem. Ja rodas šaubas, pirms LUCEN lietošanas konsultējieties ar ārstu vai farmaceitu.
Piesardzība lietošanā Kas jāzina pirms Lucen lietošanas
Īpaša piesardzība, lietojot LUCEN, nepieciešama šādos gadījumos
Pirms LUCEN lietošanas konsultējieties ar ārstu vai farmaceitu, ja:
- Jums ir smagi aknu darbības traucējumi
- Jums ir smagi nieru darbības traucējumi.
LUCEN var maskēt citu slimību simptomus. Tādēļ, ja pirms LUCEN lietošanas sākšanas vai lietošanas laikā ar Jums notiek kāds no turpmāk minētajiem gadījumiem, nekavējoties pastāstiet ārstam:
- Jūs zaudējat daudz svara bez iemesla vai rodas apgrūtināta rīšana
- Rodas sāpes vēderā vai gremošanas traucējumi
- Sāciet vemt pārtiku vai asinis
- Izkārnījumi ir melni (izkārnījumi ar asinīm).
Ja Jums ir izrakstīts LUCEN "pēc vajadzības", sazinieties ar savu ārstu, ja simptomi saglabājas vai mainās īpašības.
Ja lietojat protonu sūkņa inhibitoru, piemēram, LUCEN, īpaši ilgāk par vienu gadu, Jums var būt nedaudz paaugstināts gūžas, plaukstas vai mugurkaula lūzuma risks. Ja Jums ir osteoporoze vai lietojat kortikosteroīdus (kas var palielināt osteoporoze), konsultējieties ar ārstu
Mijiedarbība Kuras zāles vai pārtikas produkti var mainīt Lucen iedarbību
Pastāstiet ārstam vai farmaceitam par visām zālēm, kuras lietojat vai pēdējā laikā esat lietojis, ieskaitot zāles, ko var iegādāties bez receptes.
Patiešām, LUCEN var ietekmēt dažu zāļu iedarbību un dažas zāles var ietekmēt LUCEN.Jums nevajadzētu lietot LUCEN, ja lietojat zāles, kas satur nelfinavīru (lieto HIV ārstēšanai).
Pastāstiet ārstam vai farmaceitam, ja lietojat kādas no šīm zālēm:
- Atazanavīrs (lieto HIV ārstēšanai)
- Klopidogrels (lieto, lai novērstu asins recekļu veidošanos)
- Ketokonazolu, itrakonazolu vai vorikonazolu (lieto sēnīšu izraisītu infekciju ārstēšanai).
- Erlotinibs (lieto vēža ārstēšanai).
- Citaloprams, imipramīns vai klomipramīns (lieto depresijas ārstēšanai).
- Diazepāms (lieto trauksmes ārstēšanai, muskuļu relaksācijai vai epilepsijas ārstēšanai).
- Fenitoīns (lieto epilepsijas ārstēšanai) Ja lietojat fenitoīnu, ārstam būs jānovēro, uzsākot vai pārtraucot ārstēšanu ar LUCEN.
- Zāles, ko lieto asiņu atšķaidīšanai, piemēram, varfarīns. Ārsts var jūs uzraudzīt, uzsākot vai pārtraucot ārstēšanu ar LUCEN.
- Cilostazols (lieto, lai ārstētu intermitējošu izliekumu - sāpes kājās staigājot nepietiekamas asins apgādes dēļ).
- Cisaprīdu (lieto gremošanas traucējumu un grēmas ārstēšanai).
- Digoksīns (lieto sirds slimību ārstēšanai).
- Metotreksāts (ķīmijterapijas zāles, ko lieto lielās devās vēža ārstēšanai) - ja lietojat lielas metotreksāta devas, ārsts var īslaicīgi pārtraukt ārstēšanu ar Lucen.
- Takrolīms (lieto orgānu transplantācijā)
- Rifampicīnu (lieto tuberkulozes ārstēšanai).
- Asinszāle (Hypericum perforatum) (lieto depresijas ārstēšanai).
Ja ārsts kopā ar LUCEN ir izrakstījis antibiotikas, piemēram, amoksicilīnu un klaritromicīnu Helicobacter pylori infekcijas izraisītu čūlu ārstēšanai, ir ļoti svarīgi pastāstīt ārstam par citām zālēm.
Brīdinājumi Ir svarīgi zināt, ka:
Grūtniecība un zīdīšanas periods
Pirms LUCEN lietošanas pastāstiet ārstam, ja esat grūtniece vai vēlaties grūtniecību. Pirms jebkuru zāļu lietošanas konsultējieties ar ārstu vai farmaceitu. Jūsu ārsts izlems, vai šajā laikā varat lietot LUCEN.
Nav zināms, vai LUCEN izdalās mātes pienā, tādēļ LUCEN nevajadzētu lietot, ja barojat bērnu ar krūti.
LUCEN lietošana kopā ar uzturu
Tabletes var lietot tukšā dūšā vai pilnā vēderā.
Transportlīdzekļu vadīšana un mehānismu apkalpošana
Maz ticams, ka LUCEN ietekmēs jūsu spēju vadīt transportlīdzekļus vai apkalpot mehānismus.
Svarīga informācija par kādu no LUCEN sastāvdaļām
LUCEN zarnās šķīstošās tabletes satur saharozi, kas ir cukura veids. Ja ārsts ir teicis, ka Jums ir “dažu cukuru nepanesamība, pirms zāļu lietošanas konsultējieties ar viņu.
Devas un lietošanas veids Kā lietot Lucen: Devas
Vienmēr lietojiet LUCEN tieši tā, kā ārsts Jums stāstījis. Ja rodas šaubas, konsultējieties ar ārstu vai farmaceitu.
- LUCEN zarnās šķīstošās tabletes nav ieteicamas bērniem līdz 12 gadu vecumam
- Ja esat lietojis šīs zāles ilgu laiku, ārsts jūs uzraudzīs (īpaši, ja esat lietojis šīs zāles ilgāk par gadu)
- Ja ārsts ir teicis lietot zāles pēc vajadzības, ja nepieciešams, lūdzu, pastāstiet ārstam, ja simptomi mainās.
Zāļu lietošana
- Jūs varat lietot tabletes jebkurā diennakts laikā.
- Jūs varat lietot tabletes pilnā vēderā vai tukšā dūšā.
- Norijiet tabletes veselas, uzdzerot ūdeni. Nesakošļājiet un nesasmalciniet tabletes, jo tās satur pārklātas granulas, kas aizsargā zāles no kuņģa skābuma.Tāpēc ir svarīgi nesabojāt granulas.
Ko darīt, ja Jums ir grūtības norīt tabletes
Ja Jums ir grūtības norīt tabletes:
- Ievietojiet tabletes glāzē negāzēta ūdens. Citus šķidrumus nedrīkst lietot
- Maisiet, līdz tabletes izšķīst (maisījumam nebūs skaidra izskata). Dzert nekavējoties vai vismaz 30 minūšu laikā. Vienmēr sajauc tos pirms dzeršanas
- Lai pārliecinātos, ka esat lietojis visas zāles, rūpīgi izskalojiet glāzi, līdz pusei piepildot ar ūdeni un dzeriet. Cietās daļiņas satur zāles, un tās nedrīkst sakošļāt vai sasmalcināt.
Ja jūs absolūti nevarat norīt, tableti var sajaukt ar nedaudz ūdens, ievietot šļircē un ievadīt caur cauruli tieši kuņģī (kuņģa caurulē).
Cik daudz medikamentu lietot
- Ārsts ieteiks, cik tablešu jālieto un cik ilgi. Tas ir atkarīgs no jūsu fiziskā stāvokļa, vecuma un aknu stāvokļa.
- Parastās devas ir norādītas zemāk.
Gastroezofageālā refluksa slimības (GERD) izraisītas grēmas ārstēšana:
Pieaugušie un bērni no 12 gadu vecuma:
- Ja ārsts ir konstatējis, ka jūsu barības vads ir nedaudz bojāts, parastā deva ir viena 40 mg LUCEN zarnās šķīstošā tablete vienu reizi dienā 4 nedēļas. Ja barības vads nav sadzijis, ārsts var ieteikt turpināt ārstēšanu, lietojot to pašu devu, vēl 4 nedēļas.
- Pēc barības vada dziedināšanas parastā deva ir viena 20 mg LUCEN zarnās šķīstošā tablete vienu reizi dienā.
- Ja barības vads nav bojāts, parastā deva ir viena LUCEN 20 mg zarnās šķīstošā tablete katru dienu. Kad simptomi tiek kontrolēti, ārsts informēs, ka nepieciešamības gadījumā varat lietot zāles, bet ne vairāk kā vienu rezistenta tablete Lucen 20 mg dienā.
- Ja Jums ir smagi aknu darbības traucējumi, ārsts noteiks mazāku devu.
Helicobacter pylori infekcijas izraisītu čūlu ārstēšana un to atkārtotas parādīšanās novēršana:
- Pieaugušie no 18 gadu vecuma: parastā deva ir viena LUCEN 20 mg zarnās šķīstošā tablete divas reizes dienā vienu nedēļu.
- Ārsts arī ieteiks lietot antibiotikas, ko sauc par amoksicilīnu un klaritromicīnu.
Kuņģa čūlu ārstēšana, ko izraisa NPL (nesteroīdie pretiekaisuma līdzekļi):
- Pieaugušie no 18 gadu vecuma: parastā deva ir viena LUCEN 20 mg zarnās šķīstošā tablete vienu reizi dienā 4 līdz 8 nedēļas.
Kuņģa čūlu profilakse, ja lietojat NPL (nesteroīdus pretiekaisuma līdzekļus):
- Pieaugušie no 18 gadu vecuma: parastā deva ir viena LUCEN 20 mg zarnās šķīstošā tablete vienu reizi dienā.
Pārmērīgas kuņģa skābes ārstēšana, ko izraisa aizkuņģa dziedzera augšana (Zollingera-Elisona sindroms):
- Pieaugušie no 18 gadu vecuma: parastā deva ir viena LUCEN 40 mg zarnās šķīstošā tablete divas reizes dienā.
- Ārsts pielāgos devu atbilstoši jūsu vajadzībām un arī izlems, cik ilgi turpināt ārstēšanu.
Maksimālā deva ir 80 mg divas reizes dienā.
Ilgstoša čūlu asiņošanas ārstēšana pēc profilakses, ievadot Lucen intravenozi:
Parastā deva ir viena Lucen 40 mg tablete vienu reizi dienā 4 nedēļas.
Pārdozēšana Ko darīt, ja esat lietojis pārāk daudz Lucen
Ja esat lietojis LUCEN vairāk nekā noteikts
Ja esat lietojis LUCEN vairāk nekā noteicis ārsts, nekavējoties pastāstiet par to savam ārstam vai farmaceitam.
Ja esat aizmirsis lietot LUCEN
- Ja esat aizmirsis lietot LUCEN devu, ieņemiet to, tiklīdz atceraties. Ja ir gandrīz pienācis laiks nākamajai devai, izlaidiet aizmirsto devu.
- Nelietojiet dubultu devu (divas devas vienlaikus), lai aizvietotu aizmirsto devu.
Blakusparādības Kādas ir Lucen blakusparādības
Tāpat kā citas zāles, LUCEN var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas.
Ja pamanāt kādu no šīm nopietnajām blakusparādībām, pārtrauciet LUCEN lietošanu un nekavējoties sazinieties ar ārstu:
- Pēkšņa sēkšana, lūpu, mēles un rīkles vai ķermeņa pietūkums, izsitumi, ģībonis vai rīšanas grūtības (smaga alerģiska reakcija).
- Ādas apsārtums ar pūslīšiem vai lobīšanos. Smagi pūslīši un asiņošana var parādīties arī lūpās, acīs, mutē, degunā un dzimumorgānos. Tas var būt "Stīvensa-Džonsona sindroms" vai "toksiska epidermas nekrolīze".
- Dzeltena āda, tumšs urīns un nogurums var būt aknu darbības traucējumu simptomi. Šie efekti ir reti, skar mazāk nekā 1 no 1000 cilvēkiem.
Citas blakusparādības ir:
Bieži (skar mazāk nekā 1 no 10 cilvēkiem):
- Galvassāpes.
- Ietekme uz kuņģi vai zarnām: caureja, sāpes vēderā, aizcietējums, meteorisms.
- Slikta dūša vai vemšana.
Retāk (skar mazāk nekā 1 no 100 cilvēkiem):
- Pietūkums pēdās un potītēs.
- Miega traucējumi (bezmiegs).
- Reibonis, adatas, miegainība.
- Reibonis.
- Sausa mute
- Izmaiņas asins analīzēs, kas pārbauda aknu darbību.
- Ādas izsitumi, nātrene un nieze.
- Gūžas, plaukstas locītavas vai mugurkaula lūzums (ja Lucen lieto lielās devās un ilgstoši).
Reti (skar mazāk nekā 1 no 1000 cilvēkiem):
- Asins problēmas, piemēram, samazināts balto asins šūnu un trombocītu skaits. Tas var izraisīt vājumu, zilumus vai iespēju vieglāk inficēties.
- Zems nātrija līmenis asinīs. Tas var izraisīt vājumu, vemšanu un krampjus.
- Uzbudinājuma, apjukuma vai depresijas sajūta.
- Garšas izmaiņas.
- Redzes problēmas, piemēram, neskaidra redze.
- Pēkšņa sēkšana vai elpas trūkums (bronhu spazmas).
- Mutes iekšpuses iekaisums.
- Infekcija, ko sauc par "piena sēnīti", kas var ietekmēt zarnas un ko izraisa sēne.
- Aknu darbības traucējumi, tostarp dzelte, kas var izraisīt dzeltenu ādu, tumšu urīnu un nogurumu.
- Matu izkrišana (alopēcija).
- Ādas izsitumi saulē.
- Locītavu sāpes (artralģija) vai muskuļu sāpes (mialģija).
- Vispārēja slikta pašsajūta un spēka trūkums.
- Paaugstināta svīšana.
Ļoti reti (skar mazāk nekā 1 no 10 000 cilvēkiem):
- Izmaiņas asins šūnu skaitā, ieskaitot agranulocitozi (balto asins šūnu trūkums).
- Agresija.
- Redzēt, sajust vai dzirdēt lietas, kas tur nav (halucinācijas).
- Smagi aknu darbības traucējumi, kas izraisa aknu mazspēju un smadzeņu iekaisumu.
- Pēkšņi sākās smagi izsitumi vai pūslīši vai ādas lobīšanās. Tas var būt saistīts ar paaugstinātu drudzi un locītavu sāpēm (multiformā eritēma, Stīvensa-Džonsona sindroms, toksiska epidermas nekrolīze).
- Muskuļu vājums.
- Smagi nieru darbības traucējumi.
- Krūšu palielināšanās vīriešiem.
Nav zināms (biežumu nevar noteikt pēc pieejamiem datiem)
- Ja lietojat LUCEN ilgāk par trim mēnešiem, magnija līmenis asinīs var pazemināties. Zems magnija līmenis var izpausties ar nogurumu, piespiedu muskuļu kontrakcijām, dezorientāciju, krampjiem, reiboni, paātrinātu sirdsdarbību. Ja Jums rodas kāds no šiem simptomiem, nekavējoties konsultējieties ar ārstu. Zems magnija līmenis var izraisīt arī kālija vai kalcija līmeņa pazemināšanos asinīs. Ārstam jāizlemj, vai periodiski pārbaudīt magnija līmeni asinīs.
- Iekaisums zarnās (izraisot caureju).
Ļoti retos gadījumos LUCEN var ietekmēt baltās asins šūnas, izraisot imūndeficītu. Ja Jums ir infekcija ar tādiem simptomiem kā drudzis ar smagu vispārējā fiziskā stāvokļa pasliktināšanos vai drudzis ar vietējas infekcijas simptomiem, piemēram, sāpes kaklā, rīklē vai mutē vai apgrūtināta urinēšana, jums pēc iespējas ātrāk jāredz ārsts ka, veicot asins analīzi, var izslēgt balto asins šūnu trūkumu (agranulocitozi). Jums ir svarīgi sniegt informāciju par zālēm, kuras lietojat. Neuztraucieties par iepriekš minēto iespējamo blakusparādību sarakstu. Iespējams, ka neviens neparādīsies.Ja novērojat jebkādas blakusparādības, kas šajā instrukcijā nav minētas, vai kāda no minētajām blakusparādībām Jums izpaužas smagi, lūdzu, izstāstiet to savam ārstam vai farmaceitam.
Derīguma termiņš un saglabāšana
- Uzglabāt bērniem nepieejamā un neredzamā vietā.
- Uzglabāt temperatūrā līdz 30 ° C.
- Uzglabāt oriģinālajā iepakojumā (blisterī) vai uzglabāt cieši noslēgtu (pudelē), lai pasargātu no mitruma.
- Nelietot tabletes pēc derīguma termiņa beigām, kas norādīts uz kastītes, maciņa vai blistera. Derīguma termiņš attiecas uz mēneša pēdējo dienu.
- Zāles nedrīkst izmest kanalizācijā vai sadzīves atkritumos. Jautājiet farmaceitam, kā izmest zāles, kuras vairs nelietojat. Tas palīdzēs aizsargāt vidi.
CITA INFORMĀCIJA
Ko LUCEN satur
Aktīvā viela ir esomeprazols. LUCEN zarnās šķīstošās tabletes ir 2 stiprumos, kas satur 20 vai 40 mg ezomeprazola (magnija trihidrāta veidā).
Citas sastāvdaļas ir: glicerīna monostearāts 40-55, hipoloze, hipromeloze, dzelzs oksīds (sarkanbrūns, dzeltens) (E172, tikai 20 mg tabletēm), magnija stearāts, metakrilskābes kopolimēra etilakrilāta (1: 1) dispersija 30 ° C temperatūrā. %, mikrokristāliskā celuloze, sintētiskais parafīns, makrogoli, polisorbāts 80, krospovidons, nātrija stearilfumarāts, saharozes sfēras (saharoze un kukurūzas ciete), talks, titāna dioksīds (E171), trietilcitrāts.
LUCEN izskata un iepakojuma satura apraksts
- LUCEN 20 mg zarnās šķīstošās tabletes ir gaiši rozā krāsā ar A / EH vienā pusē un 20 mg otrā pusē.
- LUCEN 40 mg zarnās šķīstošās tabletes ir rozā krāsā ar A / EI vienā pusē un 40 mg otrā pusē.
- Tabletes ir iepakotas blisteros, maciņos un / vai pudelēs
- 20 mg, 40 mg: pudele ar 2-5-7-14-15-28-30-56-60-100-140 (28x5) tabletēm.
- 20 mg, 40 mg: blisteris vai maciņa blisteris pa 3-7-7x1-14-15-25x1-28-30-50x1- 56-60-90-98-100x1-140 tabletēm.
Visi iepakojuma lielumi tirgū var nebūt pieejami
Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī. Pašlaik pieejamā informācija var nebūt atjaunināta.
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija.
01.0 ZĀĻU NOSAUKUMS
LUCENTIS 10 MG / ML Šķīdums injekcijām
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS
Viens ml satur 10 mg ranibizumaba *. Katrs flakons satur 2,3 mg ranibizumaba 0,23 ml šķīduma.
* Ranibizumabs ir humanizēts monoklonāls antivielu fragments, kas ražots Escherichia coli ar rekombinantās DNS tehnoloģiju.
Pilnu palīgvielu sarakstu skatīt apakšpunktā 6.1.
03.0 ZĀĻU FORMA
Injicējams šķīdums
Dzidrs, bezkrāsains līdz gaiši dzeltens ūdens šķīdums.
04.0 KLĪNISKĀ INFORMĀCIJA
04.1 Terapeitiskās indikācijas
Lucentis ir indicēts pieaugušajiem:
• Ar vecumu saistītas neovaskulāras (mitras) makulas deģenerācijas (AMD) ārstēšana
• Diabētiskās makulas tūskas (DME) izraisītu redzes traucējumu ārstēšana
• Redzes traucējumu ārstēšana, ko izraisa "tīklenes vēnu oklūzijas (zaru RVO vai centrālās RVO) izraisītas makulas tūskas"
• Redzes traucējumu ārstēšana, ko izraisa koroidālā neovaskularizācija (CNV), kas ir sekundāra patoloģiskas tuvredzības (PM) dēļ
04.2 Devas un lietošanas veids
Lucentis jāievada kvalificētam oftalmologam, kam ir pieredze intravitreālas injekcijās.
Devas mitras AMD ārstēšanai
Ieteicamā Lucentis deva ir 0,5 mg katru mēnesi, ievadot vienu intravitreālu injekciju. Tas atbilst 0,05 ml injicētajam tilpumam.
Ārstēšana tiek veikta reizi mēnesī un tiek turpināta, līdz tiek sasniegts maksimālais redzes asums, ti, pacienta redzes asums ir stabils trīs secīgas ikmēneša pārbaudes laikā, kas tiek veiktas ārstēšanas laikā ar ranibizumabu.
Tādēļ pacientu redzes asums jāpārbauda katru mēnesi.
Ārstēšana jāatjauno, ja novērošana liecina par redzes asuma samazināšanos mitras AMD dēļ. Pēc tam jāinjicē ikmēneša injekcijas, līdz atkal tiek sasniegts stabils redzes asums trīs secīgās ikmēneša pārbaudēs (tas nozīmē vismaz divas injekcijas). Intervāls starp divām devām nedrīkst būt mazāks par vienu mēnesi.
Devas DME vai makulas tūskas izraisītu redzes traucējumu ārstēšanai, ko izraisa RVO
Ieteicamā Lucentis deva ir 0,5 mg katru mēnesi, ievadot vienu intravitreālu injekciju. Tas atbilst 0,05 ml injicētajam tilpumam.
Ārstēšana tiek veikta reizi mēnesī un tiek turpināta, līdz tiek sasniegts maksimālais redzes asums, ti, pacienta redzes asums ir stabils trīs secīgas ikmēneša pārbaudes laikā, kas tiek veiktas ārstēšanas laikā ar ranibizumabu. Ja pirmo trīs injekciju laikā redzes asums neuzlabojas, ārstēšanu nav ieteicams turpināt.
Tādēļ pacientu redzes asums jāpārbauda katru mēnesi.
Ārstēšana jāatjauno, ja novērošana liecina par redzes asuma samazināšanos DME vai makulas tūskas dēļ, ko izraisa RVO. Pēc tam ikmēneša injekcijas jāievada, līdz atkal tiek sasniegts stabils redzes asums trīs ikmēneša pārbaudēs. Pēc kārtas (tas ietver vismaz divas injekcijas). Intervāls starp divām devām nedrīkst būt mazāks par vienu mēnesi.
Lucentis un lāzera fotokoagulācija DME un makulas tūskas gadījumā, kas ir sekundāra BRVO
Ir zināma pieredze par Lucentis lietošanu vienlaikus ar lāzera fotokoagulāciju (skatīt 5.1. Apakšpunktu). Lucentis jāievada tajā pašā dienā vismaz 30 minūtes pēc lāzera fotokoagulācijas. Lucentis var ievadīt pacientiem, kuri iepriekš saņēmuši lāzera fotokoagulāciju.
Devas CNV izraisītu redzes traucējumu ārstēšanai, ko izraisa PM
Ārstēšana jāsāk ar vienu injekciju.
Ja novērošana atklāj slimības aktivitātes pazīmes, piemēram, redzes asuma samazināšanos un / vai traumas pazīmes, ieteicama turpmāka ārstēšana.
Slimību uzraudzība var ietvert klīnisko pārbaudi, optisko koherences tomogrāfiju (AZT) vai fluoresceīna angiogrāfiju (FA).
Lai gan dažiem pacientiem pirmajā ārstēšanas gadā var būt nepieciešama tikai viena vai divas injekcijas, dažiem var būt nepieciešama biežāka ārstēšana (skatīt 5.1. Apakšpunktu). Tāpēc pirmajos divos mēnešos un vismaz reizi trijos mēnešos pirmajā ārstēšanas gadā ieteicams veikt ikmēneša uzraudzību. Pēc pirmā gada uzraudzības biežumu var noteikt ārsts.
Intervāls starp divām devām nedrīkst būt mazāks par vienu mēnesi.
Lucentis un fotodinamiskā terapija ar Visudyne CNV sekundārajā PM
Nav pieredzes par Lucentis lietošanu kombinācijā ar Visudyne.
Īpašas populācijas
Aknu mazspēja
Lucentis nav pētīts pacientiem ar aknu mazspēju. Tomēr šai polācijai nav nepieciešami īpaši apsvērumi.
Nieru mazspēja
Pacientiem ar nieru mazspēju devas pielāgošana nav nepieciešama (skatīt 5.2. Apakšpunktu).
Pensionāriem
Gados vecākiem cilvēkiem deva nav jāpielāgo. Ir ierobežota pieredze par pacientiem ar DME, kas vecāki par 75 gadiem.
Pediatriskā populācija
Lucentis drošība un efektivitāte, lietojot bērniem un pusaudžiem līdz 18 gadu vecumam, nav pierādīta.
Lietošanas veids
Vienreizējas lietošanas flakoni tikai intravitreālai lietošanai.
Pirms lietošanas Lucentis vizuāli jāpārbauda, vai tajā nav daļiņu un vai nav mainījusies krāsa.
Injekcijas procedūra jāveic aseptiskos apstākļos, kas ietver roku dezinfekciju tāpat kā jebkurai ķirurģiskai procedūrai, sterilus cimdus, sterilu drapējumu un sterilu blefarostatu (vai līdzvērtīgu) un iespēju veikt sterilu paracentēzi (ja nepieciešams) pirms intravitreālās procedūras rūpīgi jāizvērtē pacienta paaugstinātas jutības reakcijas vēsture (skatīt apakšpunktu 4.4). Pirms injekcijas jāievada atbilstoša anestēzija un plaša spektra lokāls pretmikrobu līdzeklis, lai dezinficētu periokulāro, acs un plakstiņu virsmu saskaņā ar klīnisko praksi.
Informāciju par Lucentis sagatavošanu skatīt 6.6. Apakšpunktā.
Ievietojiet injekcijas adatu 3,5–4,0 mm aiz ekstremitāšu stiklveida kamerā, izvairoties no horizontālā meridiāna un virzot adatu uz acs ābola centru. Ievadiet 0,05 ml injekcijas tilpumu; nomainiet sklera vietu nākamajām injekcijām.
04.3 Kontrindikācijas
Paaugstināta jutība pret aktīvo vielu vai jebkuru no 6.1. Apakšpunktā uzskaitītajām palīgvielām.
Pacienti ar esošām vai aizdomām par acu vai periokulārām infekcijām.
Pacienti ar ilgstošu smagu intraokulāru iekaisumu.
04.4 Īpaši brīdinājumi un piesardzība lietošanā
Reakcijas, kas saistītas ar intravitreālu injekciju
Intravitreālas injekcijas, ieskaitot Lucentis, ir saistītas ar endoftalmītu, intraokulāru iekaisumu, tīklenes regmatogēnu atslāņošanos, tīklenes plīsumu un jatrogēnu traumatisku kataraktu (skatīt apakšpunktu 4.8). Lucentis ievadīšanai vienmēr jāizmanto atbilstošas aseptiskas injekcijas metodes. Turklāt pacienti jānovēro nedēļā pēc injekcijas, lai infekcijas gadījumā varētu ātri ārstēties. Pacienti jāinformē, kā nekavējoties ziņot par jebkādiem simptomiem, kas liecina par endoftalmītu vai kādu no iepriekš minētajiem notikumiem.
Palielinās acs iekšējais spiediens
60 minūšu laikā pēc Lucentis injekcijas novērots pārejošs acs iekšējā spiediena (IOP) pieaugums. Ir novērota arī ilgstoša IOP palielināšanās (skatīt 4.8. Apakšpunktu). Ir jākontrolē un atbilstoši jāārstē acs iekšējais spiediens un redzes nerva galvas perfūzija.
Divpusēja ārstēšana
Ierobežoti dati par Lucentis divpusēju lietošanu (ieskaitot vienas dienas devu) neliecina par paaugstinātu sistēmisku blakusparādību risku, salīdzinot ar vienpusēju ārstēšanu.
Imunogenitāte
Lietojot Lucentis, pastāv iespēja imunogenitātei. Tā kā pacientiem ar DME ir iespējama pastiprināta sistēmiskā iedarbība, nevar izslēgt paaugstinātu paaugstinātas jutības risku šajā pacientu grupā. Pacienti arī jāapmāca, kā ziņot, ja acs iekšējais iekaisums pasliktinās, jo tas varētu būt klīnisks simptoms, kas saistīts ar intraokulāro antivielu veidošanās.
Vienlaicīga lietošana ar citiem anti-VEGF (asinsvadu endotēlija augšanas faktors)
Lucentis nedrīkst ievadīt vienlaikus ar citām zālēm pret VEGF (sistēmiskas vai acu).
Lucentis lietošanas pārtraukšana
Devu nedrīkst ievadīt un ārstēšanu nedrīkst atsākt pirms nākamās plānotās ārstēšanas šādos gadījumos:
• labāk koriģētā redzes asuma (BCVA) samazināšanās ≥30 burti, salīdzinot ar pēdējo novērtējumu;
• acs iekšējais spiediens ≥30 mmHg;
• tīklenes pārtraukums;
• "subretināla asiņošana, kas stiepjas līdz fovea centram, vai ja asiņošana ir ≥ 50% no kopējās bojājuma zonas";
• intraokulārā operācija, kas veikta vai plānota iepriekšējo vai nākamo 28 dienu laikā.
Tīklenes pigmenta epitēlija plīsums
Riska faktori, kas saistīti ar tīklenes pigmenta epitēlija plīsuma rašanos pēc anti-VEGF terapijas mitrai AMD, ietver lielu un / vai augstu tīklenes pigmenta epitēlija atslāņošanos. Uzsākot terapiju ar Lucentis, jāievēro piesardzība pacientiem ar šiem tīklenes pigmenta epitēlija plīsuma riska faktoriem.
Regmatogēna tīklenes atslāņošanās vai makulas caurumi
Ārstēšana jāpārtrauc cilvēkiem ar tīklenes regmatogēnu atslāņošanos vai 3. vai 4. stadijas makulas caurumiem.
Populācijas ar ierobežotiem datiem
Pieredze par to, kā ārstēt pacientus ar I tipa cukura diabētu izraisītu sekundāro DME, ir tikai ierobežota. Lucentis nav pētīts pacientiem, kuri iepriekš saņēmuši intravitreālas injekcijas, pacientiem ar aktīvām sistēmiskām infekcijām, proliferējošu diabētisko retinopātiju vai pacientiem ar vienlaicīgiem veselības traucējumiem. piemēram, tīklenes atslāņošanās vai makulas caurums Nav arī pieredzes par ārstēšanu ar Lucentis pacientiem ar cukura diabētu, kuriem HbAlc ir lielāks par 12% un kuriem ir nekontrolēta hipertensija. Ārstējot šos pacientus, ārstam jāņem vērā informācijas trūkums.
Par PM pacientiem ir ierobežoti dati par Lucentis iedarbību pacientiem, kuri iepriekš tika ārstēti ar neveiksmīgu fotodinamisko terapiju ar verteporfīnu (vPDT). Turklāt, lai gan konsekventa iedarbība tika novērota pacientiem ar subfoveālu un jukstafoveālu bojājumu, nav pietiekami daudz datu par ietekmi Lucentis PM pacientiem ar ekstrafoveāliem bojājumiem.
Sistēmiskā iedarbība pēc intravitreālas ievadīšanas
Pēc VEGF inhibitoru intravitreālas injekcijas ziņots par sistēmiskām nevēlamām blakusparādībām, tostarp asiņošanu, kas nav okulāri, un artēriju trombemboliju.
Ir ierobežoti dati par DME, makulas tūskas, ko izraisa RVO un CNV izraisītu sekundāro PM ārstēšanu, drošumu pacientiem, kuriem anamnēzē ir insults vai pārejoši išēmiski lēkmes. Īpaša piesardzība jāievēro, ārstējot šādus pacientus (skatīt 4.8. Apakšpunktu).
Iepriekšējās RVO, išēmiskās filiāles un centrālās RVO epizodes
Pieredze ārstēšanā pacientiem ar iepriekšējām RVO epizodēm un pacientiem ar išēmisku atzarojumu RVO (BRVO) un centrālo RVO (CRVO). Pacientiem ar RVO, kuriem ir redzes funkcijas zudums un neatgriezeniskas išēmijas klīniskās pazīmes, ārstēšana ir nav ieteicams.
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi
Parastie mijiedarbības pētījumi nav veikti.
Kombinētu fotodinamiskās terapijas (PDT) lietošanu ar verteporfīnu un Lucentis mitrā AMD un PM, skatīt apakšpunktu 5.1.
Par lāzera fotokoagulācijas un Lucentis kombinēto lietošanu DME un BRVO ārstēšanā skatīt 4.2. Un 5.1.
04.6 Grūtniecība un zīdīšana
Sievietes reproduktīvā vecumā / kontracepcija sievietēm
Sievietēm reproduktīvā vecumā ārstēšanas laikā jāizmanto efektīva kontracepcijas metode.
Grūtniecība
Nav pieejami klīniskie dati par ranibizumaba lietošanu grūtniecības laikā. Pētījumi ar cynomolgus pērtiķiem neuzrādīja tiešu vai netiešu kaitīgu ietekmi uz grūtniecību vai embrija / augļa attīstību (skatīt apakšpunktu 5.3). Pēc acu ievadīšanas sistēmiskā ranibizumaba iedarbība ir zema, taču darbības mehānisma dēļ ranibizumabs jāuzskata par potenciāli teratogēnu un embriju / augļa toksisku. Tādēļ ranibizumabu nedrīkst lietot grūtniecības laikā, ja vien paredzamais ieguvums neatsver iespējamo risku auglim. Sievietēm, kuras plāno grūtniecību un ir ārstētas ar ranibizumabu, pirms bērna ieņemšanas ieteicams nogaidīt vismaz 3 mēnešus pēc pēdējās ranibizumaba devas.
Grūtniecība
Nav zināms, vai Lucentis izdalās mātes pienā. Lucentis lietošanas laikā nav ieteicams barot bērnu ar krūti.
Auglība
Nav pieejami dati par auglību.
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus
Ārstēšanas procedūra Lucentis var izraisīt pārejošus redzes traucējumus, kas var ietekmēt spēju vadīt transportlīdzekļus vai apkalpot mehānismus (skatīt 4.8. Apakšpunktu). Pacientiem, kuriem rodas šie simptomi, nevajadzētu vadīt transportlīdzekļus un apkalpot mehānismus, kamēr šie pārejošie redzes traucējumi nav novērsti.
04.8 Nevēlamās blakusparādības
Drošības profila kopsavilkums
Lielākā daļa blakusparādību, par kurām ziņots pēc Lucentis ievadīšanas, ir saistītas ar intravitreālu injekcijas procedūru.
Visbiežāk novērotās blakusparādības acīs pēc Lucentis injekcijas ir: sāpes acīs, acs hiperēmija, paaugstināts acs iekšējais spiediens, vitreīts, stiklveida ķermeņa atslāņošanās, tīklenes asiņošana, redzes traucējumi, pludiņi (stiklveida peldētāji), konjunktīvas asiņošana, kairinājums acīs, svešķermeņa sajūta acs, pastiprināta asarošana, blefarīts, sausa acs un niezoša acs.
Visbiežāk novērotās ne acu blakusparādības ir galvassāpes, nazofaringīts un artralģija.
Retāk ziņotās, bet nopietnākās blakusparādības ir endoftalmīts, aklums, tīklenes atslāņošanās, tīklenes plīsums un jatrogēna traumatiska katarakta (skatīt apakšpunktu 4.4).
Pacienti jāinformē par šo iespējamo nevēlamo blakusparādību simptomiem un jāiesaka informēt ārstu, ja viņiem rodas tādas pazīmes kā sāpes acīs vai paaugstināts diskomforts, acu apsārtuma pasliktināšanās, neskaidra vai pasliktināta redze, palielināts stiklveida peldētāju skaits vai paaugstināta jutība pret gaismu.
Blakusparādības, par kurām ziņots pēc Lucentis lietošanas klīniskajos pētījumos, ir apkopotas tabulā zemāk.
Blakusparādību tabula #
Nevēlamās blakusparādības ir uzskaitītas pēc orgānu sistēmas klasēm un biežuma, izmantojot šādu vienošanos: ļoti bieži (≥1 / 10), bieži (≥1 / 100,
Infekcijas un invāzijas
Ļoti bieži sastopams Nazofaringīts
bieži Urīnceļu infekcijas *
Asins un limfātiskās sistēmas traucējumi
bieži Anēmija
Imūnsistēmas traucējumi
bieži Paaugstināta jutība
Psihiskie traucējumi
bieži Trauksme
Nervu sistēmas traucējumi
Ļoti bieži sastopams Galvassāpes
Acu slimības
Ļoti bieži sastopams Vitreīts, stiklveida ķermeņa atslāņošanās, asiņošana tīklenē, redzes traucējumi, sāpes acīs, stiklveida pludiņi, konjunktīvas asiņošana, acu kairinājums, svešķermeņa sajūta acī, pastiprināta asarošana, blefarīts, sausa acs, acs hiperēmija, acs nieze.
bieži Tīklenes deģenerācija, tīklenes traucējumi, tīklenes atslāņošanās, tīklenes plīsums, tīklenes pigmenta epitēlija atdalīšanās, tīklenes pigmenta epitēlija plīsums, samazināts redzes asums, stiklveida asiņošana, stiklveida traucējumi, uveīts, irīts, iridociklīts, katarakta, subkapsulārā katarakta aizmugurējā kapsula keratīts, radzenes nobrāzums, priekšējās kameras reakcija, neskaidra redze, asiņošana injekcijas vietā, asiņošana acīs, konjunktivīts, konjunktivīts
alerģija, izdalījumi no acīm, gaismas zibspuldzes, fotofobija, diskomforts acīs, plakstiņu tūska, plakstiņu sāpes, konjunktīvas hiperēmija.
Retāk Aklums, endoftalmīts, hipopions, hiphema, keratopātija, varavīksnenes sinhijas, radzenes nogulsnes, radzenes tūska, radzenes strijas, sāpes injekcijas vietā, kairinājums injekcijas vietā, patoloģiskas sajūtas acī, plakstiņu kairinājums.
Elpošanas, krūšu kurvja un videnes slimības
bieži Klepus
Kuņģa -zarnu trakta traucējumi
bieži Slikta dūša
Ādas un zemādas audu bojājumi
bieži Alerģiskas reakcijas (izsitumi, nātrene, nieze, eritēma)
Skeleta -muskuļu un saistaudu sistēmas bojājumi
Ļoti bieži sastopams Artralģija
Diagnostikas testi
Ļoti bieži sastopams Paaugstināts acs iekšējais spiediens
# Blakusparādības tika definētas kā blakusparādības (vismaz 0,5 procentpunktos pacientu), kas biežāk (vismaz 2 procentpunkti) radās pacientiem, kuri saņēma 0,5 mg Lucentis, salīdzinot ar tiem, kuri saņēma kontroles terapiju (viltus vai PDT) verteporfīns).
* novērots tikai populācijā ar DME
Blakusparādības, kas saistītas ar narkotiku kategoriju
III fāzes mitrā AMD pētījumos ar ranibizumabu ārstētiem pacientiem nedaudz palielinājās ne-acu asiņošanas biežums, kas bija nevēlama parādība, kas varētu būt saistīta ar VEGF inhibitoriem (endotēlija asinsvadu augšanas faktors). modelis starp dažādiem asinsizplūdumiem. VEGF inhibitoru intravitreālas lietošanas dēļ pastāv teorētisks arteriālās trombembolijas, tai skaitā insulta un miokarda infarkta, risks. Klīniskajos Lucentis pētījumos pacientiem ar AMD, DME, RVO un PM tika novērots neliels arteriālās trombembolijas gadījumu skaits, un atšķirības starp ranibizumaba grupām netika novērotas, salīdzinot ar kontroli.
Ziņošana par iespējamām blakusparādībām
Ir svarīgi ziņot par iespējamām blakusparādībām, kas rodas pēc zāļu reģistrācijas, jo tas ļauj nepārtraukti uzraudzīt zāļu ieguvuma un riska attiecību. Veselības aprūpes speciālistus lūdz ziņot par jebkādām iespējamām blakusparādībām, izmantojot Itālijas Zāļu aģentūru. , vietne: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Pārdozēšana
Klīniskajos pētījumos ar slapju AMD un pēcreģistrācijas datiem ziņots par nejaušas pārdozēšanas gadījumiem. Visbiežāk ar šiem gadījumiem saistītās blakusparādības bija paaugstināts acs iekšējais spiediens, pārejošs aklums, redzes asuma samazināšanās, radzenes tūska un sāpes. Ja notiek pārdozēšana, acs iekšējais spiediens jākontrolē un jāārstē pēc ārsta ieskatiem.
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS
05.1 Farmakodinamiskās īpašības
Farmakoterapeitiskā grupa: oftalmoloģiskie līdzekļi, pretneovaskulāri līdzekļi, ATĶ kods: S01LA04
Ranibizumabs ir humanizēts rekombinants monoklonāls antivielu fragments, kas vērsts pret cilvēka asinsvadu endotēlija augšanas faktoru A (VEGF-A). Tas ar lielu afinitāti saistās ar VEGF-A izoformām (piemēram, VEGF110, VEGF121 un VEGF165), tādējādi novēršot VEGF-A saistīšanos ar saviem VEGFR-1 un VEGFR-2 receptoriem. Pie tā receptoriem izraisa endotēlija šūnu proliferāciju neovaskularizācija un asinsvadu caurlaidības palielināšanās, kas, domājams, veicina ar vecumu saistītas makulas deģenerācijas, patoloģiskas tuvredzības vai redzes pasliktināšanās neovaskulārās formas progresēšanu, ko izraisa vai nu diabētiskā makulas tūska, vai "makulas tūska, kas ir sekundāra RVO.
Mitrās AMD ārstēšana
Mitrās AMD gadījumā Lucentis drošība un klīniskā efektivitāte tika novērtēta trīs 24 mēnešus garos randomizētos, dubultmaskētos, viltus vai aktīvi kontrolētos pētījumos pacientiem ar neovaskulāru AMD. Šajos pētījumos tika iekļauti 1323 pacienti (879 ārstēti un 444 kontroles).
Pētījumā FVF2598g (MARINA) 716 pacienti ar minimāli klasisku vai slēptu koroīdu neovaskularizācijas (CNV) bojājumu bez klasiskās sastāvdaļas saņēma ikmēneša intravitreālas 0,3 mg (n = 238) vai 0,5 mg (n = 240) injekcijas vai fiktīvas injekcijas (n = 238).
Pētījumā FVF2587g (ANCHOR) 423 pacienti ar pārsvarā klasisku CNV saņēma vienu no šādām ārstēšanas metodēm: 1) ikmēneša intravitreālas 0,3 mg Lucentis un PDT fiktīvas injekcijas (n = 140); 2) ikmēneša intravitreālas Lucentis 0,5 mg un PDT fiktīvas injekcijas (n = 140); vai 3) intravitreālas fiktīvas injekcijas un PDT ar verteporfīnu (n = 143). PDT ar verteporfīnu vai fiktīvu ievadīja kopā ar sākotnējo Lucentis injekciju un pēc tam ik pēc 3 mēnešiem, ja fluorangiogrāfija parādīja noturību vai asinsvadu noplūdes atjaunošanos.
Galvenie secinājumi ir apkopoti 1., 2. tabulā un 1. attēlā.
1. tabula Rezultāti 12. un 24. mēnesī pētījumā FVF2598g (MARINA)
ap
2. tabula Rezultāti 12. un 24. mēnesī pētījumā FVF2587g (ANCHOR)
Tabula
Abu pētījumu rezultāti parādīja, ka ilgstoša ārstēšana ar ranibizumabu varētu būt noderīga arī pacientiem, kuri pirmajā ārstēšanas gadā zaudēja ≥15 burtus ar vislabāk koriģēto redzes asumu (BCVA).
Pētījums FVF3192g (PIER) bija randomizēts, dubultmaskēts, fiktīvi kontrolēts pētījums, kura mērķis bija novērtēt Lucentis drošību un efektivitāti 184 pacientiem ar visu veidu neovaskulāru AMD. Pacienti saņēma intravitreālas 0,3 mg (n = 60) Lucentis injekcijas vai 0,5 mg (n = 61) vai fiktīvas injekcijas (n = 63) vienu reizi mēnesī 3 devās pēc kārtas, kam seko viena deva reizi 3 mēnešos. No 14. pētījuma mēneša pacienti, kuri tika ārstēti ar fiktīvu injekciju, tika uzņemti terapiju ar ranibizumabu un no 19. mēneša ārstēšanu varētu veikt biežāk. Pacienti, kuri tika ārstēti ar Lucentis PIER pētījumā, kopumā saņēma vidēji 10 procedūras.
Primārais efektivitātes mērķa kritērijs bija vidējās redzes asuma izmaiņas pēc 12 mēnešiem, salīdzinot ar sākotnējo. Pēc sākotnējā redzes asuma palielināšanās (pēc ikmēneša devas) pacienti, lietojot ceturkšņa devu, vidēji samazināja redzes asumu, 12. mēnesī atgriežoties sākotnējā stāvoklī, un šī ietekme saglabājās lielākajā daļā ārstēto pacientu. 24. mēnesis. Dati par ierobežotu skaitu pacientu, kuri tika pārcelti uz ārstēšanu ar ranibizumabu pēc vairāk nekā viena gada fiktīvas ārstēšanas, liecināja, ka agrīna ārstēšanas uzsākšana var būt saistīta ar labāku redzes asuma saglabāšanu.
Gan MARINA, gan ANCHOR pētījumos redzes asuma uzlabošanos, kas novērota, lietojot Lucentis 0, 5 mg 12 mēnešus, papildināja pacienta ziņotais ieguvums, ko mēra pēc Nacionālā acu institūta vizuālās funkcijas anketas (VFQ-25) rādītāja. Atšķirības starp Lucentis 0, 5 mg un abas kontroles grupas tika novērtētas ar p vērtībām robežās no 0,009 līdz
Lucentis efektivitāte mitras AMD ārstēšanā tika apstiprināta AMD pēcreģistrācijas pētījumos. Divi pētījumi (MONT BLANC, BPD952A2308 un DENALI, BPD952A2309) neuzrādīja verteporfīna (Visudyne PDT) kombinētās lietošanas papildu ietekmi un Lucentis, salīdzinot ar Lucentis vien.
Redzes traucējumu ārstēšana DME dēļ
Lucentis drošums un efektivitāte tika novērtēta divos randomizētos, dubultmaskētos, viltus kontrolētos vai aktīvos 12 mēnešu pētījumos ar pacientiem ar redzes pasliktināšanos diabētiskās makulas tūskas dēļ. Kopumā tika iekļauti šie pētījumi. No 496 pacientiem (336 aktīvi un 160 kontroles), lielākajai daļai bija II tipa diabēts, 28 ārstētiem pacientiem bija I tipa diabēts.
Pētījuma D2201 (RESOLVE) II fāzē 151 pacients tika ārstēts ar ranibizumabu (6 mg / ml, n = 51, 10 mg / ml, n = 51) vai fiktīvu (n = 49) ar vienu "intravitreālu injekciju mēnesī. līdz tiek sasniegti iepriekš definētie kritēriji.Ranibizumaba sākuma devu (0,3 mg vai 0,5 mg) jebkurā pētījuma laikā pēc pirmās injekcijas var dubultot. Lāzera fotokoagulācija bija atļauta kā glābšanas terapija no 3. mēneša abās ārstēšanas grupās. Pētījumam bija divas daļas: izpētes daļa (pirmie 42 pacienti apmeklēja 6. mēnesī) un apstiprinošā daļa (atlikušie 109 pacienti apmeklēja 12. mēnesī).
Galvenie secinājumi no apstiprinošās pētījuma daļas (2/3 pacientu) ir apkopoti 3. tabulā.
3. tabula. Rezultāti 12. mēnesī pētījumā D2201 (RESOLVE) (kopējā pētījuma populācija)
ap
III fāzes pētījumā D2301 (RESTORE) 345 pacienti ar redzes traucējumiem makulas tūskas dēļ tika randomizēti, lai saņemtu vai nu "intravitreālu 0,5 mg ranibizumaba injekciju monoterapijā un lāzera fiktīvu fotokoagulāciju (n = 116), vai kombināciju ar 0,5 mg ranibizumabu un lāzera fotokoagulāciju (n = 118) vai "fiktīvu injekciju un lāzera fotokoagulāciju" (n = 111). Ārstēšana ar ranibizumabu tika uzsākta ar ikmēneša intravitreālām injekcijām un turpināta, līdz redzes asums saglabājās stabils vismaz trīs secīgas ikmēneša pārbaudes. Ārstēšana tika atsākta, kad tika novērots BCVA samazinājums DME progresēšanas dēļ. Lāzera fotokoagulācija tika ievadīta sākotnēji tajā pašā dienā, vismaz 30 minūtes pirms ranibizumaba injekcijas un pēc tam, ja nepieciešams, pamatojoties uz ETDRS kritērijiem.
Galvenie secinājumi ir apkopoti 4. tabulā un 2. attēlā.
4. tabula. Rezultāti 12. mēnesī pētījumā D2301 (ATJAUNOT)
ap
Ietekme bija konsekventa lielākajā daļā apakšgrupu. Tomēr pacientiem ar sākotnēji diezgan augstu BCVA (> 73 burti) ar makulas tūsku un centrālo tīklenes biezumu
Redzes asuma uzlabošanos 12. mēnesī, ko novēroja, lietojot Lucentis 0,5 mg, pievienoja pacienta ziņotie ieguvumi no galvenajām ar redzi saistītajām funkcijām, ko mēra pēc Nacionālā acu institūta redzes funkciju anketas (VFQ-25) vērtējuma. Ārstēšanas dēļ atšķirības nevar būt Atšķirība starp Lucentis 0,5 mg un kontroles grupu tika novērtēta ar p-vērtību 0,0137 (ranibizumaba mono) un 0,0041 (ranibizumabs + lāzers) attiecībā uz VFQ-25 salikto punktu skaitu.
Abos pētījumos redzes uzlabošanos papildināja nepārtraukta makulas tūskas samazināšanās, ko mēra kā tīklenes centrālo biezumu (CRT).
Redzes traucējumu ārstēšana, ko izraisa RVO izraisīta makulas tūska
Lucentis klīniskā drošība un efektivitāte pacientiem ar redzes traucējumiem RVO izraisītas makulas tūskas dēļ tika novērtēta randomizētos, dubultmaskētos, kontrolētos pētījumos: BRAVO un CRUISE, kuros tika pieņemti pacienti ar BRVO (n = 397) un CRVO (n = 392). Abos pētījumos pacienti saņēma vai nu 0,3 mg, vai 0,5 mg ranibizumaba intravitreālas vai fiktīvas injekcijas. Pēc 6 mēnešiem pacienti viltus kontroles grupā tika pārvietoti uz 0,5 mg ranibizumaba grupu. BRAVO pētījumā lāzera fotokoagulācija kā glābšanas līdzeklis bija atļauts visās rokās no 3. mēneša.
Galvenie BRAVO un CRUISE pētījumu rezultāti ir parādīti 5. un 6. tabulā
5. tabula. Rezultāti 6. un 12. mēnesī (BRAVO)
ap
6. tabula. Rezultāti 6. un 12. mēnesī (CRUISE)
ap
Abos pētījumos redzes uzlabošanos papildināja nepārtraukts un ievērojams makulas tūskas samazinājums, ko mēra pēc tīklenes centrālā biezuma.
BRVO pacientiem (BRAVO pētījums un HORIZON pētījuma pagarinājums): Pēc 2 gadiem pacientiem, kuri pirmajos 6 mēnešos tika ārstēti ar fiktīvām injekcijām un pēc tam pārgāja uz ārstēšanu ar ranibizumabu, AV palielinājās (& simp; 15 burti), kas ir salīdzināms ar to pacientu, kuri kopš pētījuma uzsākšanas tika ārstēti ar ranibizumabu (& simp; 16 burti). Tomēr 2 gadus veco pacientu skaits bija ierobežots, un HORIZON pētījumā bija ieplānoti tikai ceturkšņa apmeklējumi. ir pietiekami daudz pierādījumu, lai noslēgtu ieteikumus par kad pacientiem ar BRVO jāsāk ārstēšana ar ranibizumabu.
Pacientiem ar CRVO (CRUISE pētījums un HORIZON pētījuma pagarinājums): Pēc 2 gadiem pacientiem, kuri pirmajos 6 mēnešos tika ārstēti ar fiktīvām injekcijām un pēc tam tika pārcelti uz ārstēšanu ar ranibizumabu, nebija vērojama AV palielināšanās (& simp; 6 burti) pacientu, kuri kopš pētījuma uzsākšanas tika ārstēti ar ranibizumabu (& simp; 12 burti).
Redzes asuma uzlabošanos, kas tika novērota, ārstējot ranibizumabu 6. un 12. mēnesī, papildināja pacienta ziņotais ieguvums, ko mēra Nacionālā acu institūta vizuālās funkcijas anketas (NEI VFQ-25) tuvu un tālu darbību apakšgrupā Atšķirība starp Lucentis 0,5 mg un tika konstatēts, ka kontroles grupa atrodas starp p vērtībām starp 0,02 un 0,0002.
Redzes traucējumu ārstēšana CNV dēļ, kas ir sekundāra PM
Lucentis drošība un klīniskā efektivitāte pacientiem ar redzes traucējumiem CNV dēļ PM tika apstiprināta, pamatojoties uz 12 mēnešu datiem no galvenā randomizētā, dubultmaskētā, kontrolētā pētījuma F2301 (RADIANCE). Šī pētījuma mērķis bija novērtēt divas dažādas dozēšanas shēmas 0,5 mg ranibizumaba ievadīšana intravitreālā injekcijā, salīdzinot ar verteporfīna PDT (vPDT, Visudyne fotodinamiskā terapija). 277 pacienti tika randomizēti vienā no šādām grupām:
• I grupa (0,5 mg ranibizumaba, ārstēšanas režīms noteikts pēc "stabilitātes" kritērijiem, kas definēti kā nemainīgas BCVA salīdzinājumā ar iepriekšējo divu mēnešu novērtējumiem).
• II grupa (0,5 mg ranibizumaba, ārstēšanas režīmu nosaka pēc "slimības aktivitātes" kritērijiem, kas definēti kā redzes traucējumi, kas saistīti ar intra- vai subretinālo šķidrumu vai aktīvu noplūdi, ko izraisa CNV bojājumi, par ko liecina AZT un / vai AF).
• III grupa (pacienti, kas ārstēti ar vPDT - ar iespēju ārstēties ar ranibizumabu, sākot no 3. mēneša).
Pētījuma 12 mēnešu laikā pacienti saņēma vidēji 4,6 injekcijas (diapazons 1-11) I grupā un 3,5 injekcijas (diapazons 1-12) II grupā. Starp II grupas pacientiem, kas atspoguļo ieteicamo devu (skatīt 4.2. Apakšpunktu), 50,9% pacientu tika ārstēti ar 1 līdz 2 injekcijām, 34,5% no 3 līdz 5 injekcijām un 14,7% veica 6 līdz 12 injekcijas 12 mēnešu pētījuma laikā . 62,9% II grupas pacientu pētījuma otro 6 mēnešu laikā nebija nepieciešamas injekcijas.
RADIANCE galvenie secinājumi ir apkopoti 7. tabulā un 5. attēlā.
7. tabula. Rezultāti 3. un 12. mēnesī (RADIANCE)
ap
b Salīdzinošā kontrole līdz 3. mēnesim. Pacienti, kuri tika randomizēti vPDT saņemšanai, bija tiesīgi saņemt ārstēšanu ar ranibizumabu 3. mēnesī (III grupā 38 pacienti saņēma ranibizumabu 3. mēnesī)
Redzes uzlabošanos papildināja tīklenes centrālā biezuma samazināšanās.
Salīdzinot ar vPDT ārstēto grupu, pacienti ar ranibizumabu ārstēto grupu ziņoja par ieguvumu (p vērtība
Pediatriskā populācija
Ranibizumaba drošība un efektivitāte bērniem vēl nav pierādīta.
Eiropas Zāļu aģentūra ir atteikusies no pienākuma iesniegt pētījumu rezultātus ar Lucentis visās pediatriskās populācijas apakšgrupās attiecībā uz neovaskulāru AMD, redzes traucējumiem DME dēļ, redzes traucējumiem sekundāras makulas tūskas dēļ līdz RVO un redzes traucējumiem, ko izraisa sekundāra CNV PM (informāciju par lietošanu bērniem skatīt 4.2. Apakšpunktā).
05.2 Farmakokinētiskās īpašības
Pēc Lucentis ikmēneša intravitreālas ievadīšanas pacientiem ar neovaskulāru AMD, ranibizumaba koncentrācija serumā parasti bija zema, un maksimālā koncentrācija (C , novērtēts testā in vitro šūnu proliferācija). Cmax bija proporcionāls devai visā devu diapazonā no 0,05 līdz 1,0 mg / acī. Ierobežotam skaitam pacientu ar DME konstatētā koncentrācija serumā liecina, ka nevar izslēgt nedaudz lielāku sistēmisko iedarbību nekā tiem, kas novēroti pacientiem ar neovaskulāru AMD. Ranibizumaba koncentrācija serumā pacientiem ar RVO bija līdzīga vai nedaudz augstāka nekā pacientiem ar neovaskulāru AMD.
Pamatojoties uz populācijas farmakokinētikas analīzi un ranibizumaba klīrensu serumā neovaskulāras AMD slimniekiem, kuri tika ārstēti ar 0,5 mg devu, ranibizumaba vidējais eliminācijas pusperiods ir aptuveni 9 dienas. Laikā, kad katru mēnesi intravitreāli ievadīja 0,5 mg Lucentis uz aci, ranibizumaba C serums, kas sasniegts aptuveni 1 dienu pēc devas, parasti ir robežās no 0,79 līdz 2,90 ng / ml, bet paredzams, ka Cmin parasti svārstās starp 0,07 un 0,49 ng / ml. Tiek lēsts, ka ranibizumaba koncentrācija serumā ir aptuveni 90 000 reizes zemāka nekā stiklveida.
Pacienti ar nieru mazspēju: Nav veikti tradicionāli pētījumi, lai pārbaudītu Lucentis farmakokinētiku pacientiem ar nieru mazspēju. "Farmakokinētikas analīzē neovaskulāras AMD pacientu populācijā 68% (136 no 200) pacientu bija" nieru mazspēja (46,5% viegla [50-80 ml / min], 20% vidēji [30-50 ml / min] un 15% smagi [sistēmiskais klīrenss bija nedaudz zemāks, bet tas nebija klīniski nozīmīgs.
Pacienti ar aknu mazspēju: Nav veikti tradicionāli pētījumi, lai pārbaudītu Lucentis farmakokinētiku pacientiem ar aknu mazspēju.
05.3 Preklīniskie drošības dati
Ranibizumaba divpusēja intravitreāla ievadīšana cynomolgus pērtiķiem devās no 0,25 mg līdz 2,0 mg / acī reizi 2 nedēļās līdz 26 nedēļām izraisīja no devas atkarīgu acu efektu.
Intraokulāri priekšējā kamerā novēroja devas atkarīgu uzliesmojumu un šūnu skaita palielināšanos, sasniedzot maksimumu 2 dienas pēc injekcijas. Iekaisuma reakcijas smagums parasti samazinās ar turpmākajām injekcijām vai atveseļošanās periodā. Aizmugurējā segmentā radās šūnu infiltrācijas un stiklveida peldētāji, kas arī bija atkarīgi no devas un parasti saglabājās līdz ārstēšanas perioda beigām. 26 nedēļu pētījumā stiklveida ķermeņa iekaisuma smagums palielinājās līdz ar injekciju skaitu. Tomēr pēc atveseļošanās perioda tika novērota atgriezeniskums. Aizmugurējā segmenta iekaisuma raksturs un ilgums liecina par imūnsistēmas izraisītu antivielu reakciju, kas var būt klīniski nenozīmīga. Dažiem dzīvniekiem pēc salīdzinoši ilga intensīva iekaisuma perioda novērota kataraktas veidošanās, kas liecina, ka lēcas izmaiņas bija sekundāras līdz smagam iekaisumam. Pēc ievadīšanas, neatkarīgi no devas, pēc intravitreālas injekcijas tika novērots pārejošs acs iekšējā spiediena pieaugums.
Acu mikroskopiskās izmaiņas bija saistītas ar iekaisumu un nenorādīja uz deģeneratīviem procesiem. Dažu acu redzes diskā tika konstatētas iekaisuma granulomatozas izmaiņas. Šīs aizmugurējās segmenta izmaiņas samazinājās un dažos gadījumos izzuda atveseļošanās periodā.
Pēc intravitreālas ievadīšanas nebija sistēmiskas toksicitātes pazīmju. Seruma un stiklveida antivielas pret ranibizumabu tika atrastas ārstēto dzīvnieku apakšgrupā.
Dati par kancerogenitāti vai mutagēnitāti nav pieejami.
Grūtniecēm pērtiķiem intranitreāla ranibizumaba injekcija, kuras maksimālā sistēmiskā iedarbība 0,9-7 reizes pārsniedza sliktāko klīnisko iedarbību, neizraisīja toksisku ietekmi uz attīstību vai teratogenitāti, kā arī neietekmēja ķermeņa svaru vai struktūru. Placenta teratogēns un embrija / augļa toksisks, pamatojoties uz tā farmakoloģisko iedarbību.
Ranibizumaba mediētās ietekmes trūkums uz embrija / augļa attīstību ir ticami saistīts galvenokārt ar Fab fragmenta nespēju šķērsot placentu. Tomēr tika aprakstīts gadījums ar augstu ranibizumaba līmeni mātes serumā un ranibizumaba klātbūtni augļa serumā, kas liecina, ka anti-ranibizumaba antiviela darbojās kā proteīns (satur FC reģionu), kas transportē ranibizumabu, tādējādi samazinot tā izvadīšanu no mātes seruma un ļaujot to pārnest uz placentu. Tā kā embriju / augļa attīstības testi ir veikti veseliem grūsniem dzīvniekiem un dažas slimības (piemēram, diabēts) var mainīt placentas caurlaidību līdz Fab fragmentam, pētījums jāinterpretē piesardzīgi.
06.0 FARMACEITISKĀ INFORMĀCIJA
06.1 Palīgvielas
α, α-trehalozes dihidrāts
Histidīna hidrohlorīds, monohidrāts
Histidīns
Polisorbāts 20
Ūdens injekcijām
06.2 Nesaderība
Saderības pētījumu trūkuma dēļ šīs zāles nedrīkst sajaukt ar citām zālēm.
06.3 Derīguma termiņš
3 gadi
06.4 Īpaši uzglabāšanas nosacījumi
Uzglabāt ledusskapī (2 ° C - 8 ° C).
Nesasaldēt.
Uzglabāt flakonu ārējā iepakojumā, lai pasargātu zāles no gaismas.
06.5 Tiešā iepakojuma veids un iepakojuma saturs
0,23 ml sterila šķīduma flakonā (I tipa stikls) ar aizbāzni (hlorbutilgumija), 1 neass filtra adata (18G x 1½ ", 1,2 mm x 40 mm, 5 mcm), 1 injekcijas adata (30G x ½", 0,3 mm x 13 mm) un 1 šļirce (polipropilēns) (1 ml). Iepakojumā ir 1 flakons.
06.6 Norādījumi lietošanai un lietošanai
Flakons, injekcijas adata, filtra adata un šļirce ir paredzēti tikai vienreizējai lietošanai. Atkārtota izmantošana var izraisīt infekciju vai citas slimības / ievainojumus. Visi komponenti ir sterili. Nedrīkst izmantot nevienu sastāvdaļu ar iepakojumu, kam ir bojājuma vai manipulācijas pazīmes. Sterilitāti nevar garantēt, ja komponenta iepakojuma blīvējums nav neskarts.
Lai sagatavotu Lucentis intravitreālai injekcijai, lūdzu, izpildiet tālāk sniegtos norādījumus.
1. Pirms savākšanas dezinficējiet flakona gumijas aizbāžņa ārpusi.
2. Aseptiski pievienojiet 5 mcm filtra adatu (18G x 1½ ", 1,2 mm x 40 mm, komplektā) 1 ml šļircei (komplektā). Ievietojiet neasu filtra adatu vāciņa centrā, līdz tā pieskaras flakona apakšai.
3. Izvelciet visu šķidrumu no flakona, turot to vertikālā stāvoklī, nedaudz noliektu, lai atvieglotu pilnīgu izņemšanu.
4. Pārliecinieties, ka, iztukšojot flakonu, šļirces virzulis ir pietiekami atvilkts atpakaļ, lai pilnībā iztukšotu filtra adatu.
5. Atstājiet flakonā neasu filtra adatu un izņemiet no tās šļirci.Pēc flakona satura izņemšanas izmetiet filtra adatu un neizmantojiet to intravitreālai injekcijai.
6. Droši un aseptiski pievienojiet šļircei injekcijas adatu (30G x ½ ", 0,3 mm x 13 mm, komplektā).
7. Uzmanīgi noņemiet injekcijas adatas uzgali, neatvienojot injekcijas adatu no šļirces.
Piezīme: noņemot vāciņu, turiet injekcijas adatas dzelteno pamatni.
8. Uzmanīgi izvadiet gaisu no šļirces un noregulējiet devu līdz 0,05 ml, kas atzīmēta uz šļirces.Šļirce ir gatava injekcijai.
Piezīme: Netīriet injekcijas adatu un nevelciet virzuli atpakaļ.
Pēc injekcijas neaizveriet adatu un neatvienojiet to no šļirces. Izmetiet izlietoto šļirci kopā ar adatu piemērotā traukā vai saskaņā ar vietējām prasībām.
07.0 REĢISTRĀCIJAS APLIECĪBAS ĪPAŠNIEKS
Novartis Europharm Limited
Vimbblerstas ceļš
Horsham
Rietumsaseksa, RH12 5AB
Lielbritānija
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS
EU/1/06/374/001
037608027
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS
Reģistrācijas datums: 2007. gada 22. janvāris
Pēdējās pārreģistrācijas datums: 2012. gada 24. janvāris
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS
05/2014