Aktīvās sastāvdaļas: fentanils
Effentora 100 mikrogramu vaigu tabletes
Effentora 200 mikrogramu vaigu tabletes
Effentora 400 mikrogramu vaigu tabletes
Effentora 600 mikrogramu vaigu tabletes
Effentora 800 mikrogramu vaigu tabletes
Kāpēc lieto Effentora? Kam tas paredzēts?
Effentora aktīvā sastāvdaļa ir fentanila citrāts. Effentora ir pretsāpju līdzeklis, kas pazīstams kā opioīds un ko lieto izrāvienu sāpju ārstēšanai pieaugušiem vēža slimniekiem, kuri jau tiek ārstēti ar citiem opioīdiem pret hroniskām pastāvīgām (24 stundas diennaktī) sāpēm vēža dēļ.
Izrāvienu sāpes ir pēkšņas, papildu sāpes, kas rodas pat pēc parasto opioīdu pretsāpju līdzekļu lietošanas.
Kontrindikācijas Kad Effentora nedrīkst lietot
Nelietojiet Effentora šādos gadījumos:
- Ja neesat lietojis recepšu opioīdu zāles (piemēram, kodeīnu, fentanilu, hidromorfonu, morfīnu, oksikodonu, petidīnu) katru dienu un regulāri vismaz vienu nedēļu, lai kontrolētu pastāvīgas sāpes. Ja nelietojat šīs zāles, nevajadzētu lietot Effentora, jo tas var palielināt risku, ka jūsu elpošana kļūs bīstami lēna un / vai sekla, vai pat aizsprostota.
- Ja Jums ir alerģija pret fentanilu vai kādu citu (6. punktā minēto) šo zāļu sastāvdaļu.
- Ja Jums ir smagas elpošanas problēmas vai smaga obstruktīva plaušu slimība.
- Ja jūs ciešat no īslaicīgām sāpēm, kas nav izrāviena sāpes.
Piesardzība lietošanā Kas jāzina pirms Effentora lietošanas
Pirms Effentora lietošanas konsultējieties ar ārstu vai farmaceitu.
Ārstēšanas laikā ar Effentora turpiniet lietot opioīdu pretsāpju līdzekļus, ko lietojat pastāvīgu (24 stundu) vēža sāpju gadījumā.
Lietojot Effentora, nelietojiet nekādas citas terapijas, kas balstītas uz fentanilu. Ja jums joprojām ir kāda no šīm terapijām mājās, sazinieties ar farmaceitu, lai uzzinātu, kā no tām atbrīvoties.
Pirms ārstēšanas ar Effentora pastāstiet ārstam vai farmaceitam, ja Jums ir kāds no šiem stāvokļiem:
- Vēl nav atrasta galīgā deva citam opioīdam, ko viņa lieto, lai ārstētu pastāvīgās (ilgstošas) sāpes, ko izraisa vēzis.
- Ja Jums ir kāds stāvoklis, kas ietekmē elpošanas funkciju (piemēram, astma, sēkšana, elpas trūkums).
- Ja jums ir galvas trauma.
- Ja Jums ir ārkārtīgi zems sirdsdarbības ātrums vai citas sirds problēmas.
- Ja Jums ir kādi aknu vai nieru darbības traucējumi, jo šie orgāni ietekmē zāļu sadalīšanās veidu.
- Ja Jums ir zems šķidruma daudzums asinsritē vai zems asinsspiediens.
- Ja Jums ir sirds problēmas, īpaši lēna sirdsdarbība.
- Ja lietojat antidepresantus vai antipsihotiskos līdzekļus, lūdzu, skatiet sadaļu Citas zāles un Effentora.
Ko darīt, ja kāds nejauši lieto Effentora
Ja domājat, ka kāds nejauši ir lietojis Effentora, nekavējoties sazinieties ar ārstu.
Centieties noturēt cilvēku nomodā, līdz ieradīsies medicīniskā palīdzība.
Ja nejauši esat lietojis Effentora, Jums var būt tādas pašas blakusparādības, kā aprakstīts 3. sadaļā "Ja esat lietojis Effentora vairāk nekā noteikts".
Bērni un pusaudži
Nedodiet šīs zāles bērniem vecumā no 0 līdz 18 gadiem.
Mijiedarbība Kādas zāles vai pārtikas produkti var mainīt Effentora iedarbību
Pirms Effentora lietošanas pastāstiet ārstam vai farmaceitam par visām zālēm, kuras lietojat, pēdējā laikā esat lietojis vai varētu lietot.
- Jebkuras zāles, kas parasti var izraisīt miegainību (t.i., tai ir nomierinoša iedarbība), piemēram, miegazāles, anksiolītiskie līdzekļi, antihistamīni vai trankvilizatori.
- Jebkuras zāles, kas var ietekmēt jūsu ķermeņa Effentora apstrādi, piemēram, ritonavīrs, nelfinavirs, amprenavirs un fosamprenavirs (zāles, kas palīdz kontrolēt HIV infekciju) vai citi tā sauktie CYP3A4 inhibitori, piemēram, ketokonazols, itrakonazols vai flukonazols (zāles, ko lieto sēnīšu infekcijas), troleandomicīns, klaritromicīns vai eritromicīns (zāles, ko lieto bakteriālu infekciju ārstēšanai), aprepitants (zāles smagas sliktas dūšas ārstēšanai) un diltiazems un verapamils (zāles hipertensijas vai sirds mazspējas ārstēšanai)
- Zāles, ko sauc par monoamīnoksidāzes (MAO) inhibitoriem (lieto smagas depresijas gadījumā), kas lietotas pēdējo divu nedēļu laikā.
- Daži sāpju mazināšanas veidi, ko sauc par daļējiem agonistiem / antagonistiem, piemēram. buprenorfīns, nalbufīns un pentazocīns (zāles sāpju ārstēšanai). Lietojot šīs zāles, Jums var rasties abstinences simptomi (slikta dūša, vemšana, caureja, trauksme, drebuļi, trīce un svīšana).
- Blakusparādību risks palielinās, ja lietojat tādas zāles kā daži antidepresanti vai antipsihotiskie līdzekļi. Effentora var mijiedarboties ar šīm zālēm un var mainīties garīgais stāvoklis (piemēram, uzbudinājums, halucinācijas, koma) un citas sekas, piemēram, ķermeņa temperatūra virs 38 ° C, ātra sirdsdarbība, nestabils asinsspiediens un pārmērīgi refleksi, stīvums. koordinācijas trūkums un / vai kuņģa -zarnu trakta simptomi (piemēram, slikta dūša, vemšana, caureja). Ārsts jums pateiks, vai Effentora ir piemērots Jums.
Pastāstiet ārstam vai farmaceitam par visām zālēm, kuras lietojat, pēdējā laikā esat lietojis vai varētu lietot.
Effentora kopā ar uzturu, dzērienu un alkoholu
- Effentora var lietot pirms vai pēc, bet ne ēšanas laikā. Pirms Effentora lietošanas varat dzert nedaudz ūdens, lai samitrinātu muti, bet lietošanas laikā nevajadzētu ēst vai dzert.
- Lietojot Effentora, nevajadzētu dzert greipfrūtu sulu, jo tas var ietekmēt jūsu ķermeņa apstrādes veidu.
- Lietojot Effentora, nelietojiet alkoholu, jo tas var palielināt bīstamu blakusparādību risku.
Brīdinājumi Ir svarīgi zināt, ka:
Grūtniecība un zīdīšanas periods
Ja esat grūtniece vai barojat bērnu ar krūti, ja domājat, ka Jums varētu būt grūtniecība vai plānojat grūtniecību, pirms šo zāļu lietošanas konsultējieties ar ārstu vai farmaceitu.
Effentora nedrīkst lietot grūtniecības laikā, ja vien neesat to apspriedis ar savu ārstu. Effentora nedrīkst lietot dzemdību laikā, jo fentanils jaundzimušajam var izraisīt elpošanas nomākumu.
Fentanils var nonākt mātes pienā un var izraisīt blakusparādības zīdainim, kas baro bērnu ar krūti. Nelietojiet Effentora, ja barojat bērnu ar krūti. Jūs nedrīkstat sākt zīdīt bērnu vismaz 5 dienas pēc pēdējās Effentora devas lietošanas.
Transportlīdzekļu vadīšana un mehānismu apkalpošana
Jums jāapspriež ar ārstu, vai pēc Effentora lietošanas ir droši vadīt transportlīdzekļus vai apkalpot mehānismus. Nevadiet transportlīdzekli un neapkalpojiet mehānismus, ja: jūtaties miegains vai reibonis; ir neskaidra vai dubultā redze; vai ir grūtības koncentrēties. Pirms vadīt transportlīdzekļus vai apkalpot mehānismus, ir svarīgi zināt, kā jūs reaģējat uz Effentora.
Effentora satur nātriju
Katra Effentora 100 mikrogramu tablete satur 10 mg nātrija. Katra Effentora 200 mikrogramu, Effentora 400 mikrogramu, Effentora 600 mikrogramu un Effentora 800 mikrogramu tablete satur 20 mg nātrija. Tas jāpatur prātā, ja ievērojat diētu ar zemu nātrija saturu, tāpēc jums jālūdz padoms ārstam.
Deva, lietošanas veids un laiks Kā lietot Effentora: Devas
Vienmēr lietojiet šīs zāles tieši tā, kā ārsts Jums stāstījis. Ja rodas šaubas, konsultējieties ar ārstu vai farmaceitu.
Devas un lietošanas biežums
Pirmo reizi lietojot Effentora, ārsts sadarbosies ar jums, lai atrastu optimālo devu, lai mazinātu izrāviena sāpes. Ir ļoti svarīgi lietot Effentora tieši tā, kā ārsts Jums teicis. Sākuma deva ir 100 mikrogrami. Nosakot Jums pareizo devu, ārsts var norādīt lietot vairāk nekā vienu tableti vienā epizodē. Ja pēc 30 minūtēm jūsu izrāvienu sāpju epizode netiek atvieglota, titrēšanas fāzē šajā brīdī izmantojiet vēl tikai 1 Effentora tableti.
Kad ārsts ir noteicis pareizo devu, parasti lietojiet 1 tableti vienā smagu sāpju epizodē. Turpmākajos terapijas kursos jūsu vajadzība pēc pretsāpju terapijas var atšķirties. Var būt nepieciešamas lielākas devas. Ja pēc 30 minūtēm sāpes nerimstas, devas pielāgošanas fāzē lietojiet vēl vienu Effentora tableti.
Sazinieties ar savu ārstu, ja pareizā Effentora deva neatbrīvo sāpes no izrāviena. Ārsts izlems, vai deva jāmaina.
Pirms citas smagu sāpju epizodes ārstēšanas ar Effentora pagaidiet vismaz 4 stundas.
Ja lietojat Effentora vairāk nekā četras reizes dienā, nekavējoties pastāstiet par to savam ārstam, jo viņš var mainīt zāles pret jūsu pastāvīgajām sāpēm. Kad jūsu pastāvīgās sāpes ir pārbaudītas, ārstam, iespējams, būs jāmaina Effentora deva. Lai efektīvāk mazinātu sāpes, pastāstiet ārstam par savām sāpēm un to, kā Effentora darbojas jūsu gadījumā, lai nepieciešamības gadījumā devu varētu mainīt.
Nemainiet Effentora vai citu pretsāpju līdzekļu devu pats. Jebkuras devas izmaiņas jānosaka un jāuzrauga ārstam.
Ja neesat pārliecināts, kāda ir pareizā deva, vai ja jums ir citi jautājumi par šo zāļu lietošanu, lūdzu, sazinieties ar savu ārstu.
Lietošanas veids
Effentora vaigu tabletes ir paredzētas lietošanai mutes dobumā (caur mutes gļotādu). Ievietojot tableti mutē, tā izšķīst un zāles caur mutes gļotādu uzsūcas asinsritē. Lietojot zāles šādā veidā, tās ātri uzsūcas, lai mazinātu izrāviena sāpes.
Zāļu lietošana
- Atveriet blisteri tikai tad, kad esat gatavs lietot tableti. Tablete jāizlieto tūlīt pēc izņemšanas no blistera.
- Atdaliet vienu no vienībām no visa blistera, saplēšot gar perforēto līniju.
- Salieciet ierīci pa norādīto līniju.
- Lai izņemtu tableti, noņemiet foliju blistera aizmugurē. Nemēģiniet izbīdīt tableti caur foliju, jo tas var to sabojāt.
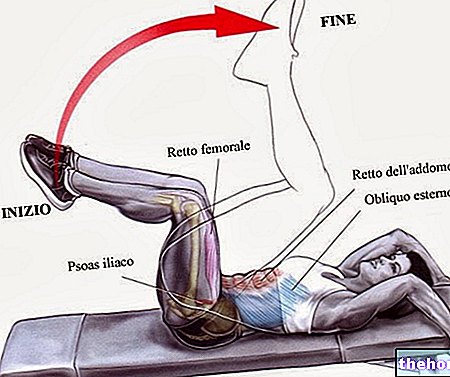
- Izņemiet tableti no ierīces un nekavējoties novietojiet visu tableti blakus molārajam zobam, starp smaganu un vaigu (kā parādīts attēlā). Dažreiz ārsts var ieteikt tableti novietot zem mēles.
- Nemēģiniet sasmalcināt vai salauzt tableti.
- Nekodiet, nesūciet, nesakošļājiet un nerijiet tableti, jo tas mazinās sāpes, nekā tad, ja tableti lieto atbilstoši norādījumiem.
- Tablete jātur starp vaigu un smaganu, līdz tā pilnībā izšķīst, kas prasīs 14 līdz 25 minūtes.
- Kad tablete izšķīst, starp vaigu un smaganu var būt jūtama neliela putojoša sajūta.
- Kairinājuma gadījumā tabletes stāvoklis uz smaganas var mainīties.
- Ja pēc 30 minūtēm mutē vēl ir palikušas tabletes paliekas, tās var norīt, uzdzerot glāzi ūdens.
Ja esat aizmirsis lietot Effentora
Ja sāpju paasinājuma epizode joprojām turpinās, varat lietot Effentora, kā norādījis ārsts.Ja sāpes jau ir beigušās, nelietojiet Effentora līdz nākamajai sāpīgajai epizodei.
Ja pārtraucat lietot Effentora
Jums jāpārtrauc Effentora lietošana, kad vairs neizjūtat izrāvienu sāpes.
Jums jāturpina lietot parastais pretsāpju opioīds, lai ārstētu pastāvīgas vēža sāpes, kā norādījis ārsts. Pārtraucot lietot Effentora, var rasties abstinences simptomi, kas līdzīgi Effentora iespējamām blakusparādībām. Ja Jums rodas abstinences simptomi vai jūs uztrauc sāpju mazināšana, konsultējieties ar ārstu. Viņš apsvērs, vai ir nepieciešamas zāles, lai mazinātu vai likvidētu abstinences simptomus.
Ja jums ir kādi jautājumi par šo zāļu lietošanu, jautājiet savam ārstam vai farmaceitam.
Pārdozēšana Ko darīt, ja esat lietojis pārāk daudz Effentora
Ja esat lietojis Effentora vairāk nekā noteikts
- Visbiežāk novērotās blakusparādības ir miegainība, slikta dūša vai reibonis. Ja pirms tabletes pilnīgas izšķīšanas sākat justies īpaši miegains vai miegains, izskalojiet muti ar ūdeni un atlikušo tableti pilnībā izmetiet izlietnē vai tualetē.
- Nopietna Effentora blakusparādība ir lēna un / vai sekla elpošana. Tas var notikt, ja lietotā Effentora deva ir pārāk liela vai ja esat lietojis pārāk daudz zāļu. Šādos gadījumos ir nepieciešams nekavējoties konsultēties ar ārstu.
Blakusparādības Kādas ir Effentora blakusparādības
Tāpat kā citas zāles, šīs zāles var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas. Ja pamanāt kādu no šīm blakusparādībām, lūdzu, sazinieties ar savu ārstu.
Visnopietnākās blakusparādības ir sekla elpošana, zems asinsspiediens un šoks. Tāpat kā citi fentanila produkti, Effentora var izraisīt ļoti nopietnas elpošanas problēmas, kas var izraisīt nāvi.
Ja jūtat ievērojamu miegainību un lēnu un / vai virspusēju elpošanu, jums vai aprūpētājiem nekavējoties jāsazinās ar savu ārstu un jāmeklē steidzama palīdzība.
Ļoti bieži sastopamas blakusparādības (var skart vairāk nekā 1 no 10 cilvēkiem):
- papēža sajūta, galvassāpes
- slikta dūša, vemšana
- tabletes lietošanas vietā: sāpes, čūlas, kairinājums, asiņošana, nejutīgums, jutīguma zudums, apsārtums, pietūkums vai pūslīši.
Biežas blakusparādības (var skart līdz 1 no 10 cilvēkiem):
- trauksme vai apjukums, depresija, bezmiegs
- mainīta garšas sajūta, svara zudums
- miegainība, sedācija, pārmērīgs nogurums, vājums, migrēna, nejutīgums, roku vai kāju pietūkums, zāļu abstinences sindroms (var rasties ar šādām blakusparādībām: slikta dūša, vemšana, caureja, trauksme, drebuļi, trīce un svīšana), kritieni, drebuļi
- aizcietējums, stomatīts, sausa mute, caureja, grēmas, apetītes zudums, sāpes vēderā, diskomforts kuņģī, gremošanas traucējumi, zobu sāpes, piena sēnīte
- nieze, pārmērīga svīšana, izsitumi
- elpas trūkums, iekaisis kakls
- leikocītu un sarkano asins šūnu skaita samazināšanās, asinsspiediena paaugstināšanās vai pazemināšanās, reti paātrināta sirdsdarbība
- muskuļu sāpes, muguras sāpes
- nogurums
Retākas blakusparādības (var skart līdz 1 no 100 cilvēkiem):
- kairinājums vai iekaisis kakls,
- trombocītu skaita samazināšanās
- eiforijas sajūta, nervozitāte, vispār neparasti, uzbudinājums vai palēnināšanās; redzes vai dzirdes halucinācijas, samazināts apziņas līmenis, garīgā stāvokļa izmaiņas, atkarība (atkarība no zālēm, atkarība), dezorientācija, koncentrēšanās trūkums, līdzsvara zudums, reibonis, grūtības runāt, troksnis ausīs, diskomforts ausīs
- redzes traucējumi vai neskaidra redze, acu apsārtums
- neparasti lēns sirdsdarbības ātrums, ļoti karsta sajūta (karstuma viļņi)
- smaga sēkšana, apgrūtināta elpošana miega laikā
- viens vai vairāki no šiem mutes traucējumiem: čūlas, sajūtu zudums, diskomforts, krāsas izmaiņas, mīksto audu bojājumi, sāpes mēlē, tulznas vai mēles čūlas, smaganu sāpes, sausas lūpas vai sasprēgājuši, zobu bojājumi
- barības vada iekaisums, zarnu paralīze, žultspūšļa darbības traucējumi
- auksti sviedri, sejas pietūkums, vispārējs nieze, matu izkrišana, muskuļu raustīšanās, muskuļu vājums, slikta dūša, diskomforts krūtīs, slāpes, aukstuma vai karstuma sajūta, grūtības urinēt
- slimība
- apsārtums
Retas blakusparādības (var skart līdz 1 no 1000 cilvēkiem):
- domāšanas traucējumi, kustību traucējumi
- tulznas mutē, sausas lūpas, strutas savākšana zem mutes gļotādas
- testosterona trūkums, patoloģiskas sajūtas acī, redzot gaismas zibspuldzes, trauslus nagus
- alerģiskas reakcijas, piemēram, izsitumi, apsārtums, lūpu un sejas pietūkums, nātrene
Biežums nav zināms:
- samaņas zudums, elpošanas apstāšanās, krampji (krampji)
Ziņošana par blakusparādībām
Ja Jums rodas jebkādas blakusparādības, konsultējieties ar ārstu vai farmaceitu. Tas attiecas arī uz iespējamām blakusparādībām, kas nav minētas šajā instrukcijā. Jūs varat ziņot par blakusparādībām arī tieši, izmantojot V pielikumā minēto valsts ziņošanas sistēmu. Ziņojot par blakusparādībām, jūs varat palīdzēt iegūt vairāk informācijas par šo zāļu drošumu.
Derīguma termiņš un saglabāšana
Effentora sastāvā esošā pretsāpju sastāvdaļa ir ļoti spēcīga un var būt dzīvībai bīstama, ja to nejauši lieto bērns. Šīs zāles jāuzglabā bērniem neredzamā un nepieejamā vietā.
- Nelietot šīs zāles pēc derīguma termiņa beigām, kas norādīts uz blistera etiķetes un kastītes.
- Uzglabāt oriģinālajā iepakojumā, lai pasargātu zāles no mitruma.
- Neizmetiet zāles kanalizācijā vai sadzīves atkritumos. Jautājiet farmaceitam, kā izmest zāles, kuras vairs nelietojat. Tas palīdzēs aizsargāt vidi.
Termiņš "> Cita informācija
Ko Effentora satur
Aktīvā viela ir fentanils. Katra tablete satur:
- 100 mikrogrami fentanila (citrāta veidā)
- 200 mikrogrami fentanila (citrāta veidā)
- 400 mikrogrami fentanila (citrāta veidā)
- 600 mikrogrami fentanila (citrāta veidā)
- 800 mikrogrami fentanila (citrāta veidā)
Citas sastāvdaļas ir mannīts, A tipa cietes glikolāts, nātrija bikarbonāts, bezūdens nātrija karbonāts, bezūdens citronskābe, magnija stearāts.
Effentora ārējais izskats un iepakojums
Vaigu tabletes ir apaļas, ar plakanu virsmu un slīpu malu, vienā pusē iespiests burts "C" un skaitlis "1", ja Effentora 100 mikrogrami, "2" - Effentora 200 mikrogrami, "4" - Effentora uz 400 mikrogrami, "6" - Effentora 600 mikrogrami un "8" - Effentora 800 mikrogrami.
Katrs blisteris satur 4 vaigu tabletes, kastītē ar 4 vai 28 vaigu tabletēm.
Visi iepakojuma lielumi tirgū var nebūt pieejami.
Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī. Pašlaik pieejamā informācija var nebūt atjaunināta.
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija.
01.0 ZĀĻU NOSAUKUMS -
EFFENTORA 100 MCG ZELTA Šķīstošās tabletes
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS -
Katra mutes tablete satur 100 mikrogramus fentanila (citrāta veidā).
Palīgviela (-as) ar zināmu iedarbībuKatra tablete satur 8 mg nātrija.
Pilnu palīgvielu sarakstu skatīt apakšpunktā 6.1.
03.0 ZĀĻU FORMA -
Vaigu tablete.
Baltas, apaļas, plakanas tabletes ar slīpu malu, ar iespiestu burtu "C" vienā pusē un "1" otrā pusē.
04.0 KLĪNISKĀ INFORMĀCIJA -
04.1 Terapeitiskās indikācijas -
Effentora ir paredzēts izrāvienu sāpju (izrāviena sāpju) ārstēšanai pieaugušajiem ar vēzi, kuri jau saņem opioīdu uzturošo terapiju hronisku vēža sāpju gadījumā.
"Pārejošs sāpju paasinājums" vai "izrāviena sāpes" nozīmē "īslaicīgu sāpju paasinājumu papildus pastāvīgām sāpēm, kas tiek kontrolētas ar citām zālēm.
Pacienti, kuri jau saņem uzturošo opioīdu terapiju, ir tie pacienti, kuri lieto vismaz 60 mg perorālā morfīna dienā, vismaz 25 mikrogramus transdermālā fentanila stundā, vismaz 30 mg oksikodona dienā, vismaz 8 mg hidromorfona dienā, vai cita opioīda devu ar vienādu pretsāpju iedarbību vismaz vienu nedēļu.
04.2 Devas un lietošanas veids -
Ārstēšana jāsāk un jāturpina ārsta vadībā, kam ir pieredze opioīdu terapijas ārstēšanā vēža slimniekiem. Ārstiem jāapzinās fentanila ļaunprātīgas izmantošanas iespēja. Pacienti jābrīdina, ka DEI ārstēšanai vienlaikus nedrīkst lietot divus dažādus fentanila preparātus un, pārejot uz Effentora, jāiznīcina visi DEI paredzētie fentanila preparāti. Lai izvairītos no apjukuma un iespējamās pārdozēšanas, pacientiem jāsamazina tablešu stiprumu skaits, kas vienlaicīgi pieejams pacientiem.
Devas
Devas titrēšana
Effentora deva jāpielāgo katrā gadījumā atsevišķi, līdz tiek iegūta "optimāla" deva, kas nodrošina "adekvātu atsāpināšanu un vienlaikus samazina blakusparādības. Klīniskajos pētījumos nebija iespējams paredzēt optimālo devu." pamatojoties uz ikdienas apkopes opioīdu.
Pacienti rūpīgi jāuzrauga, līdz tiek atrasta optimālā deva.
Devas titrēšana pacientiem, kuri pēc citu fentanila zāļu lietošanas nepārslēdzas uz Effentora
Sākotnējai Effentora devai jābūt 100 mikrogramiem, pēc vajadzības palielinot, pamatojoties uz pieejamām stiprībām (100, 200, 400, 600 un 800 mikrogramu tabletes).
Devas titrēšana pacientiem, kuri pēc citu fentanila zāļu lietošanas pāriet uz Effentora
Sakarā ar to atšķirīgo absorbcijas profilu, pāreja no vienas zāles uz otru nav jāveic proporcijā 1: 1. Pārejot no cita perorāla fentanila citrāta preparāta, neatkarīga Effentora devu titrēšana, jo abu produktu bioloģiskā pieejamība ir ievērojami atšķirīga. Tomēr šiem pacientiem var apsvērt sākuma devu, kas lielāka par 100 mcg.
Devas titrēšanas metode
Meklējot optimālo devu, ja 30 minūšu laikā no vienas tabletes lietošanas sākuma netiek panākta atbilstoša atsāpināšana, jāizmanto otra tāda paša stipruma Effentora tablete.
Ja BTP epizodes ārstēšanai nepieciešama vairāk nekā viena tablete, nākamajā BTP epizodē jāapsver devas palielināšana, izmantojot nākamo augstāko zāļu koncentrāciju.
Meklējot optimālo devu, var izmantot dažādas tablešu kombinācijas: līdz četrām 100 mikrogramu tabletēm vai līdz četrām 200 mikrogramu tabletēm var lietot vienas BTP epizodes ārstēšanai devas titrēšanas laikā saskaņā ar šādu shēmu:
• Ja pirmā 100 mikrogramu tablete nav efektīva, pacientam var norādīt, lai nākamo BTP epizodi ārstētu ar divām 100 mikrogramu tabletēm. Ieteicams novietot vienu tableti pret katru vaigu. Ja šī deva ir optimāla, turpmāko BPH epizožu ārstēšanu var turpināt ar vienu 200 mikrogramu Effentora tableti.
• Ja viena 200 mikrogramu Effentora tablete (vai divas 100 mikrogramu tabletes) nav efektīva, pacientam var norādīt nākamo BTP epizodi ārstēt ar divām 200 mikrogramu tabletēm (vai četrām 100 mikrogramu tabletēm). Ieteicams likt divas tabletes pret katru vaigu. Ja šī deva ir atzīta par optimālo, turpmāko BPH epizožu ārstēšanu var turpināt ar vienu 400 mikrogramu Effentora tableti.
Lai titrētu 600 un 800 mikrogramu tablešu devu, jāizmanto 200 mikrogramu tabletes.
Devas, kas pārsniedz 800 mcg, nav novērtētas klīniskajos pētījumos.
Nelietojiet vairāk par divām tabletēm, lai ārstētu vienu BTP epizodi, izņemot optimālo devu fāzi, kurai var izmantot līdz četrām tabletēm, kā aprakstīts iepriekš.
Pacientiem jānogaida vismaz 4 stundas, pirms titrēšanas laikā ar Effentora jāārstē cita BTP epizode.
Uzturošā terapija
Kad ir noteikta optimālā deva, pacientiem jāturpina lietot šo stiprumu, lietojot vienu šāda stipruma tableti. Pārejošu sāpju paasinājumu epizodes laika gaitā var atšķirties, un tādēļ Effentora nepieciešamā deva var palielināties ļaundabīgā audzēja progresēšanas dēļ. Šādos gadījumos var izmantot otru tāda paša stipruma Effentora tableti. Ja otra Effentora tablete ir nepieciešama vairākas reizes pēc kārtas, parastā uzturošā deva ir jāpielāgo (kā aprakstīts turpmāk).
Pacientiem jāgaida vismaz 4 stundas, pirms uzturošās terapijas laikā ar Effentora jāārstē cita BTP epizode.
Devas pielāgošana
Effentora uzturošā deva jāpalielina, ja pacientam nepieciešama vairāk nekā viena deva vienā BTP epizodē vairākas epizodes pēc kārtas. Devas pielāgošanai piemēro tos pašus principus kā titrēšanai (kā aprakstīts iepriekš).
Fona opioīdu zāļu deva var būt jāpārskata, ja pacientam ir vairāk nekā četras BTP epizodes dienā (24 stundas).
Terapijas pārtraukšana
Effentora terapija nekavējoties jāpārtrauc, ja tā vairs nav nepieciešama.
Aknu vai nieru darbības traucējumi:
Effentora jālieto piesardzīgi pacientiem ar vidēji smagiem vai smagiem aknu vai nieru darbības traucējumiem (skatīt apakšpunktu 4.4).
Pacienti ar kserostomiju:
Pacientiem, kuriem ir kserostomija, pirms Effentora lietošanas ieteicams dzert ūdeni, lai samitrinātu muti.Ja tas neizraisa atbilstošu putošanu, var norādīt citu terapiju.
Lietošana gados vecākiem pacientiem (vecākiem par 65 gadiem)
Klīniskajos pētījumos tika atklāts, ka pacientiem, kas vecāki par 65 gadiem, bija nepieciešama mazāka optimālā deva nekā nepieciešama jaunākiem cilvēkiem. Īpaši piesardzīgi ieteicams atrast optimālu Effentora devu gados vecākiem pacientiem.
Pediatriskā populācija:
Effentora drošība un efektivitāte 0–18 gadus veciem bērniem nav noteikta. Dati nav pieejami.
Lietošanas veids
Effentora tablete, nonākot mitruma iedarbībā, izmanto putojošu reakciju, lai atbrīvotu aktīvo vielu, tāpēc pacientiem jāiesaka neatvērt blisteri, kamēr tablete nav ievietota mutē.
Blistera atvēršana
Pacienti jāinformē, lai NEMĒDINĀT tableti caur blisteri, jo tas var sabojāt vaigu tableti. Pareizais veids, kā izņemt tableti no blistera, ir šāds:
Atdaliet blistera blisteri no blistera iepakojuma, noņemot to pa perforētajām līnijām. Pēc tam vienu blisteri jāsaliek pie līnijas, kas uzdrukāta uz aizmugurējās plēves. Visbeidzot, lai noņemtu tableti, plēve ir jānoņem. Pacienti jābrīdina nemēģiniet sasmalcināt vai salauzt tableti.
Kad tablete ir izņemta no blistera iepakojuma, to nedrīkst uzglabāt, jo nevar garantēt tā integritāti, kā arī nejaušas iedarbības iespējamību.
Tabletes ievadīšana
Pacientiem jāizņem tablete no blistera un nekavējoties jāievieto visa Effentora tablete vaigu dobumā (tuvu molāram starp vaigu un smaganu).
Effentora tableti nedrīkst sūkāt, sakošļāt vai norīt, jo tas izraisītu zemāku koncentrāciju plazmā nekā tad, ja tableti lieto atbilstoši norādījumiem.
Effentora jāievieto un jātur mutē pietiekami ilgu laiku, lai tablete varētu izšķīst, kas parasti ilgst 14-25 minūtes.
Alternatīvi, tableti var novietot zem mēles (skatīt 5.2. Apakšpunktu).
Pēc 30 minūtēm Effentora tabletes atlikumu klātbūtnē tās var norīt, uzdzerot glāzi ūdens.
Laiks, kas nepieciešams, lai tablete pilnībā izjuktu pēc ievadīšanas mutē, šķiet, neietekmē sākotnējo sistēmisko fentanila iedarbību.
Turot tableti mutē, pacienti nedrīkst lietot ēdienu un dzērienus.
Mutes gļotādas kairinājuma gadījumā ieteicams mainīt tabletes stāvokli mutē.
04.3 Kontrindikācijas -
Paaugstināta jutība pret aktīvo vielu vai jebkuru no 6.1. Apakšpunktā uzskaitītajām palīgvielām.
Pacienti bez uzturošas opioīdu terapijas (skatīt 4.1. Apakšpunktu), jo pastāv paaugstināts elpošanas nomākuma risks.
Smaga elpošanas nomākums vai smaga obstruktīva plaušu slimība.
Akūtu sāpju, izņemot DEI, ārstēšana (piemēram, pēcoperācijas sāpes, galvassāpes, migrēna).
04.4 Īpaši brīdinājumi un piesardzība lietošanā -
Pacientiem un aprūpētājiem jāiemāca, ka Effentora satur tādu aktīvās sastāvdaļas daudzumu, kas var būt letāls, īpaši bērnam. Tādēļ visas tabletes jāuzglabā bērniem neredzamā un nepieejamā vietā.
Lai samazinātu ar opioīdiem saistīto nevēlamo blakusparādību risku un noteiktu optimālo devu, devas titrēšanas fāzē obligāti rūpīgi jāuzrauga pacienti veselības aprūpes speciālisti.
Ir svarīgi, lai ilgstošas darbības opioīdu terapija pacienta pastāvīgo sāpju ārstēšanai būtu stabilizēta pirms Effentora terapijas uzsākšanas un lai pacients Effentora lietošanas laikā turpinātu ilgstošas darbības opioīdu terapiju.
Elpošanas nomākums
Tāpat kā ar visiem opioīdiem, ir klīniski nozīmīgs elpošanas nomākuma risks, kas saistīts ar fentanila lietošanu opioīdu uzturošā terapijā) un / vai neatbilstoša lietošana izraisīja letālu iznākumu.
Effentora drīkst lietot tikai apstākļos, kas norādīti 4.1.
Hroniska obstruktīva plaušu slimība
Īpaši uzmanīgi jārīkojas, titrējot Effentora devu pacientiem ar ne-smagu hronisku obstruktīvu plaušu slimību vai citiem veselības stāvokļiem, kuriem ir nosliece uz elpošanas nomākumu, jo pat parasti Effentora terapeitiskās devas var vēl vairāk samazināt elpošanas spēju līdz tādam līmenim, kas var izraisīt elpošanas mazspēju. .
Paaugstināts intrakraniālais spiediens, izmaiņas apziņas stāvoklī
Effentora jāievada ļoti piesardzīgi pacientiem, kuri var būt īpaši jutīgi pret CO2 aiztures intrakraniālajiem efektiem, piemēram, tiem, kuriem ir paaugstināta intrakraniālā spiediena pazīmes vai samaņas pasliktināšanās. Opioīdi var maskēt pacienta ar galvas traumu klīnisko gaitu, un tāpēc tie jālieto tikai tad, ja ir klīniska nepieciešamība.
Sirds slimība
Intravenozi ievadīts fentanils var izraisīt bradikardiju. Effentora klīniskajos pētījumos nebija skaidru pierādījumu par bradikardiju. Tomēr Effentora jālieto piesardzīgi pacientiem, kuriem jau ir bradiaritmija.
Aknu vai nieru darbības traucējumi
Turklāt Effentora piesardzīgi jāievada pacientiem ar aknu vai nieru mazspēju. Aknu un nieru mazspējas ietekme uz zāļu farmakokinētiku nav novērtēta, bet pēc intravenozas ievadīšanas fentanila klīrenss tika mainīts metabolisma klīrensa un plazmas olbaltumvielu izmaiņu dēļ. Pēc Effentora lietošanas gan nieru, gan aknu mazspēja var palielināt uzņemtā fentanila biopieejamību un samazināt tā sistēmisko klīrensu, kā rezultātā var palielināties un pagarināties opioīdu iedarbība. Līdz ar to īpaša piesardzība jāievēro devas titrēšanas posmā pacientiem ar mērena vai smaga aknu vai nieru mazspēja.
Īpaša uzmanība jāpievērš pacientiem ar hipovolemiju un hipotensiju.
Iecietība, atkarība
Pēc atkārtotas opioīdu, piemēram, fentanila, lietošanas var attīstīties fiziska un / vai psiholoģiska atkarība. Tomēr jatrogēna atkarība pēc opioīdu terapeitiskas lietošanas ir reta.
Kontrolēta nātrija diēta
Šīs zāles vienā tabletē satur 8 mg nātrija.
Tas jāpatur prātā pacientiem, kuri ievēro diētu ar zemu nātrija saturu.
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi -
Fentanils tiek metabolizēts galvenokārt caur citohroma P450 3A4 (CYP3A4) izoenzīmu sistēmu, un tāpēc mijiedarbība var rasties, ja Effentora lieto vienlaikus ar līdzekļiem, kas ietekmē CYP3A4 aktivitāti. Vienlaicīga līdzekļu lietošana, kas inducē CYP3A4 aktivitāti, var samazināt Effentora efektivitāti. Vienlaicīga Effentora un spēcīgu CYP3A4 inhibitoru (piemēram, ritonavīra, ketokonazola, itrakonazola, troleandomicīna, klaritromicīna un nelfinavira) lietošana vai mērena (piem., Amprenavirs, aprepitants, diltiazems, eritromicīns, flamprenazols, fosfāts) var palielināt plazmas koncentrāciju , izraisot iespējamas nopietnas zāļu blakusparādības, tostarp letālu elpošanas nomākumu. Pacienti, kuri tiek ārstēti ar Effentora kopā ar spēcīgiem un mēreniem CYP3A4 inhibitoriem, ilgstoši rūpīgi jānovēro. "Devas palielināšana jāveic piesardzīgi.
Vienlaicīga lietošana ar citiem CNS nomācošiem līdzekļiem, ieskaitot citus opioīdus, sedatīvus vai miega līdzekļus, vispārējos anestēzijas līdzekļus, fenotiazīnus, trankvilizatorus, muskuļu un skeleta relaksantus, sedatīvus antihistamīna līdzekļus un alkoholu, var izraisīt papildu nomācošu iedarbību.
Effentora nav ieteicams lietot pacientiem, kuri iepriekšējo 14 dienu laikā ir lietojuši monoamīnoksidāzes (MAO) inhibitorus, jo ziņots par spēcīgu un neparedzamu MAO inhibitoru pastiprināšanos, lietojot opioīdu pretsāpju līdzekļus.
Nav ieteicama vienlaicīga daļēju opioīdu agonistu / antagonistu (piemēram, buprenorfīna, nalbufīna, pentazocīna) lietošana. Tiem piemīt augsta afinitāte pret opioīdu receptoriem un salīdzinoši zema raksturīgā aktivitāte, tāpēc tie daļēji antagonizē fentanila pretsāpju iedarbību un var izraisīt abstinences simptomus pacientiem, kas ir atkarīgi no opioīdiem.
04.6 Grūtniecība un zīdīšanas periods -
Grūtniecība
Nav pietiekamu datu par fentanila lietošanu grūtniecēm. Pētījumi ar dzīvniekiem parādīja reproduktīvo toksicitāti (skatīt 5.3. Apakšpunktu). Iespējamais risks cilvēkiem nav zināms. Effentora nedrīkst lietot grūtniecības laikā, grūtniecības laikā, ja vien tas nav absolūti nepieciešams.
Ilgstoši lietojot, fentanils jaundzimušajam var izraisīt abstinences sindromu.
Dzemdību un dzemdību laikā (ieskaitot ķeizargriezienu) nav ieteicams lietot fentanilu, jo fentanils šķērso placentu un var izraisīt augļa elpošanas nomākumu. Lietošanas gadījumā jaundzimušajam jābūt viegli pieejamam pretlīdzeklim.
Barošanas laiks
Fentanils nonāk mātes pienā un var izraisīt sedāciju un elpošanas nomākumu zīdainim, kas baro bērnu ar krūti. Sievietes, kas baro bērnu ar krūti, nedrīkst lietot fentanilu, un zīdīšanu nedrīkst atsākt vismaz 48 stundas pēc pēdējās fentanila lietošanas.
Auglība
Nav datu par auglību cilvēkiem. Pētījumos ar dzīvniekiem vīriešu auglība tika nelabvēlīgi ietekmēta (skatīt 5.3. Apakšpunktu).
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus -
Nav veikti pētījumi par spēju vadīt transportlīdzekļus un apkalpot mehānismus, tomēr opioīdu pretsāpju līdzekļi pasliktina garīgās un / vai fiziskās spējas, kas nepieciešamas, lai veiktu potenciāli bīstamas darbības (piemēram, vadot transportlīdzekļus vai apkalpojot mehānismus). Pacientiem jāiesaka nevadīt transportlīdzekļus un neapkalpot mehānismus, ja Effentora terapijas laikā ir miegainība, reibonis vai redzes traucējumi, un nevadīt transportlīdzekļus un neapkalpot mehānismus, kamēr nav pārbaudīta reakcija uz zālēm.
04.8 Nevēlamās blakusparādības -
Drošības profila kopsavilkums
Lietojot Effentora, var sagaidīt tipiskas opioīdu grupas zāļu blakusparādības. Bieži vien šie efekti izzūd vai samazinās, turpinot zāļu lietošanu, kad tiek atrasta optimālā deva pacientam. Tomēr visnopietnākās blakusparādības ir elpošanas nomākums (kas var izraisīt apnoja vai elpošanas apstāšanos), asinsrites nomākums, hipotensija un šoks, un tāpēc visi pacienti rūpīgi jānovēro, lai noteiktu šīs sekas.
Effentora klīniskie pētījumi tika izstrādāti, lai novērtētu tā drošību un efektivitāti BPH ārstēšanā, un visi pacienti vienlaikus lietoja citas opioīdu zāles, piemēram, ilgstošas darbības morfīnu vai transdermālu fentanilu, lai kontrolētu hroniskas sāpes. Tādēļ ir iespējams galīgi noteikt nošķirt efektus, kas saistīti tikai ar Effentora.
Blakusparādību tabula
Klīniskajos pētījumos un pēcreģistrācijas periodā ziņots par šādām blakusparādībām, lietojot Effentora. Blakusparādības ir uzskaitītas pēc orgānu sistēmas un biežuma saskaņā ar MedDRA terminoloģiju un konvenciju. Biežums ir definēts kā: ļoti bieži (≥1 / 10), bieži (≥ 1/100 un
Izvēlēto blakusparādību apraksts
Atkārtoti lietojot opioīdus, piemēram, fentanilu, var attīstīties fiziska un / vai psiholoģiska tolerance un atkarība.
Pētījumos ar Effentora tika novēroti zāļu lietošanas pārtraukšanas simptomi, piemēram, slikta dūša, vemšana, caureja, trauksme un trīce.
Pārdozēšanas gadījumā tika novērots samaņas zudums un elpošanas apstāšanās.
04.9 Pārdozēšana -
Fentanila pārdozēšanas simptomi pēc būtības ir līdzīgi tiem, kas novēroti fentanila un citu intravenozi ievadītu opioīdu simptomiem, un tie sastāv no tā farmakoloģiskās iedarbības pagarināšanās, un vissmagākā nozīmīgā ietekme ir izmainīts garīgais stāvoklis, samaņas zudums, hipotensija, elpošanas nomākums, elpošanas traucējumi ciešanas un elpošanas mazspēja, kam sekoja nāve.
Tūlītēja opioīdu pārdozēšanas ārstēšana sastāv no Effentora vaigu tabletes izņemšanas, ja tā joprojām atrodas mutē, nodrošinot, ka elpceļi ir brīvi, pacienta verbālā un fiziskā stimulācija, apziņas līmeņa, ventilācijas un asinsrites stāvokļa novērtēšana, kā arī veicināta ventilācija (ventilācija atbalstu), ja nepieciešams.
Pārdozēšanas (nejaušas norīšanas) ārstēšanai cilvēkiem, kuri nekad nav lietojuši opioīdus, ir nepieciešama intravenoza piekļuve un ārstēšana ar naloksonu vai citu opioīdu antagonistu saskaņā ar klīniskām indikācijām. Elpošanas nomākuma ilgums pēc zāļu pārdozēšanas var būt ilgāks nekā opioīdu antagonista iedarbība (piemēram, naloksona eliminācijas pusperiods ir no 30 līdz 81 minūtei), un tāpēc tas var būt jāatkārto. Informāciju par tā lietošanu šajā gadījumā skatiet atsevišķā opioīdu antagonista zāļu aprakstā.
Pārdozēšanas ārstēšanai pacientiem, kuri jau ir ārstēti ar opioīdiem, ir jānodrošina intravenoza piekļuve. Saprātīga naloksona vai cita opioīdu antagonista lietošana dažos gadījumos var būt pamatota, taču tas ir saistīts ar risku izraisīt akūtu abstinences sindromu.
Lai gan pēc Effentora lietošanas netika novērots muskuļu stīvums, kas traucē elpošanu, tas ir iespējams, lietojot fentanilu un citus opioīdus. Šādā gadījumā tas jāārstē ar palīdzību ventilāciju, opioīdu antagonistu un, kā pēdējo alternatīvu, ar neiromuskulāro blokatoru.
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS -
05.1 "Farmakodinamiskās īpašības -
Farmakoterapeitiskā grupa: pretsāpju līdzekļi; opioīdi; ATĶ kods N02AB03.
Fentanils ir opioīdu pretsāpju līdzeklis, kas galvenokārt mijiedarbojas ar opioīdu µ-receptoriem. Tās galvenās terapeitiskās darbības ir atsāpināšana un sedācija.Sekundārā farmakoloģiskā iedarbība ir: elpošanas nomākums, bradikardija, hipotermija, aizcietējums, mioze, atkarība un eiforija.
Fentanila pretsāpju iedarbība ir saistīta ar tā līmeni plazmā. Kopumā efektīvā koncentrācija un toksiskā koncentrācija palielinās, palielinoties tolerancei pret opioīdiem. Līdz ar to Effentora deva ir jātitrē katram pacientam, lai sasniegtu vēlamo efektu (skatīt 4.2. Apakšpunktu).
Visi opioīdu µ-receptoru agonisti, ieskaitot fentanilu, izraisa elpošanas nomākumu, kas ir atkarīgs no devas. Elpošanas nomākuma risks pacientiem, kuri saņem hronisku opioīdu terapiju, ir mazāks, jo šiem pacientiem attīstīsies tolerance pret zālēm, kas ir atbildīgas par elpošanas nomākumu.
Effentora drošums un efektivitāte ir novērtēta pacientiem, kuri lietoja zāles sāpju paasinājuma epizodes sākumā.Effentora profilaktiska lietošana paredzamu sāpju epizožu laikā nav pētīta. Divi dubultmaskēti, randomizēti, placebo kontrolēti krustošanās pētījumi tika veikti kopā 248 pacientiem, kuri slimo ar BPH un vēzi un kuriem bija vidēji 1 līdz 4 BPH epizodes dienā, vienlaikus ārstējot ar opioīdu balstterapiju terapija. Sākotnējā atklātā fāzē katram pacientam tika noteikta optimālā Effentora deva. Pacienti, kuriem tika noteikta optimālā deva, pārcēlās uz pētījuma dubultmaskēto fāzi. Galvenais efektivitātes mainīgais lielums bija pacienta sāpju intensitātes novērtējums. Pacienti sāpes novērtēja 11 ballu skalā. Katrai BTP epizodei sāpju intensitāte tika novērtēta gan pirms ievadīšanas, gan dažādos laika intervālos pēc tās.
Optimālu devu varētu noteikt 67% pacientu.
Pivotālajā klīniskajā pētījumā (1. pētījums) galvenais parametrs, ko attēlo sāpju intensitātes rādītāju atšķirību summas vidējais rādītājs no zāļu lietošanas brīža līdz 60 minūtēm ieskaitot (SPID60), bija statistiski nozīmīgs salīdzinājumā ar placebo (P.
Otrajā galvenajā pētījumā (2. pētījums) galvenais parametrs bija SPID30, kas arī bija statistiski nozīmīgs salīdzinājumā ar placebo (P.
Statistiski nozīmīgs sāpju intensitātes atšķirību uzlabojums tika novērots, lietojot Effentora, salīdzinot ar placebo, jau 10 minūtes 1. pētījumā un jau 15 minūtes (pirmais konstatētais intervāls) 2. pētījumā. Šie novērojumi palika nozīmīgi katrā nākamajā intervālā. Abos pētījumos .
05.2 "Farmakokinētiskās īpašības -
Vispārējs ievads
Fentanils ir ļoti lipofils un var ļoti ātri uzsūkties no mutes gļotādas un lēnāk, izmantojot parasto kuņģa -zarnu trakta ceļu. Tas tiek pakļauts aknu un zarnu pirmā metabolisma metabolismam, un tā metabolīti neveicina tā terapeitisko iedarbību.
Effentora izmanto aktīvās sastāvdaļas izdalīšanās paņēmienu, kurā tiek izmantota putojoša reakcija, kas uzlabo fentanila uzsūkšanās ātrumu un daudzumu caur mutes gļotādu. Pārejošas pH izmaiņas, kas pavada putojošo reakciju, var optimizēt tablešu izšķīšanu (ar zemāku pH) un membrānas caurlaidību (ar augstāku pH).
Uzturēšanās laiks (definēts kā laiks, kas nepieciešams, lai tablete pilnībā sadalītos pēc iekšķīgas lietošanas) neietekmē vispārējās fentanila iedarbības priekšlaicību. Salīdzinošs pētījums starp Effentora tabletēm 400 mcg gan vaigu (ti, starp vaigu un smaganu), kas zem mēles atbilst bioekvivalences kritērijiem.
Nieru vai aknu darbības traucējumu ietekme uz Effentora farmakokinētiku nav pētīta.
Uzsūkšanās
Pēc Effentora mutes dobuma ievadīšanas fentanils viegli uzsūcas, un tā absolūtā biopieejamība ir 65%. Effentora uzsūkšanās profils lielā mērā ir saistīts ar ātru sākotnējo uzsūkšanos no mutes gļotādas, maksimālā koncentrācija plazmā tiek sasniegta pēc venozas izņemšanas parasti vienas stundas laikā pēc ievadīšanas mutē. Aptuveni 50% no kopējās ievadītās devas ātri uzsūcas caur gļotādu Pārējie 50% no kopējās devas tiek uzņemti un lēni uzsūcas caur kuņģa -zarnu traktu. Aptuveni 30% no uzņemtā daudzuma (50% no kopējās devas) izkļūst caur aknām un zarnām un kļūst pieejami sistēmiski.
Galvenie farmakokinētiskie parametri ir parādīti tabulā zemāk.
Farmakokinētiskie parametri * pieaugušajiem, kas ārstēti ar Effentora
* Attiecas uz venozo asiņu (plazmas) paraugiem. Fentanila citrāta koncentrācija serumā bija augstāka nekā koncentrācija plazmā: serumā AUC un Cmax bija attiecīgi aptuveni par 20% un 30% augstākas nekā koncentrācija plazmā. Šīs atšķirības iemesls nav zināms.
** Tmax dati ir norādīti kā mediāna (diapazons).
Farmakokinētikas pētījumos, kas tika veikti, lai salīdzinātu Effentora un perorāli transmukozālā fentanila citrāta (OTFC) absolūto un relatīvo biopieejamību, fentanila uzsūkšanās ātrums un apjoms Effentora uzrādīja par 30–50% lielāku iedarbību nekā OTFC. Pārejot no cita fentanila citrāta preparāta, jāveic neatkarīga Effentora devas titrēšana, jo produktu bioloģiskā pieejamība ir ievērojami atšķirīga. Tomēr šiem pacientiem var apsvērt devu, kas lielāka par 100 mikrogramiem.
Ekspozīcijas atšķirības tika novērotas Effentora klīniskajā pētījumā, kas tika veikts pacientiem ar 1. pakāpes mukozītu. Cmax un AUC0-8 bija attiecīgi par 1% un 25% augstāki pacientiem ar mukozītu nekā tiem, kuriem nebija mukozīta. Novērotās atšķirības nebija klīniski nozīmīgas.
Izplatīšana
Fentanils ir ļoti lipofils un viegli izplatās ārpus asinsvadu sistēmas, ar lielu šķietamo izkliedes tilpumu. Pēc Effentora iekšķīgas lietošanas fentanils sāk strauji izplatīties, kas izsaka fentanila līdzsvaru starp plazmu un audiem ar augstu perfūziju (smadzenes, sirds un plaušas). Pēc tam fentanils tiek pārdalīts starp dziļo audu nodalījumu (muskuļiem un taukiem) un plazmu.
Fentanila saistīšanās ar plazmas olbaltumvielām svārstās no 80% līdz 85%. Galvenais saistošais proteīns ir alfa-1-skābes glikoproteīns, bet daļēji veicina arī albumīns un lipoproteīni.Brīvā fentanila daļa palielinās līdz ar acidozi.
Biotransformācija
Metabolisma ceļi pēc Effentora iekšķīgas lietošanas klīniskajos pētījumos nav raksturoti. Fentanils tiek izvadīts aknās un zarnu gļotādā par norfentanilu, izmantojot izoforma CYP3A4. Pētījumos ar dzīvniekiem norfentanils nav farmakoloģiski aktīvs. Vairāk nekā 90% no ievadītās fentanila devas pēc biotransformācijas tiek izvadīti par neaktīviem N-dealkilētiem metabolītiem un hidroksilātiem.
Eliminācija
Pēc fentanila intravenozas ievadīšanas mazāk nekā 7% no ievadītās devas izdalās nemainītā veidā ar urīnu un tikai aptuveni 1% no izkārnījumiem.
Pēc Effentora lietošanas fentanila galīgā eliminācijas fāze ir pārdalīšanās starp plazmu un dziļo audu nodalījumu rezultāts. Šī eliminācijas fāze ir lēna, un vidējais beigu eliminācijas pusperiods t½ ir aptuveni 22 stundas pēc vaigu ievadīšanas. un aptuveni 18 stundas pēc intravenozas ievadīšanas. Kopējais fentanila plazmas klīrenss pēc intravenozas ievadīšanas ir aptuveni 42 l / h.
Linearitāte / nelinearitāte
Ir pierādīta devu proporcionalitāte no 100 līdz 1000 mcg.
05.3 Preklīniskie drošības dati -
Pamatojoties uz tradicionālajiem pētījumiem, neklīniskie dati neliecina par īpašu risku cilvēkam drošības farmakoloģija, atkārtotu devu toksicitāte, genotoksicitāte un kancerogenitāte.
Embrija-augļa attīstības toksicitātes pētījumi, kas veikti žurkām un trušiem, neatklāja malformācijas vai izmaiņas attīstībā, ko izraisīja zāles organoģenēzes laikā.
Auglības un agrīnas embrionālās attīstības pētījumā ar žurkām un trušiem, lietojot lielas devas (300 mcg / kgnomirt,s.c.), un pētījumos ar dzīvniekiem to uzskata par sekundāru fentanila nomierinošajai iedarbībai.
Pirms un pēcdzemdību attīstības pētījumos ar žurkām pēcnācēju izdzīvošana tika ievērojami samazināta, lietojot devas, kas izraisīja smagu toksisku ietekmi uz mātīti. Papildu atklājumi, lietojot mātēm toksiskas devas, bija palēnināta fiziskā attīstība, maņu funkcijas, refleksi un uzvedība pirmās paaudzes pēcnācējiem. Šī ietekme var būt netieša, jo ir traucēta mātes aprūpe un / vai samazināta zīdīšana, vai arī fentanila tiešas sekas pēcnācējiem.
Kancerogenitātes pētījumi (alternatīvs ādas bioloģiskais tests Tg.AC 26 nedēļu transgēnām pelēm; 2 gadus vecs subkutānas kancerogenitātes pētījums ar žurkām) neatklāja nekādus konstatējumus, kas liecinātu par onkogēnu potenciālu.
06.0 FARMACEITISKĀ INFORMĀCIJA -
06.1 Palīgvielas
Mannīts
A tipa nātrija cietes glikolāts
Nātrija bikarbonāts
Bezūdens nātrija karbonāts
Bezūdens citronskābe
Magnija stearāts
06.2 Nesaderība "-
Nav būtisks.
06.3 Derīguma termiņš "-
3 gadi.
06.4 Īpaši uzglabāšanas nosacījumi -
Uzglabāt oriģinālajā iepakojumā, lai pasargātu no mitruma.
06.5 Tiešā iepakojuma veids un iepakojuma saturs -
PVC laminēts alumīnija blisteris / alumīnija folija / poliamīds / PVC papīrs / poliestera pārklājums.
Blistera iepakojumi ir kastītēs pa 4 vai 28 tabletēm.
Visi iepakojuma lielumi tirgū var nebūt pieejami.
06.6 Lietošanas un lietošanas instrukcijas -
Pacientiem un aprūpētājiem jāiesaka atbrīvoties no atlikušajām tabletēm, kad tās vairs nav vajadzīgas.
Zāles lietotas vai nelietotas, jo tās vairs nav vajadzīgas, un no šīm zālēm radušies atkritumi jāiznīcina saskaņā ar vietējiem noteikumiem.
07.0 "REĢISTRĀCIJAS APLIECĪBAS" ĪPAŠNIEKS
TEVA Pharma B.V.
Computerweg 10
3542DR Utrehta
Nīderlande
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS -
EU/1/08/441/001 - AIC Nr. 038660015
EU/1/08/441/002 - AIC Nr. 038660027
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS -
Reģistrācijas datums: 2008. gada 4. aprīlis
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS -
2013. gada februāris